Clear Sky Science · it
Nanozima mimetico della granzima B per applicazioni antitumorali mirate tramite nanovesichette
Reinventare gli assassini naturali del corpo
Il nostro sistema immunitario dispone di cellule specializzate in grado di individuare e uccidere le cellule tumorali, ma in molti tumori solidi faticano a penetrare, si esauriscono rapidamente o attaccano bersagli sbagliati. Questo studio descrive un sistema completamente artificiale su scala nanometrica che imita una delle armi più potenti del sistema immunitario e la consegna direttamente all'interno delle cellule tumorali. Il lavoro è importante perché indica la strada verso terapie antitumorali che si comportano come cellule immunitarie viventi, pur essendo realizzate con materiali stabili e controllabili anziché con cellule umane fragili.
Trasformare un assassino naturale in un progetto
Le cellule T citotossiche, un tipo di globulo bianco, uccidono le cellule pericolose usando un enzima chiamato granzima B. Una volta riconosciuto il bersaglio, praticano piccoli fori nella sua membrana e iniettano la granzima B, che attiva i programmi di suicidio all'interno della cellula. Questa strategia è alla base di terapie moderne come le cellule CAR-T, in grado di curare alcuni tumori del sangue. Tuttavia, nei tumori solidi le CAR-T spesso falliscono perché non raggiungono tutte le regioni tumorali, si esauriscono o colpiscono tessuti sani per errore. Gli autori si sono chiesti se fosse possibile costruire un dispositivo non vivente su scala nanometrica che riproduca la funzione chiave della granzima B — attivare il meccanismo di autodistruzione cellulare — senza dipendere dalle cellule T viventi.
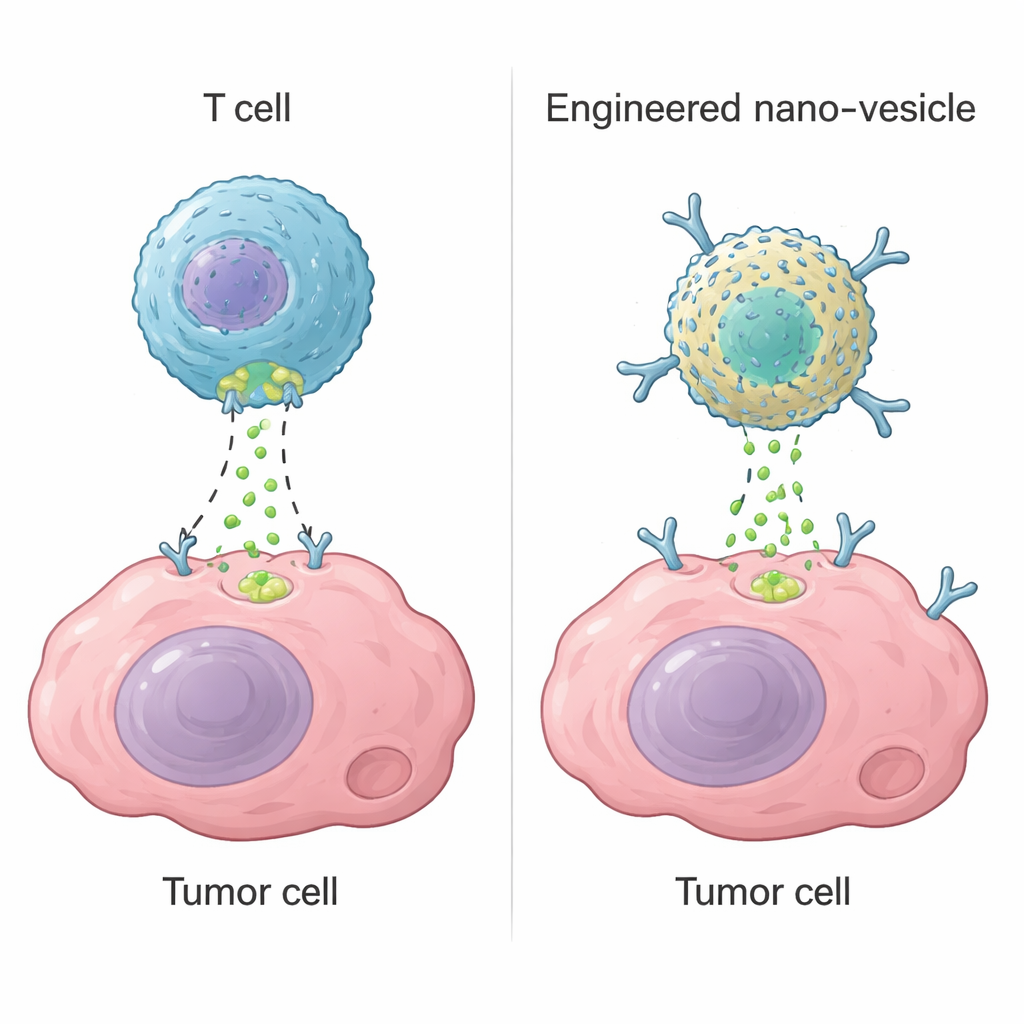
Progettare un piccolo enzima artificiale
Il gruppo è partito dalla ferritina, una proteina naturale che forma nanocassette cave ed è facile da produrre in grandi quantità. Legando ioni di palladio alla ferritina umana, hanno creato un “nanozima” con comportamento simile a un enzima. Studi strutturali accurati hanno rivelato che due atomi di palladio si sistemano in una tasca specifica sulla superficie della proteina, trattenuti da amminoacidi contenenti zolfo e azoto e da molecole d'acqua. Questo centro metallico binucleare funge da sito di taglio artificiale che riconosce la stessa breve sequenza usata dalla granzima B su un bersaglio cruciale noto come caspasi-3. In test di laboratorio il nanozima ha clivato efficacemente la caspasi-3 nella posizione corretta, attivandola, mentre ignorava proteine strettamente correlate. L'enzima artificiale era leggermente meno efficiente della granzima B naturale ma notevolmente più stabile su un ampio intervallo di temperature e acidità.
Introdurre di nascosto il nanozima nelle cellule tumorali
Enzimi come la granzima B funzionano solo se raggiungono l'interno delle cellule tumorali. Per ottenerlo, i ricercatori hanno incapsulato il loro nanozima palladio–ferritina all'interno di nanovesicole lipidiche — piccole bolle morbide fatte di molecole simili ai grassi. Hanno quindi rivestito queste vescicole con frammenti di anticorpi che riconoscono HER2, una proteina spesso sovraespressa nelle cellule di tumori al seno e alla vescica. Quando queste vescicole camuffate incontrano cellule ricche di HER2, si legano saldamente e si fondono con la membrana cellulare, permettendo al carico di nanozima di scivolare direttamente nel citoplasma invece di rimanere intrappolato e digerito nei compartimenti di riciclo cellulare. La microscopia ha mostrato le vescicole ferme sulla superficie cellulare mentre il nanozima diffondeva all'interno, predisponendo l'ambiente per un'autodistruzione controllata dall'interno.
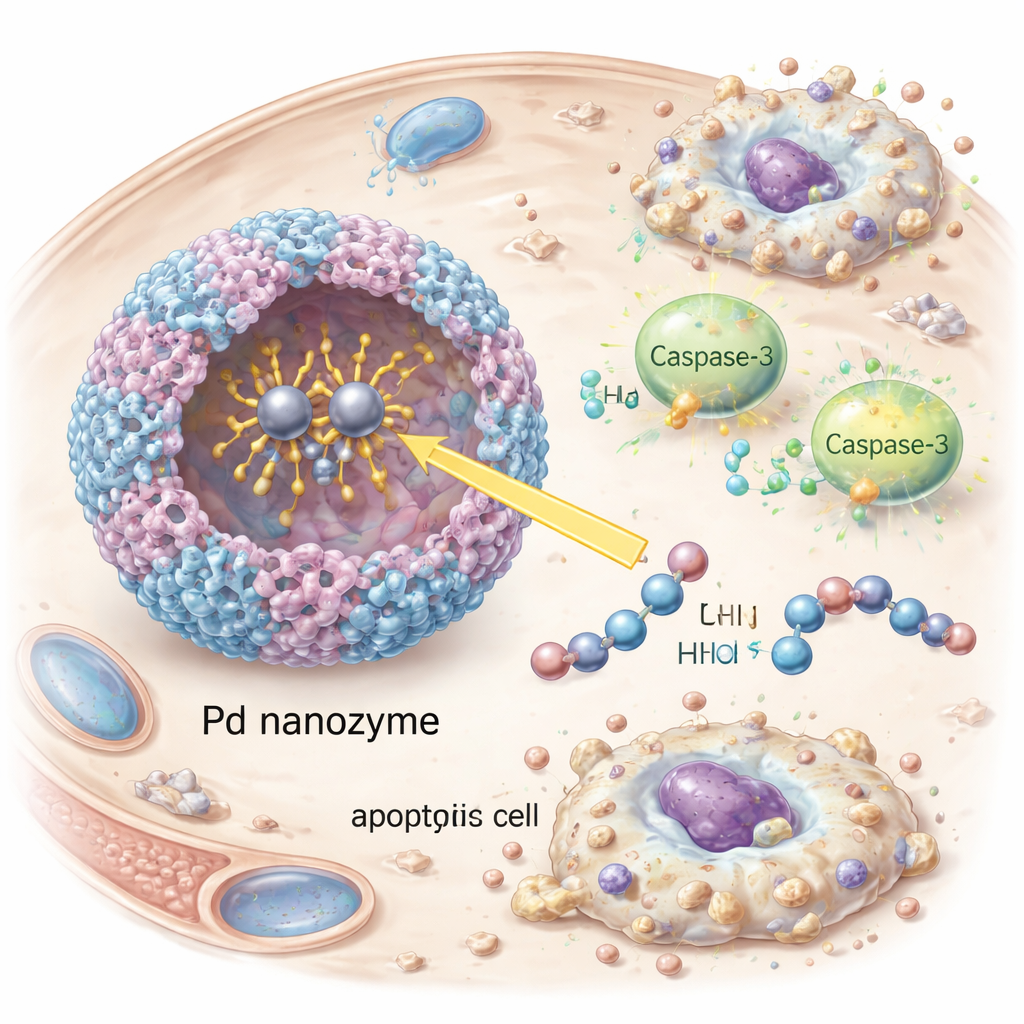
Innescare il suicidio delle cellule tumorali con precisione
Una volta all'interno delle cellule tumorali, il nanozima ha attivato la caspasi-3, un esecutore centrale della morte cellulare programmata. I ricercatori hanno osservato la comparsa di caspasi-3 attivata e del suo bersaglio a valle PARP, oltre a chiari segni di apoptosi — cellule che si restringono e si frammentano — in colture di cellule tumorali HER2-positive. Silenziare la caspasi-3 con interferenza a RNA ha ridotto drasticamente la morte cellulare, confermando che l'effetto dipendeva da questa via piuttosto che da danni non specifici. In topi portatori di tumori HER2-positivi, le vescicole decorate con anticorpi sono rimaste più a lungo in circolo, si sono accumulate maggiormente nei tumori e hanno rallentato la crescita tumorale in modo più efficace rispetto a vescicole prive degli anticorpi bersaglio o del carico di nanozima. È importante che gli animali trattati non mostrassero perdita di peso evidente, anomalie del sangue o danni ai tessuti negli organi principali, suggerendo un profilo di sicurezza favorevole in questi test iniziali.
Cosa potrebbe significare per la cura del cancro in futuro
Per i non specialisti, il messaggio centrale è che i ricercatori hanno costruito un piccolo dispositivo non vivente che si comporta come una parte chiave del macchinario immunitario che uccide il cancro. Invece di ingegnerizzare cellule T viventi, hanno progettato un nanoenzima stabile che attiva la stessa “leva di suicidio” all'interno delle cellule tumorali e lo hanno avvolto in un involucro di consegna intelligente che si dirige verso specifici tumori. Pur restando molto lavoro da fare prima dell'impiego umano, questo approccio offre una piattaforma flessibile: in linea di principio il rivestimento anticorpale potrebbe essere sostituito per mirare a diversi marcatori tumorali e l'enzima artificiale potrebbe essere ulteriormente ottimizzato. Lo studio dimostra una via promettente verso un'immunoterapia senza cellule, in cui nanomateriali progettati con cura, anziché cellule immunitarie vive, vengono utilizzati per cercare e distruggere tumori solidi.
Citazione: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
Parole chiave: nanomedicina oncologica, immunoterapia, granzima B, nanozima, tumori HER2-positivi