Clear Sky Science · it
Chimica bioortogonale attivata da specie reattive dell’ossigeno nei sistemi viventi resa possibile da diidrotetrazine protette con boronato
Trasformare lo stress cellulare in un interruttore preciso
Molte malattie, dal cancro ai disturbi cardiaci, si caratterizzano per cellule sotto stress ossidativo che producono alti livelli di specie reattive dell’ossigeno come il perossido di idrogeno. Questo studio mostra come i chimici possano sfruttare proprio quello stress come un interruttore incorporato per attivare terapie potenti soltanto dove sono necessarie. Progettando componenti farmacologici che reagiscono esclusivamente in questi ambienti stressati, i ricercatori mirano a uccidere le cellule tumorali o distruggere proteine dannose risparmiando i tessuti sani.
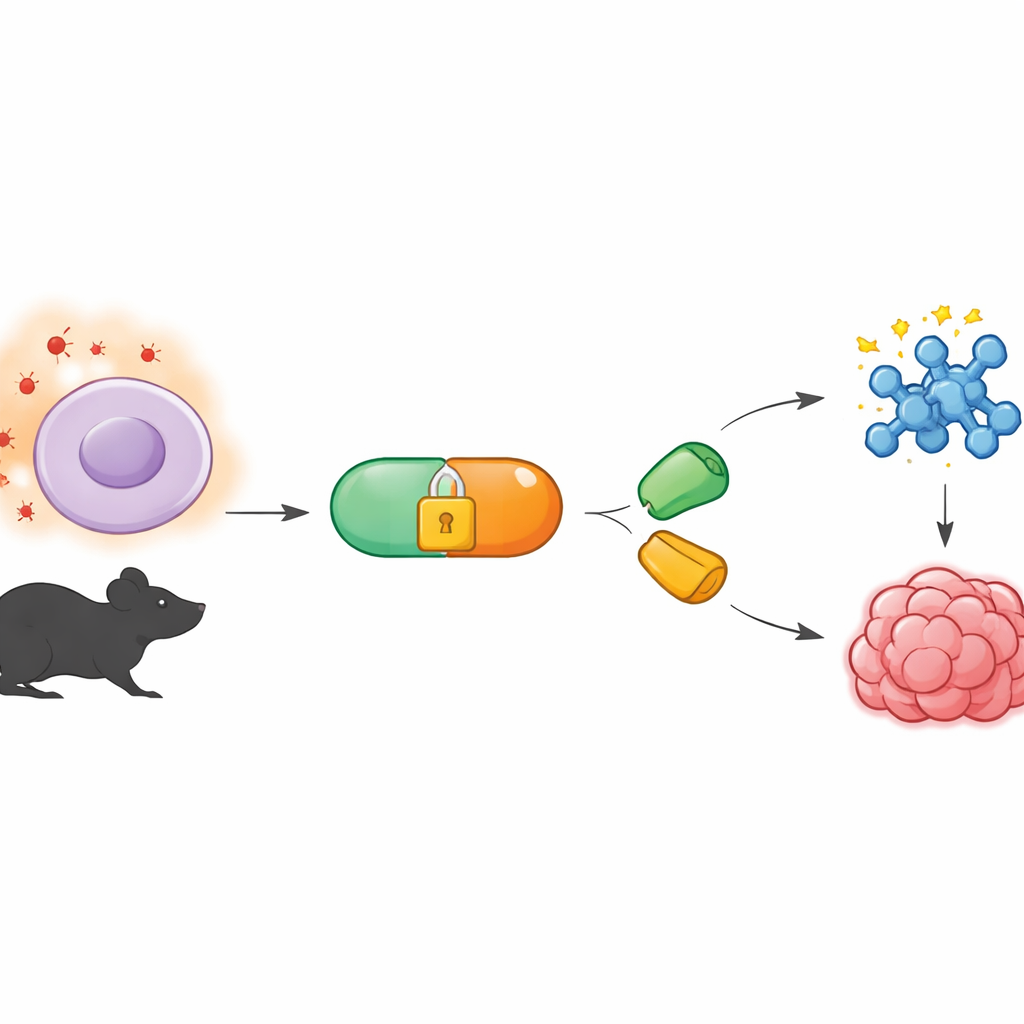
Uno strumento chimico che agisce silenziosamente in background
Il lavoro si basa su un campo chiamato chimica bioortogonale, che sviluppa reazioni in grado di avvenire all’interno di organismi viventi senza disturbare la biologia normale. Una versione molto usata impiega coppie speciali di molecole che si uniscono come pezzi di un puzzle, anche nell’intrico di una cellula. Un partner, chiamato tetrazina, reagisce molto rapidamente con un partner complementare ad anello, noto come dienofilo. Finora molte di queste reazioni sono state controllate mediante luce o aggiunta di enzimi. Gli autori hanno invece voluto un sistema che ascolti i segnali chimici del corpo—specificamente, i livelli insolitamente elevati di specie reattive dell’ossigeno riscontrati nei tumori e in altri tessuti malati.
Costruire un grilletto chimico sensibile alle ROS
Per farlo, il team ha creato precursori di tetrazina denominati BTz, chimicamente «incappucciati» in modo da rimanere inattivi nei tessuti normali. Il cappuccio è costituito da un gruppo boronato legato a una forma ridotta di tetrazina. Quando il perossido di idrogeno è scarso, BTz è stabile in acqua e in colture cellulari per molte ore. Ma quando il perossido di idrogeno è abbondante—a livelli simili a quelli misurati nei tumori—il gruppo boronato viene ossidato e si disintegra attraverso una sequenza autolimitante, rivelando la tetrazina attiva. In esperimenti in provetta, l’aumento graduale della concentrazione di perossido di idrogeno ha prodotto un corrispondente incremento nella quantità di tetrazina attiva generata, confermando che la reazione è selettiva e fortemente dipendente dalla dose.
Usare lo stress cellulare per distruggere una proteina che guida il cancro
I ricercatori hanno dapprima usato il loro interruttore per controllare una strategia farmacologica moderna chiamata degradazione mirata delle proteine. Hanno legato BTz alla talidomide, una piccola molecola che può reclutare un complesso enzimatico responsabile di marcare le proteine per lo smaltimento. Nelle cellule tumorali, questo BTz–talidomide è rimasto dormiente fino all’aumento dei livelli di perossido di idrogeno, momento in cui il cappuccio si è aperto formando una tetrazina attiva. Questa tetrazina si è poi unita rapidamente con un partner complementare legato a un farmaco che si lega a BRD4, assemblando un «chimera» più grande che trascina la proteina correlata al cancro BRD4 verso la macchina di smaltimento cellulare. In linee cellulari di cancro del polmone e della cervice, i livelli di BRD4 sono scesi nettamente solo quando tutte le parti erano presenti e il perossido di idrogeno era disponibile; bloccare le specie reattive dell’ossigeno ha impedito la degradazione, sottolineando che il processo è davvero attivato dallo stress.
Rilasciare un farmaco tossico solo dove è necessario
Successivamente, il gruppo ha trasformato la stessa chimica in un sistema di rilascio preciso per la doxorubicina, una chemioterapia potente ma dannosa per il cuore. Hanno legato la doxorubicina a un partner ad anello sottoposto a tensione, in modo che fosse bloccata in una forma pro-farmaco inattiva. Quando questo pro-farmaco incontrava BTz in un ambiente ricco di perossido di idrogeno, la tetrazina neoformata reagiva con l’anello in un processo «click-to-release», congiungendo i pezzi e liberando la doxorubicina libera. In cellule di cancro del colon coltivate in piastre, questo sistema a due passaggi uccideva le cellule quasi altrettanto efficacemente quanto il farmaco libero, ma solo quando il perossido di idrogeno era presente; senza di esso, le cellule rimanevano in gran parte indenni. Un pro-farmaco più semplice sensibile al perossido di idrogeno risultava meno efficace e meno selettivo in questi test, evidenziando il vantaggio di separare il riconoscimento dallo scatenamento in due fasi coordinate.
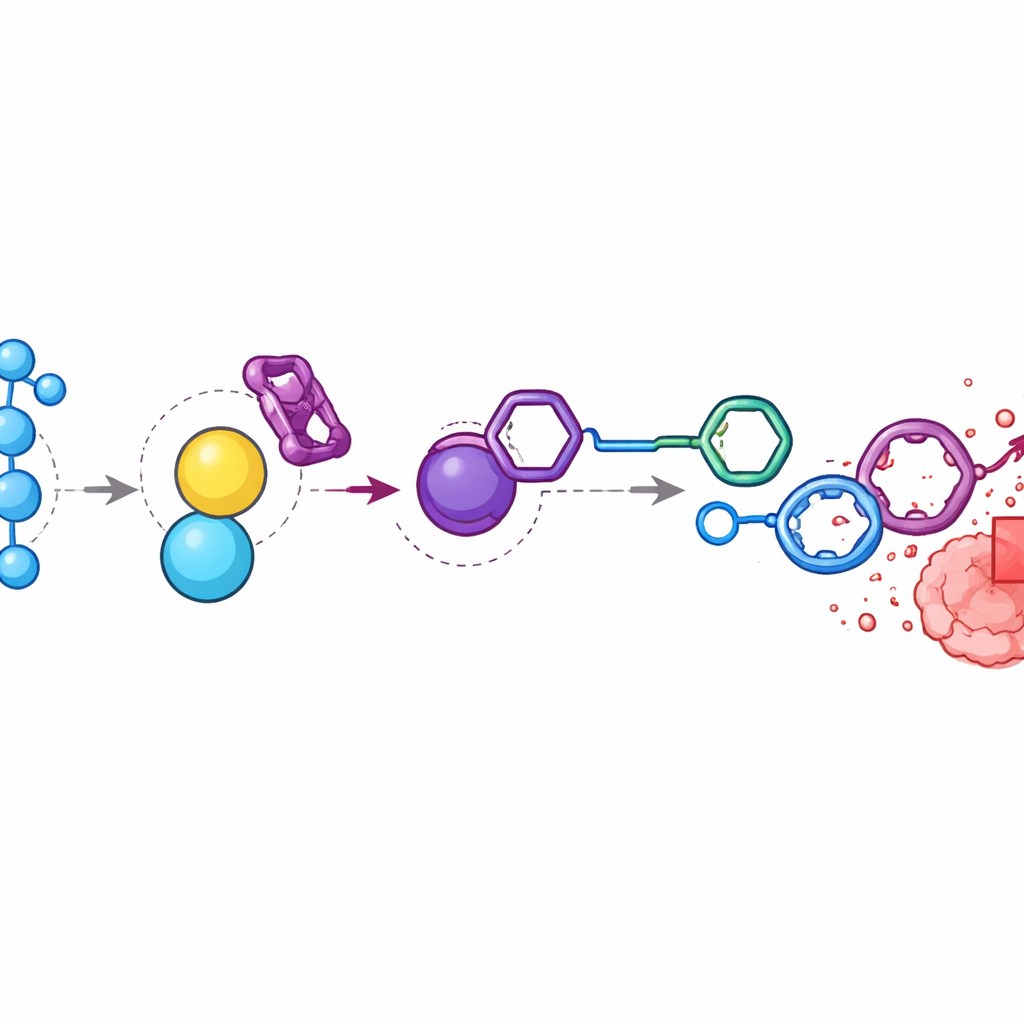
Concentrare la chemioterapia all’interno dei tumori
Nei topi portatori di tumori del colon, i ricercatori hanno rilevato che i livelli di perossido di idrogeno nei tumori erano quasi nove volte superiori rispetto al muscolo circostante. Hanno iniettato il pro-farmaco di doxorubicina e BTz in sequenza temporizzata in modo che entrambi si accumulassero vicino al tumore. L’analisi chimica ha mostrato che i componenti scomparivano in gran parte dal flusso sanguigno e dagli organi ma generavano alti livelli di doxorubicina libera all’interno dei tumori. Rispetto ad animali trattati con doxorubicina standard, quelli trattati con il sistema attivato hanno mostrato riduzioni tumorali simili o migliori ma hanno mantenuto peso corporeo stabile ed evitato la tossicità severa osservata a dosi farmacologiche più elevate. Quando il team ha interrotto il segnale del perossido di idrogeno iniettando catalasi, un enzima che rimuove il perossido di idrogeno, il rilascio del farmaco e l’accumulo selettivo nel tumore sono stati fortemente ridotti, confermando che lo stress ossidativo nel sito tumorale è il fattore chiave.
Dal segnale di stress alla terapia di precisione
Nel complesso, questo studio dimostra una piattaforma chimica versatile che trasforma un tratto distintivo della malattia—l’eccesso di ossidanti reattivi—in una manopola di controllo precisa per reazioni potenti all’interno dei sistemi viventi. Mantenendo bloccata la maniglia reattiva della tetrazina finché non incontra il perossido di idrogeno, l’approccio consente ai ricercatori di costruire terapie complesse all’interno del corpo solo dove servono, sia per smantellare una proteina che promuove il cancro sia per liberare un farmaco tossico all’interno di un tumore. Poiché lo stress ossidativo gioca ruoli anche nell’invecchiamento, nell’infiammazione, nel diabete e nelle malattie neurodegenerative, reazioni sensibili a questo tipo di stress potrebbero infine essere adattate a molte condizioni in cui la precisione e la sicurezza sono fondamentali.
Citazione: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
Parole chiave: chimica bioortogonale, specie reattive dell’ossigeno, legatura della tetrazina, rilascio mirato di farmaci, PROTAC