Clear Sky Science · it
Analisi microfluidica elettrochimica alimentata da membrane omotipiche di vescicole extracellulari per una diagnosi precisa del cancro
Trasformare l’armatura del cancro in uno strumento diagnostico
Le membrane che avvolgono le cellule tumorali sono ricche di distintive “bandiere” molecolari. Questo studio mostra come gli scienziati possano staccare quell’armatura, distribuirla su minuschele piastre d’oro e poi usarla per pescare particelle indicative nel sangue. Il risultato è un test ematico altamente sensibile che può rivelare non solo la presenza del cancro al seno, ma anche il suo sottotipo — informazione cruciale per scegliere la terapia più adeguata.
Perché il sottotipo del cancro al seno conta
Il cancro al seno non è una singola malattia. I tumori si raggruppano in sottotipi come recettore degli estrogeni positivo (ER+), HER2-positivo e triplo negativo, ciascuno dei quali risponde in modo diverso a terapie ormonali, farmaci mirati o chemio. Oggi i medici di solito determinano il sottotipo da una biopsia tissutale prelevata direttamente dal tumore. Quella procedura è invasiva, non può essere ripetuta frequentemente e può non cogliere cambiamenti che avvengono con l’evoluzione della malattia. Un test su sangue in grado di tracciare nel tempo queste firme di sottotipo permetterebbe ai clinici di aggiustare la terapia prima e con maggiore precisione.
Piccoli messaggeri che fluttuano nel sangue
Le cellule tumorali rilasciano costantemente bolle nanoscaled chiamate vescicole extracellulari (EV) nel flusso sanguigno. Le EV trasportano proteine, lipidi e materiale genetico che somigliano molto a quelli delle cellule d’origine, rendendole candidate ideali per le “biopsie liquide”. Ma c’è una sfida: le EV provenienti da diversi sottotipi di cancro al seno possono apparire molto simili se si guarda solo a una o due proteine. I test esistenti o prendono di mira marcatori condivisi — rendendo difficile distinguere i sottotipi — oppure si basano su saggi genetici complessi che sono lenti e possono dare risultati fuorvianti. Gli autori si sono posti l’obiettivo di leggere l’impronta molecolare più completa sulla superficie delle EV in modo semplice e robusto.
Costruire una rete biomimetica per pescare
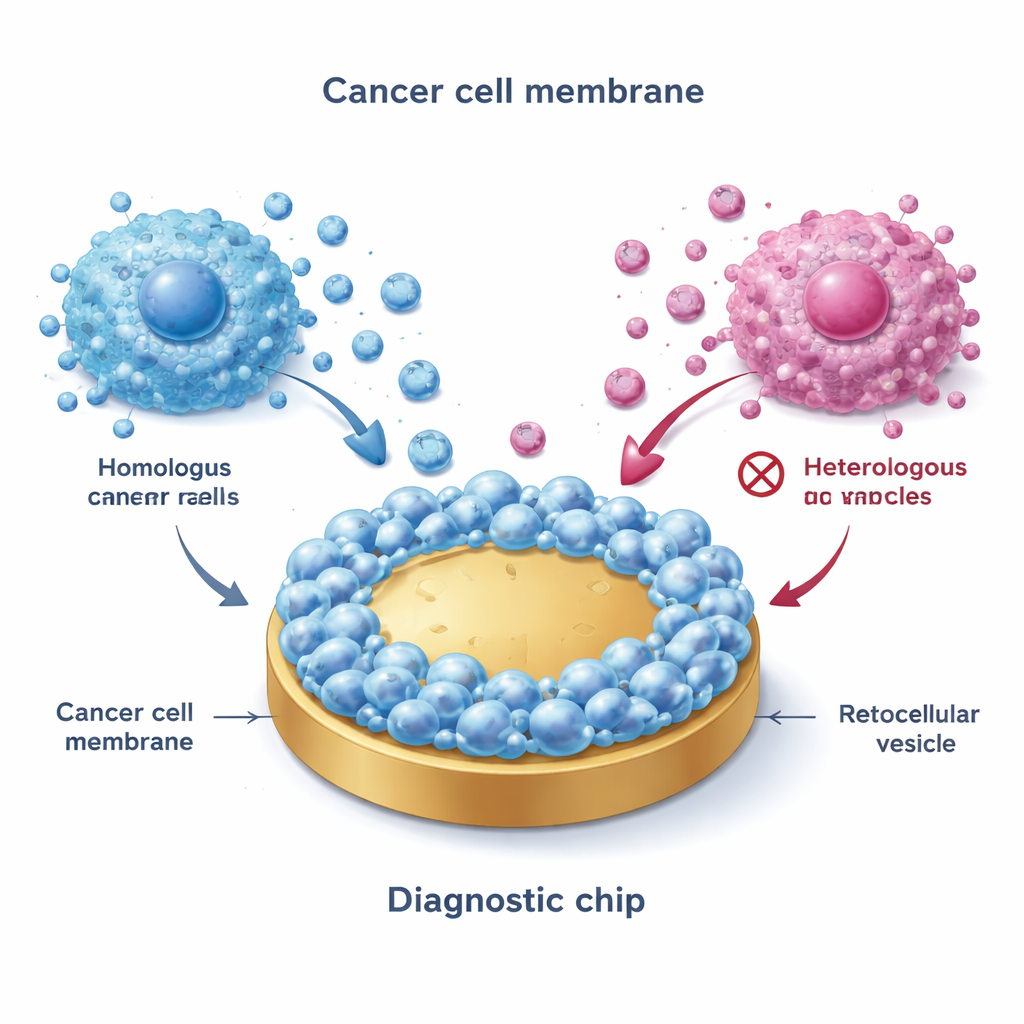
Il gruppo ha iniziato raccogliendo membrane da cellule del carcinoma mammario coltivate rappresentative dei principali sottotipi: ER+ (come MCF-7), HER2-positivo e triplo negativo. Usando un processo di congelamento-scongelamento hanno rotto le cellule, isolato le membrane esterne e quindi fuso queste membrane su superfici piane d’oro. Questo ha creato un “interfaccia biomimetica” che imita da vicino l’esterno delle cellule tumorali originali. Nota inaspettata: quando le EV venivano fatte scorrere su queste superfici rivestite, solo le vescicole dei sottotipi corrispondenti, o strettamente affini, aderivano in modo marcato — un fenomeno chiamato legame omotipico. Tecniche di imaging avanzate e misure elettriche hanno confermato che le superfici rivestite di membrana erano più ruvide, più idrofile e molto meno soggette ad adesioni non specifiche rispetto all’oro nudo, rendendole particolarmente adatte a misurazioni pulite in fluidi complessi come il sangue.
Convertire la cattura delle vescicole in un segnale elettrico
Per trasformare il legame in un segnale leggibile, i ricercatori hanno preso di mira una proteina abbondante sulla superficie delle EV chiamata CD47. Hanno attaccato anticorpi anti-CD47 a nanoparticelle d’argento usando un ponte di DNA corto, creando minuscoli marcatori elettroattivi. Dopo che la superficie rivestita di membrana aveva catturato le EV preferite, questi marcatori si agganciavano al CD47 sulle vescicole legate. Esponendo il sistema a una soluzione acida e poi misurandolo elettrochimicamente, l’argento generava una corrente netta e facilmente quantificabile. L’intensità di questo segnale aumentava in modo lineare su un ampio intervallo di concentrazioni di EV, fino a poche centinaia di vescicole per millilitro — molto più sensibile rispetto a metodi comuni come kit ELISA o tracciamento di nanoparticelle. Ogni tipo di membrana tumorale generava un forte segnale solo con le EV corrispondenti, anche in presenza di vescicole di altri sottotipi, piastrine o cellule non correlate.
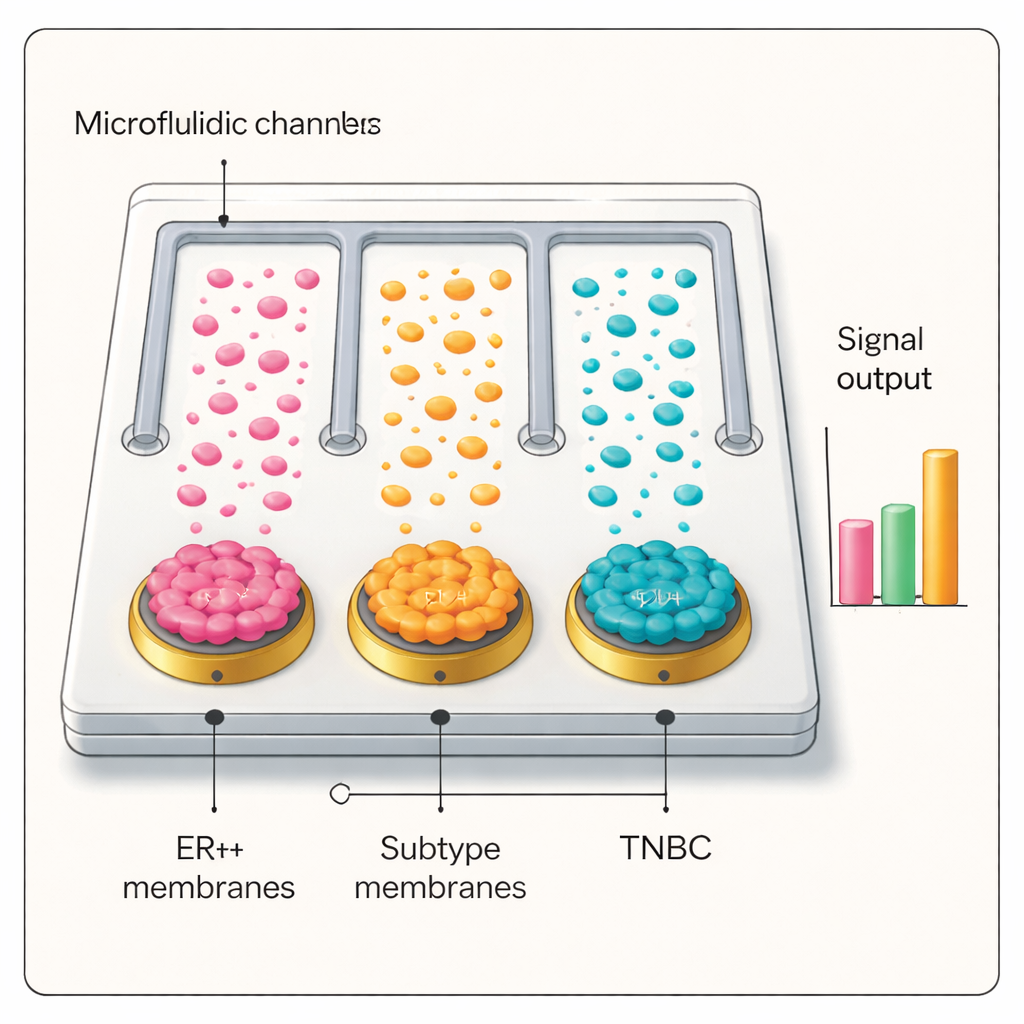
Dalla panca di laboratorio ai campioni ematici dei pazienti
Dotati di questa interfaccia selettiva e sensibile, il gruppo ha costruito una microchip microfluidico contenente canali paralleli, ciascuno rivestito con una diversa membrana di cellule del cancro al seno, più un controllo non rivestito. Quando il plasma dei pazienti veniva fatto scorrere nel chip e sondato con i marcatori argento-anticorpo, solo il canale la cui membrana corrispondeva al sottotipo tumorale del paziente produceva un segnale elettrico elevato. In test in cieco su dozzine di persone — tra cui pazienti con cancro al seno ER+ e triplo negativo, soggetti con malattia benigna della mammella, pazienti con cancro polmonare e volontari sani — la piattaforma ha distinto accuratamente cancro da non-cancro e ha identificato correttamente i sottotipi del cancro al seno. Le prestazioni diagnostiche hanno eguagliato o superato la patologia standard in molti casi e hanno mostrato potenziale per la stadiazione della malattia e il monitoraggio della sua progressione.
Cosa potrebbe significare per la cura del cancro in futuro
In termini semplici, i ricercatori hanno trasformato il guscio esterno del cancro in un’esca altamente selettiva per le particelle che i tumori rilasciano nel sangue. Leggendo la firma elettrica di quale canale «si illumina», un giorno i medici potrebbero determinare non solo se è presente un cancro, ma quale tipo è, usando solo un campione di sangue. Sebbene il sistema necessiti ancora di ulteriori perfezionamenti — come l’aggiunta di più marcatori e più tipi di membrane, e l’integrazione di analisi dati avanzate — indica un futuro in cui test ematici di routine, minimamente invasivi, guidano trattamenti oncologici personalizzati e monitorano come i tumori cambiano nel tempo.
Citazione: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
Parole chiave: sottotipi di cancro al seno, biopsia liquida, vescicole extracellulari, diagnostica microfluidica, sensori a membrana cellulare