Clear Sky Science · it
Assemblaggi molecolari che ciclicamente mirano al Golgi per imaging e perturbazione
Trasformare il centro logistico della cellula in un bersaglio strategico
All’interno di ogni cellula animale si trova l’apparato di Golgi, una vivace stazione di smistamento che completa, confeziona e invia migliaia di proteine e lipidi. Molte cellule tumorali dipendono fortemente da questo hub per modificare segnali di crescita e secernere fattori che modellano l’ambiente circostante. Questo studio presenta piccole molecole progettate che si dirigono specificamente al Golgi, lo rendono visibile per imaging rapido e, una volta riprogettate, possono bloccarne selettivamente le funzioni per compromettere le cellule tumorali risparmiando alcuni tipi di cellule sane.
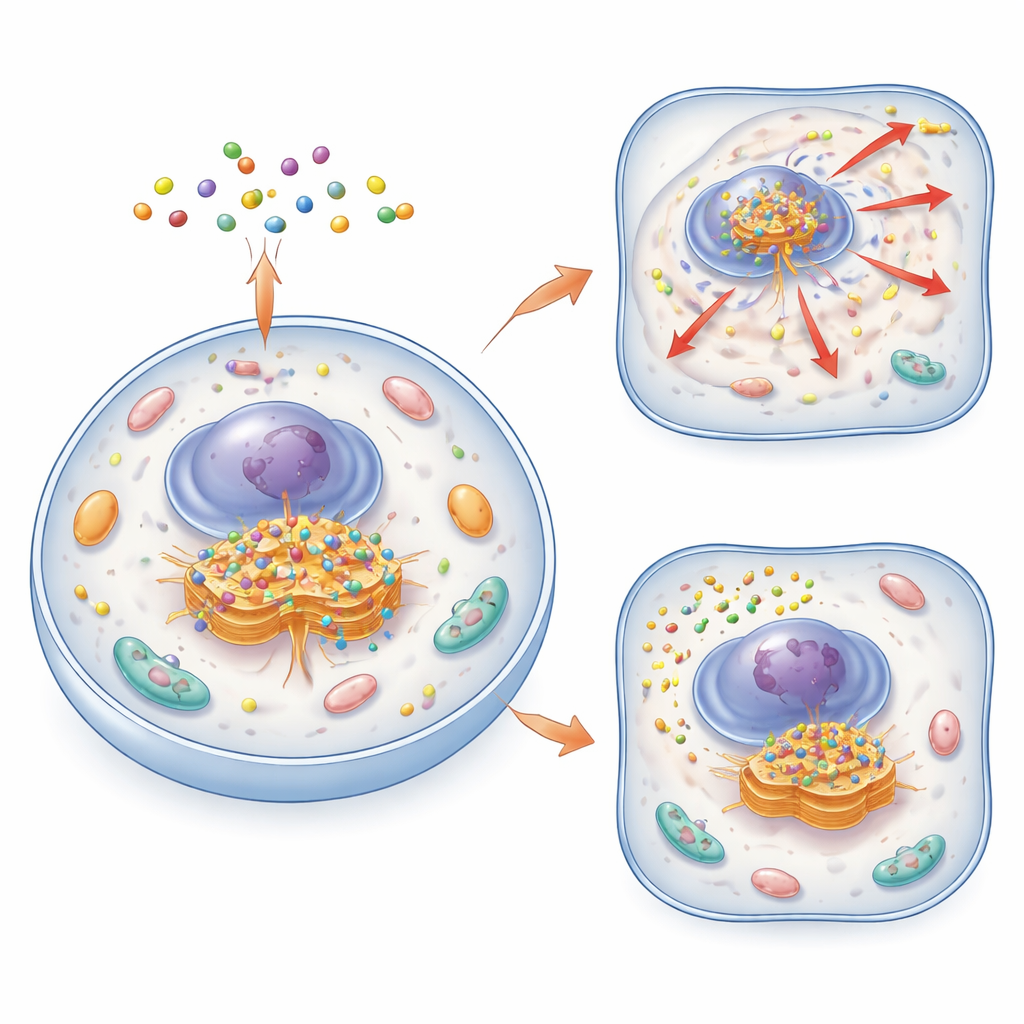
Un nuovo modo per trovare e osservare il Golgi
Gli autori hanno creato una famiglia di piccole molecole intelligenti chiamate assemblaggi molecolari ciclici, o CyMA. Queste molecole sono costruite su brevi peptidi in grado sia di attraversare le membrane cellulari sia di aggregarsi in piccole ammassi. Nella loro versione «per imaging» (CyMA‑i), i peptidi portano un colorante fluorescente che brilla intensamente quando le molecole si assemblano. Una volta all’interno della cellula, gli enzimi rimuovono un cappuccio protettivo dal precursore CyMA, esponendo un gruppo reattivo. Enzimi residenti nel Golgi quindi attaccano a questo gruppo una catena lipidica, rendendo le molecole molto più adesive e inclini ad auto‑assemblarsi proprio al Golgi. Poiché questo processo è rapido e sfrutta la macchina cellulare naturale, i ricercatori possono delineare la forma del Golgi in cellule vive in pochi minuti e a concentrazioni di sonda molto basse.
Un ciclo futile che ancora le molecole al Golgi
Le CyMA non sono semplici marcatori; sono progettate per partecipare a un «ciclo futile» nel Golgi. Un gruppo di enzimi attacca catene lipidiche al peptide, mentre un altro gruppo le rimuove. Man mano che la cellula aggiunge e toglie ripetutamente queste catene, i peptidi modificati continuano a assemblarsi e disassemblarsi sul posto. Questo continuo andirivieni intrappola un nucleo di tipo solido di assemblaggi sulle membrane del Golgi, pur mantenendo le singole molecole in ciclo. La cellula deve costantemente spendere i propri blocchi di costruzione a base di acidi grassi per mantenere questo circuito, nutrendo di fatto gli assemblaggi e contribuendo alla loro persistenza. Allo stesso tempo, altri enzimi possono lentamente tagliare uno specifico legame estere all’interno delle CyMA, trasformandole in frammenti più idrofili che si disperdono. Poiché alcune cellule sane, come gli epatociti e certi tipi di cellule immunitarie, sono ricche di tali esterase, sono in grado di smantellare più efficacemente le CyMA e quindi risultano meno colpite.
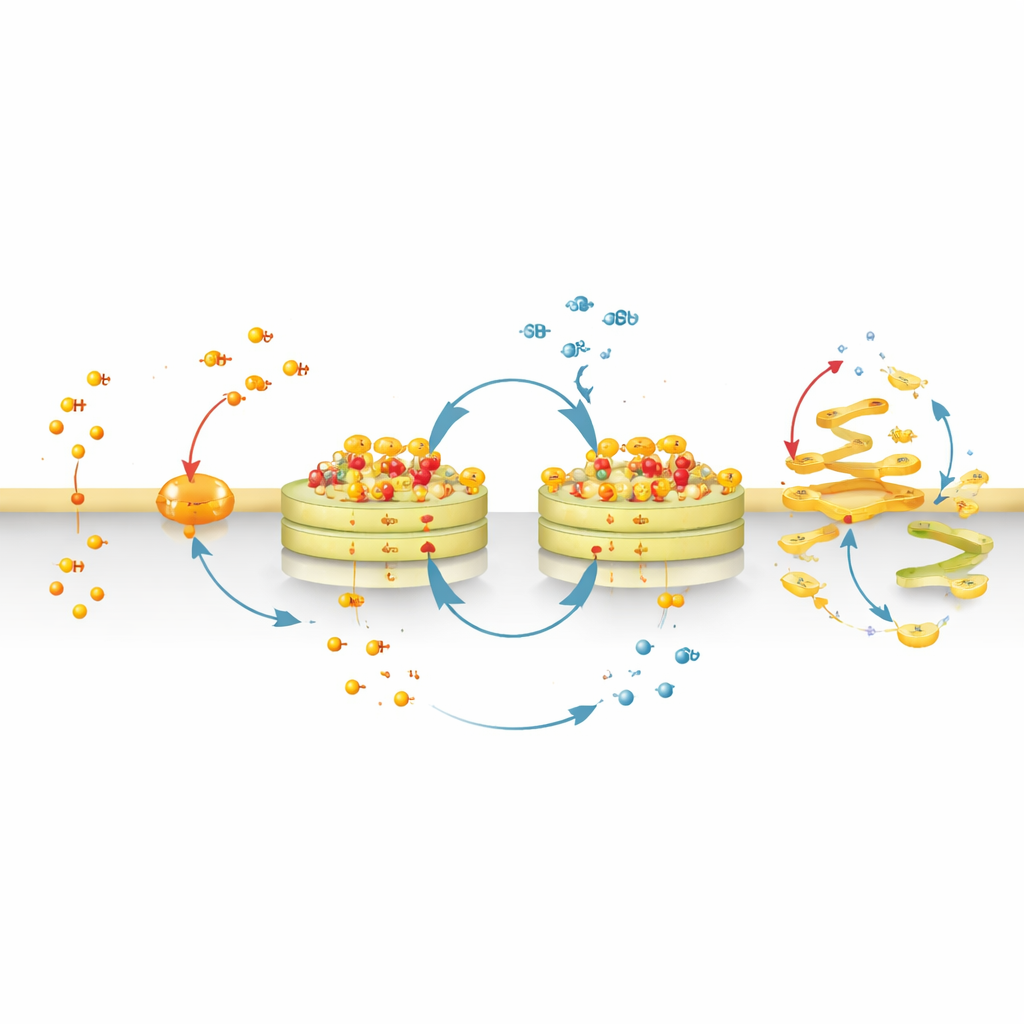
Da strumento delicato per imaging a perturbatore del Golgi
Sostituendo il colorante fluorescente con un gruppo chimico più fortemente attratto dalle membrane, il team ha convertito CyMA‑i in CyMA‑d, una versione distruttiva che non brilla più ma continua a ciclare e assemblarsi al Golgi. Questi assemblaggi disturbano fisicamente la struttura del Golgi e il continuo flusso di vescicole da e verso di esso. Le proteine che normalmente transitano dal reticolo endoplasmatico al Golgi e poi verso la superficie cellulare rimangono bloccate o vengono mal instradate. Anche le vie in ingresso — dalla membrana cellulare di ritorno al Golgi o dal Golgi verso altri organelli — risultano ostacolate. Di conseguenza, recettori chiave di superficie e molecole di segnalazione o non raggiungono le loro destinazioni o si accumulano nei punti sbagliati all’interno della cellula.
Confusione dei segnali cellulari e dei messaggi secreti
Il Golgi è dove molte proteine ricevono tocchi finali cruciali, come catene di zuccheri e code lipidiche. Gli assemblaggi CyMA‑d riducono la corretta lipidazione e glicosilazione di numerose proteine, compresi noti driver oncogenici come Ras e importanti tirosin chinasi recettoriali. Queste modifiche deviano vie di crescita promozionali quali AKT e mTOR. Allo stesso tempo, l’output secretorio della cellula viene attenuato: fattori importanti come TGF‑β1 e VEGF, che i tumori usano per sopprimere l’immunità e stimolare la formazione vascolare, non vengono più rilasciati in modo efficiente. Lo stress derivante da questo collasso provoca reti del reticolo endoplasmatico aggrovigliate, alterazioni mitocondriali, autofagia bloccata (il sistema di riciclaggio cellulare) e un aumento di proteine danneggiate taggate con ubiquitina, spingendo insieme le cellule tumorali verso la morte.
Pressione selettiva sui tumori e potenziale terapeutico
Poiché CyMA‑d dipendono da un insieme condiviso di enzimi e metaboliti che molte cellule tumorali sovrautilizzano, possono uccidere un’ampia gamma di tipi tumorali, compresi modelli di cancro ovarico resistenti ai farmaci, a dosi molto basse. Le cellule con livelli elevati di specifiche esterase, tuttavia, smontano più facilmente le CyMA‑d e sono meno danneggiate, offrendo una via intrinseca alla selettività. In sfere tumorali tridimensionali, colture derivate da pazienti e modelli murini, le CyMA‑d riducono le masse tumorali, contrastano le metastasi e diminuiscono l’accumulo di liquidi nell’addome. In combinazione con terapie che inibiscono i checkpoint immunitari, migliorano ulteriormente il controllo del tumore e la sopravvivenza. In sostanza, questo lavoro dimostra che costruire materiali dinamici all’interno del Golgi — piuttosto che mirare a una singola proteina — può arrestare contemporaneamente diversi processi critici per il cancro.
Cosa significa per i trattamenti futuri
Per un non specialista, l’idea chiave è che gli autori hanno trasformato il Golgi da semplice spettatore a bersaglio terapeutico attivo. Reclutando gli enzimi della cellula per assemblare e riciclare piccole molecole in questo hub centrale, si può sia evidenziarlo senza danno sia sopraffarne gradualmente la funzione. Questa piattaforma a doppio uso suggerisce un nuovo tipo di trattamento: invece di progettare un farmaco per una singola proteina, potremmo ingegnerizzare piccoli precursori che le cellule trasformano in materiali auto‑organizzati, capaci di perturbare intere reti di comunicazione e trasporto su cui i tumori fanno affidamento per crescere e diffondersi.
Citazione: Tan, W., Zhang, Q., Liu, Z. et al. Cycling molecular assemblies for Golgi imaging and disruption. Nat Commun 17, 2102 (2026). https://doi.org/10.1038/s41467-026-68768-8
Parole chiave: Apparato di Golgi, assemblaggi molecolari, traffico proteico, terapia oncologica, targeting degli organelli