Clear Sky Science · it
Il silenziamento del catabolismo lipidico determina la longevità in risposta al digiuno
Perché spegnere la combustione dei grassi può essere una buona cosa
Molti credono che il digiuno faccia bene perché costringe l’organismo a bruciare i grassi come carburante. Questo studio, condotto nel piccolo verme Caenorhabditis elegans, ribalta quell’idea. I ricercatori mostrano che la chiave per vivere più a lungo dopo un digiuno non è quanto intensamente le cellule attivino la combustione dei grassi, ma quanto precisamente la spengano una volta che il cibo ritorna. Capire questo interruttore on–off in un animale semplice potrebbe infine influenzare il modo in cui progettiamo strategie di digiuno e dieta negli esseri umani.
Un animale semplice con metabolismo flessibile
Gli autori usano C. elegans, un verme microscopico il cui metabolismo e le cui vie di invecchiamento condividono molte caratteristiche con i nostri. Hanno sottoposto giovani adulti a 24 ore di digiuno seguite da un ritorno al cibo. Durante il digiuno, i vermi hanno rapidamente consumato le loro principali riserve di grasso—trigliceridi immagazzinati in goccioline intestinali—pur preservando il colesterolo essenziale. Quando il cibo è stato ripristinato, le goccioline lipidiche e i profili di acidi grassi liberi sono tornati ai livelli pre-digiuno, e i vermi hanno mantenuto normali livelli di energia (ATP) nei muscoli. Nonostante questa stabilità energetica, un singolo ciclo di digiuno e riforaggiamento ha esteso la vita mediana di circa il 40% e ha mantenuto gli animali più vigorosi nelle età avanzate.
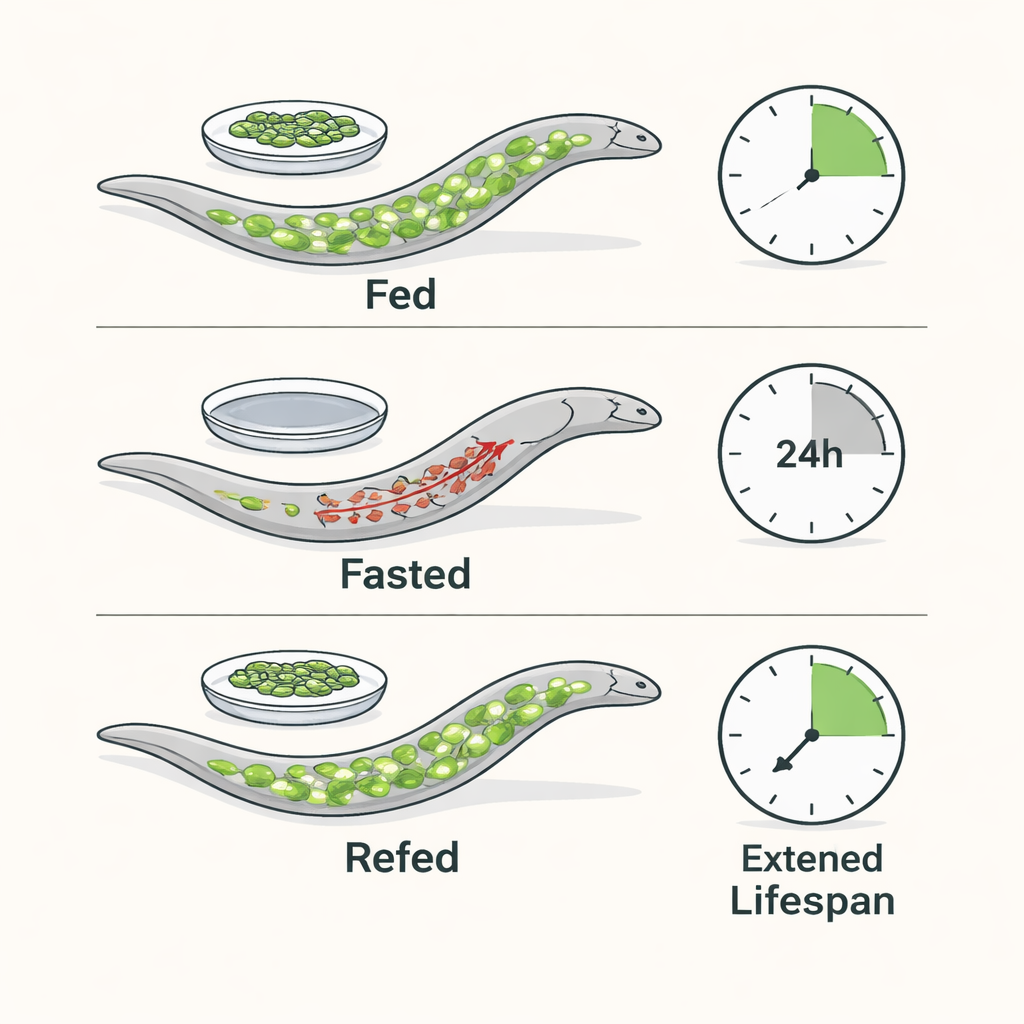
La combustione dei grassi non è necessaria per il beneficio di longevità del digiuno
Poiché il digiuno normalmente spinge le cellule a degradare i grassi, il team si è chiesto se questa combustione lipidica sia effettivamente necessaria per vivere più a lungo. Si sono concentrati su NHR-49, un recettore nucleare degli ormoni che attiva geni per la β-ossidazione mitocondriale, la principale via di combustione dei grassi. I vermi privi di NHR-49 non sono riusciti ad aumentare correttamente l’espressione di questi geni durante il digiuno e hanno mostrato cali maggiori di ATP. Eppure, sorprendentemente, hanno comunque ottenuto un forte allungamento della durata della vita dal digiuno, simile a quello dei vermi normali. Lo stesso è avvenuto quando i ricercatori hanno bloccato passaggi a monte nella degradazione dei grassi con strumenti genetici. Nel complesso, questi esperimenti mostrano che una robusta attivazione del catabolismo lipidico durante il digiuno è in gran parte superflua per il beneficio di longevità.
Un interruttore temporale che spegne la combustione dei grassi
Se attivare la combustione dei grassi non è essenziale, potrebbe esserlo spegnerla. Lo studio rivela che NHR-49 è controllato da un meccanismo indipendente dal ligando—invece di essere regolato da una piccola molecola ormonale classica, la sua attività è modulata da marchi chimici aggiunti alla proteina stessa. Durante il recupero dal digiuno, NHR-49 riceve un pattern specifico di gruppi fosfato su residui di serina vicini in una regione flessibile a “cerniera”. Questi marchi carichi negativamente indeboliscono l’ancoraggio di NHR-49 al DNA e ne favoriscono la rimozione dai geni della combustione dei grassi, silenziandoli efficacemente quando il cibo ritorna. Senza questo spegnimento temporizzato, le cellule rischiano di rimanere bloccate in una modalità di elevata combustione lipidica che può esaurire le riserve e alterare l’equilibrio a lungo termine.
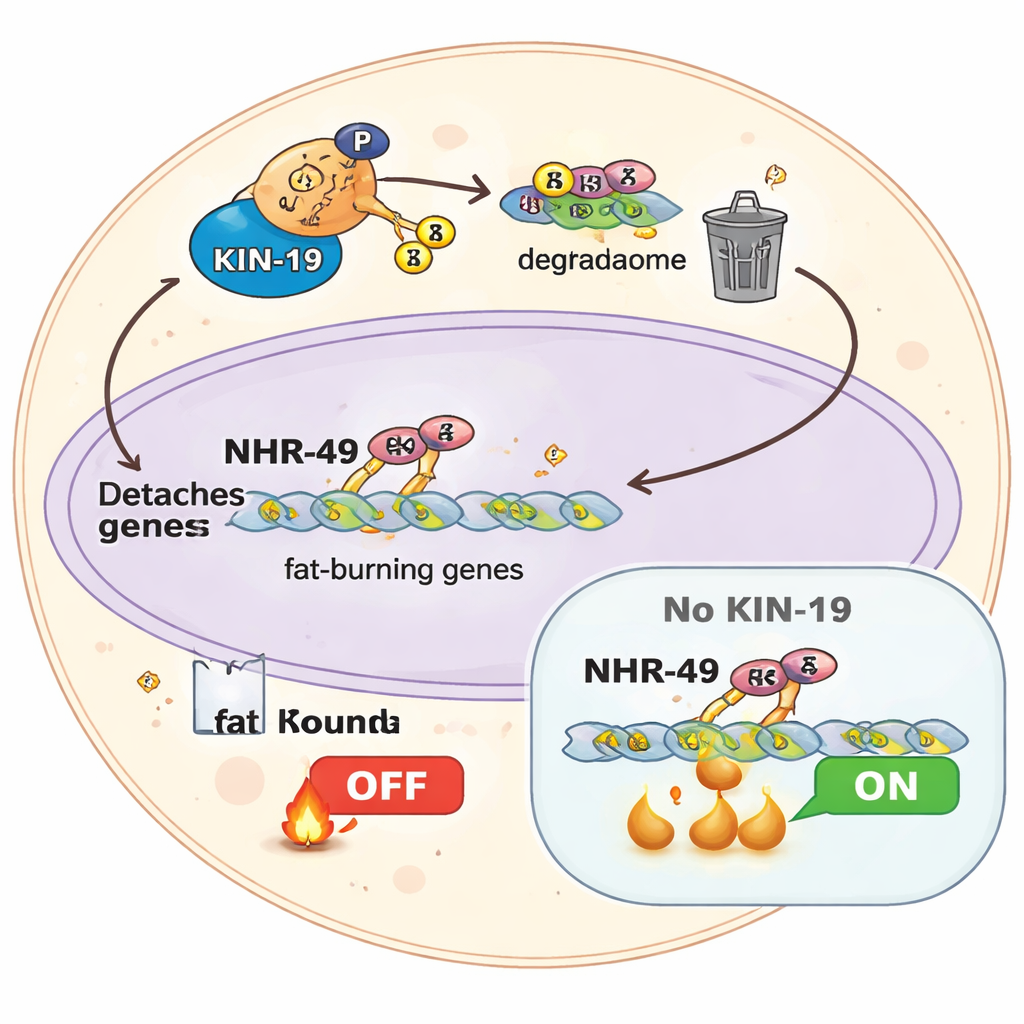
KIN-19: l’enzima che termina il digiuno
Gli autori identificano una chinasi caseinica, KIN-19, come attore centrale in questo sistema di spegnimento. Saggi biochimici mostrano che una volta che NHR-49 è “primato” da una fosforilazione iniziale, KIN-19 aggiunge efficacemente ulteriori gruppi fosfato nelle vicinanze. I vermi in cui KIN-19 è ridotto si comportano come se fossero permanentemente in digiuno: sono più piccoli, hanno basse riserve di grasso, forma mitocondriale alterata e consumo di ossigeno ridotto, anche quando il cibo è abbondante. I loro profili di espressione genica somigliano a uno stato di digiuno cronico e i loro livelli energetici non si riprendono correttamente dopo il rifacimento. Crucialmente, quando KIN-19 è compromessa, un digiuno di 24 ore non estende più la durata della vita; il guadagno di longevità si riduce a un effetto minimo. Questo indica che spegnere la combustione dei grassi guidata da NHR-49 tramite KIN-19 è essenziale perché il digiuno promuova un invecchiamento sano.
Cosa significa per il digiuno e l’invecchiamento sano
Per un lettore non specialista, il messaggio centrale è che la capacità del corpo di cambiare marcia può contare più di quanto spinga una singola marcia. Nei vermi, il digiuno è benefico non perché brucino quanti più grassi possibile, ma perché sanno passare senza intoppi a una modalità di immagazzinamento e riparazione quando il cibo ritorna. L’enzima KIN-19 aiuta a terminare la fase di combustione dei grassi marcando e rimuovendo NHR-49, prevenendo uno stato di “emergenza” dannoso e perenne. Sebbene gli esseri umani siano molto più complessi, questo lavoro suggerisce che strategie di digiuno efficaci potrebbero dipendere da periodi ben temporizzati di attivazione e riposo del metabolismo, piuttosto che da una perdita di grasso continua e aggressiva.
Citazione: Tatge, L., Kim, J., Solano Fonseca, R. et al. Silencing lipid catabolism determines longevity in response to fasting. Nat Commun 17, 1919 (2026). https://doi.org/10.1038/s41467-026-68764-y
Parole chiave: digiuno e longevità, metabolismo lipidico, recettori nucleari degli ormoni, flessibilità metabolica, invecchiamento di C. elegans