Clear Sky Science · it
Un chimera antigenico tandem stabilizzato che induce una potente attività di riduzione della trasmissione della malaria
Perché fermare la trasmissione da zanzare è importante
I vaccini contro la malaria attualmente in uso possono ridurre notevolmente le forme gravi e la mortalità nei bambini piccoli, ma lasciano una falla importante: le persone che non si sentono malate possono comunque ospitare parassiti che infettano le zanzare e mantengono la trasmissione. Questo studio presenta un progetto vaccinale di nuova generazione pensato non per proteggere solo un individuo, ma per interrompere la catena di infezione tra esseri umani e zanzare. Attraverso l’ingegnerizzazione precisa di come le proteine chiave del parassita vengono presentate al sistema immunitario, i ricercatori mirano a generare anticorpi che rendano le zanzare ospiti poco adatti per la malaria, aiutando le comunità ad avvicinarsi all’eliminazione.
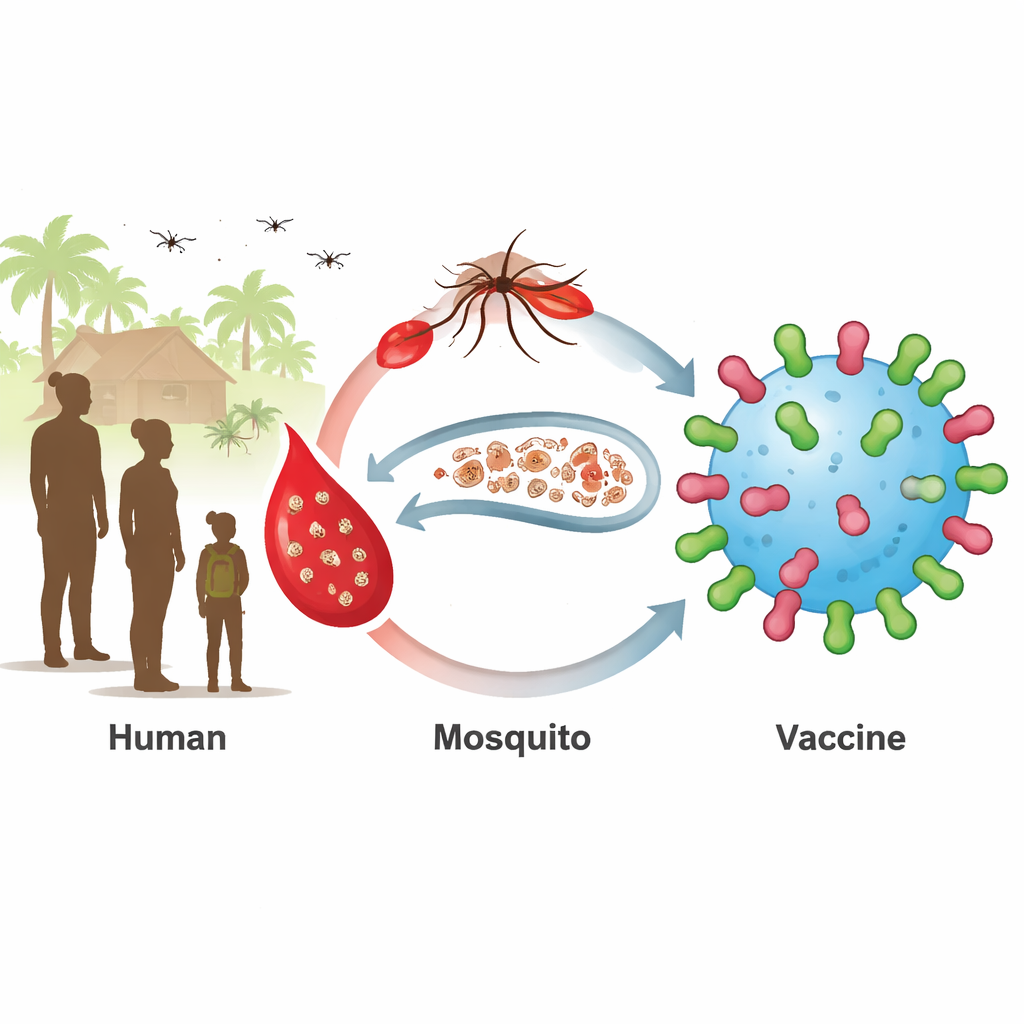
Un serbatoio nascosto che mantiene viva la malaria
I vaccini attuali contro la malaria si concentrano sulle fasi iniziali dell’infezione nel fegato e nel sangue. Funzionano meglio nei bambini piccoli, ma bambini più grandi e adulti spesso ospitano parassiti allo stadio sessuale maturo, detti gametociti, senza sintomi. Quando le zanzare pungono queste persone, acquisiscono i parassiti e li diffondono ulteriormente. Due proteine di superficie del parassita, note come Pfs230 e Pfs48/45, si trovano su questi stadi sessuali e sono bersagli interessanti per i cosiddetti vaccini che bloccano la trasmissione. Vaccini basati su frammenti di queste proteine sono entrati in studi clinici, ma hanno faticato a produrre risposte anticorpali forti e durature in tutti i riceventi.
Costruire un’esca più intelligente per il sistema immunitario
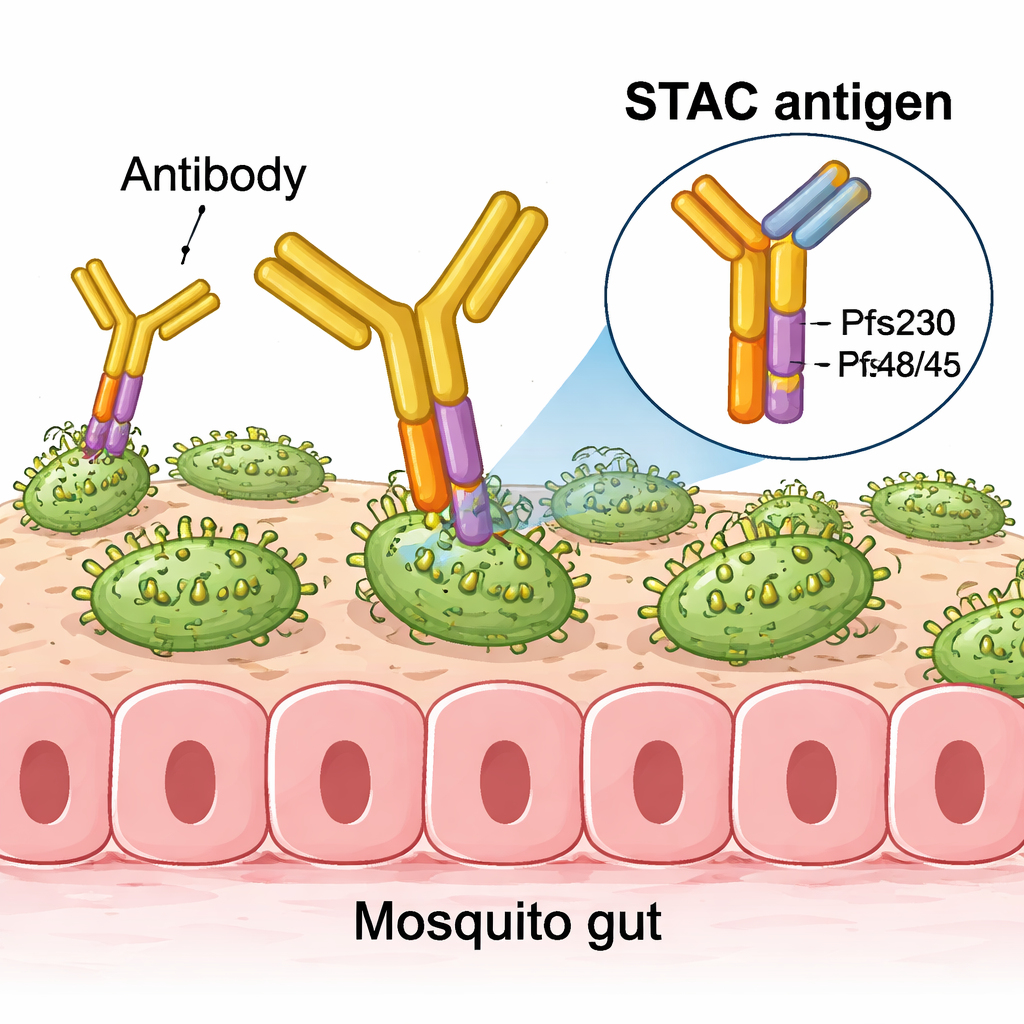
Per migliorare i progetti precedenti, gli autori hanno adottato un approccio di biologia strutturale, analizzando a livello atomico come anticorpi umani potenti si legano a Pfs230 e Pfs48/45. Hanno identificato piccole regioni, o epitopi, particolarmente efficaci nel bloccare lo sviluppo del parassita all’interno delle zanzare. Ugualmente importante, hanno mappato epitopi “non funzionali” che attraggono anticorpi che si legano ma non impediscono la trasmissione—sostanzialmente sprechi di risorse immunitarie. Usando modellizzazione al computer e strumenti di ingegneria proteica, hanno fuso la regione più potente di Pfs230 (il suo primo dominio) con la regione chiave di Pfs48/45 (il suo terzo dominio) in un’unica proteina disposta con cura che chiamano chimera antigenica tandem stabilizzata, o STAC.
Nascosto i bersagli inutili, mantenuti quelli utili
La sfida era presentare questi due domini insieme in modo che imitassero la loro disposizione sul parassita, nascondendo fisicamente le superfici non funzionali che normalmente sono sepolte nella proteina intatta. Il team ha ridisegnato in modo iterativo il breve linker e l’interfaccia tra i due domini, testando ogni versione per stabilità, corretto ripiegamento e per verificare il legame con un pannello di anticorpi ben caratterizzati. Software avanzati di progettazione hanno suggerito mutazioni che hanno consolidato l’interfaccia e migliorato l’espressione nelle cellule in coltura. Studi strutturali mediante cristallografia a raggi X, scattering a basso angolo di raggi X e crio‑microscopia elettronica hanno confermato che nella costruzione finale STAC, gli epitopi desiderati sono esposti con elevata fedeltà, mentre i siti noti non utili sono bloccati stericamente.
Dalle singole molecole a nanoparticelle potenti
I test nei topi hanno mostrato che quando STAC veniva attaccata a liposomi specializzati o a nanoparticelle proteiche auto‑assemblanti, induceva risposte anticorpali forti capaci di ridurre nettamente lo sviluppo del parassita in saggi standard di alimentazione delle zanzare. A dosi uguali o inferiori, STAC spesso ha eguagliato o superato vaccini basati su frammenti di Pfs230 e Pfs48/45 somministrati separatamente, sia somministrati da soli, miscelati insieme, o co‑esposti sulla stessa particella. In test altamente sensibili che diluivano il siero dei topi molte volte, gli anticorpi indotti da nanoparticelle decorate con STAC mantenevano meglio l’attività di riduzione della trasmissione rispetto a quelli provenienti da altre formulazioni, indicando risposte particolarmente potenti e mirate.
Cosa potrebbe significare per il controllo della malaria
Per i non specialisti, l’idea chiave è che STAC è un’esca costruita su misura che mostra al sistema immunitario esattamente le parti del parassita della malaria che contano di più per bloccarne la diffusione, nascondendo al contempo le regioni di distrazione che non aiutano. Nei modelli animali, questo progetto genera anticorpi che rendono difficile per i parassiti completare il loro ciclo vitale nelle zanzare, anche quando i livelli anticorpali sono relativamente bassi. Se risultati simili si confermassero nell’uomo, STAC potrebbe diventare un partner potente per i vaccini antimalarici esistenti: proteggendo gli individui vaccinati dalla malattia e riducendo il serbatoio infettivo nella comunità. Più in generale, il lavoro mostra come approfondite conoscenze strutturali e l’ingegneria delle proteine possano essere usate per creare vaccini multi‑componente potenti, stabili e potenzialmente più economici da produrre.
Citazione: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
Parole chiave: vaccini contro la malaria, blocco della trasmissione, Pfs230, Pfs48/45, immunogeno nanoparticellare