Clear Sky Science · it
Ruolo essenziale dell’asse NONO-HOXA1-Wnt nella differenziazione dei cardiomiociti
Perché le piccole cellule cardiache contano per tutti noi
Ogni battito cardiaco dipende da miliardi di cellule muscolari specializzate che si formano nell’utero. Quando questo processo fallisce, i neonati possono nascere con gravi difetti cardiaci. Questo studio utilizza cellule staminali umane per svelare un sistema di controllo cruciale — composto dalle molecole chiamate NONO e HOXA1 e da un noto segnale, Wnt — che aiuta le cellule precoci a impegnarsi a diventare muscolo cardiaco sano. Comprendere questo circuito nascosto potrebbe alla lunga guidare diagnosi e terapie migliori per le cardiopatie congenite.
Da cellule a una lavagna bianca ai primi costruttori del cuore
I ricercatori hanno iniziato con cellule staminali pluripotenti indotte umane — cellule versatili che possono essere indotte a diventare quasi qualsiasi tipo cellulare. Usando una procedura standard, hanno diretto queste cellule verso la differenziazione in cardiomiociti, le cellule battenti del cuore. Quando il gene NONO è stato rimosso, molte meno cellule hanno adottato con successo un’identità cardiaca. I marcatori precoci chiave che normalmente compaiono quando le cellule lasciano il loro stato primitivo e si dirigono verso la linea cardiaca sono risultati fortemente ridotti. L’analisi con RNA-seq a singola cellula ha mostrato che molte cellule carenti di NONO si sono bloccate a metà strada, intrappolate in uno stato immaturo simile a mesendoderma invece di progredire verso il muscolo cardiaco maturo.
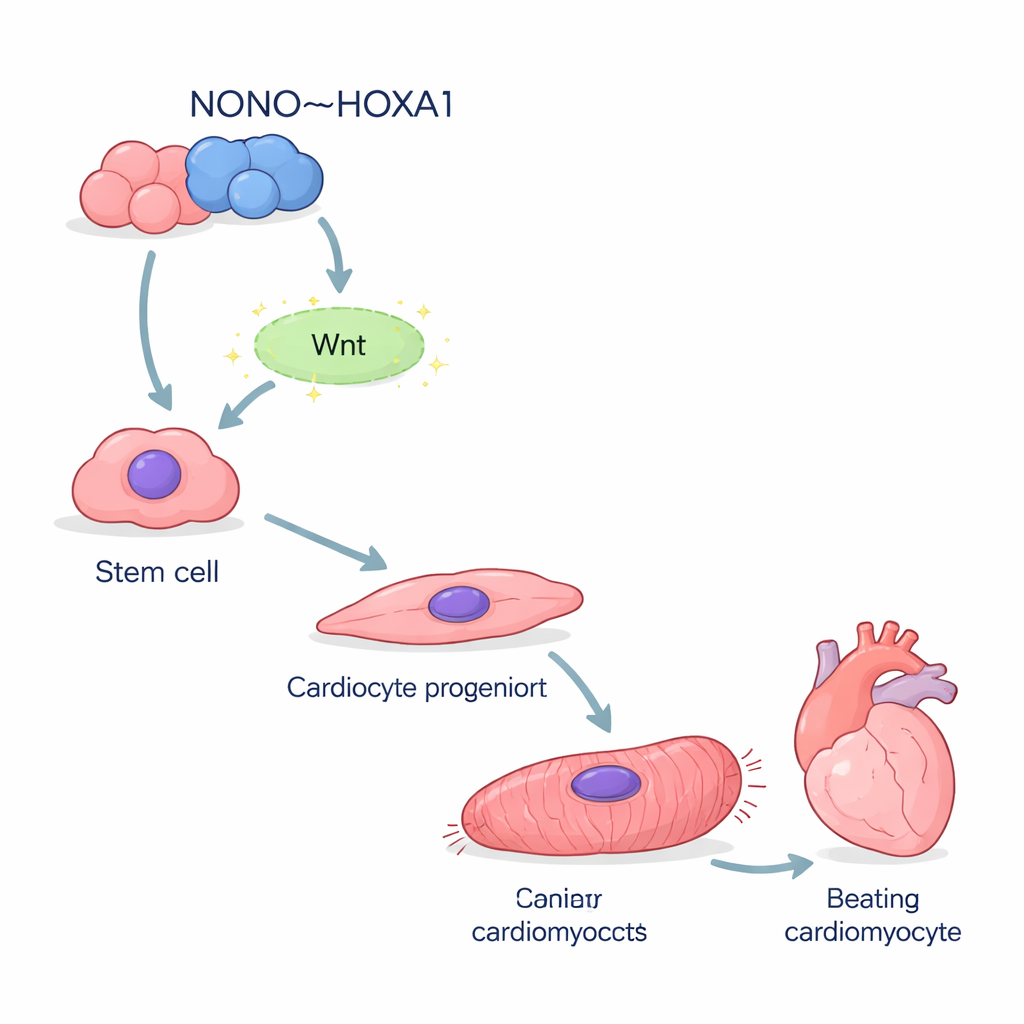
Quando viene a mancare l’impalcatura, le cellule cardiache vacillano
Le poche cellule che sono diventate cardiomiociti in assenza di NONO erano lungi dall’essere sane. Hanno espresso livelli molto più bassi di proteine strutturali che formano il sarcomero, la macchina microscopica che alimenta la contrazione. Al microscopio, la maggior parte delle cellule mutate mostrava fibre contrattili disorganizzate e frammentate anziché le striature ordinate osservate nelle cellule normali. La microscopia elettronica ha confermato che le abituali “pioli” del disco Z della scala contrattile erano mancanti o malformati. Funzionalmente, queste cellule battevano più lentamente e in modo irregolare. Le misurazioni delle ondate di calcio — eventi elettrici che innescano ogni battito — hanno rivelato forme d’onda irregolari con picchi ritardati e recupero lento, in accordo con i difetti nell’espressione genica dei canali che regolano il calcio.
Salvare lo sviluppo ed esporre la collaborazione NONO–HOXA1
Per verificare se questi problemi derivavano realmente dalla perdita di NONO, il team ha reintrodotto NONO in modo controllato e inducibile con farmaci durante i primi due giorni di differenziazione. Questo breve impulso di NONO ha in gran parte ripristinato l’aumento dei geni cardiaci precoci, ha aumentato la percentuale di cellule battenti e ha ricostruito sarcomeri e dischi Z organizzati. Il profilo di espressione genica ha confermato che molti geni legati alla contrazione muscolare e allo sviluppo cardiaco sono tornati verso livelli normali. Al contrario, versioni mutate di NONO derivate da pazienti non sono riuscite a salvare il fenotipo, a sostegno dell’idea che tali varianti causino malattia interrompendo questo programma precoce. Esperimenti di interazione proteica hanno poi rivelato che NONO si lega fisicamente a un fattore di trascrizione chiamato HOXA1, e che questo contatto stabilizza HOXA1 e ne favorisce la formazione di dimeri necessari per legare il DNA.
Accendere il segnale Wnt per impegnarsi verso destino cardiaco
La mappatura dei siti genomici occupati da queste proteine ha mostrato che NONO e HOXA1 frequentano spesso le stesse regioni regolatorie, incluse quelle che controllano importanti geni cardiaci precoci e geni della via Wnt. In assenza di NONO, l’ancoraggio di HOXA1 su molti di questi siti si è indebolito, specialmente sui geni che guidano il mesoderma precardiaco — il tessuto più precoce che forma il cuore. Anche la via a valle Wnt/β‑catenina, che normalmente favorisce l’avvio del mesoderma e dello sviluppo cardiaco, è risultata attenuata: meno β‑catenina si accumulava nel nucleo e i test con reporter sensibili a Wnt sono diminuiti. Rinforzare i segnali Wnt con una dose più alta di un farmaco attivatore di Wnt durante i primi giorni di differenziazione è stato in grado di compensare parzialmente l’assenza di NONO, ripristinando un numero maggiore di cellule cardiache e aumentando l’espressione dei geni cardiaci.
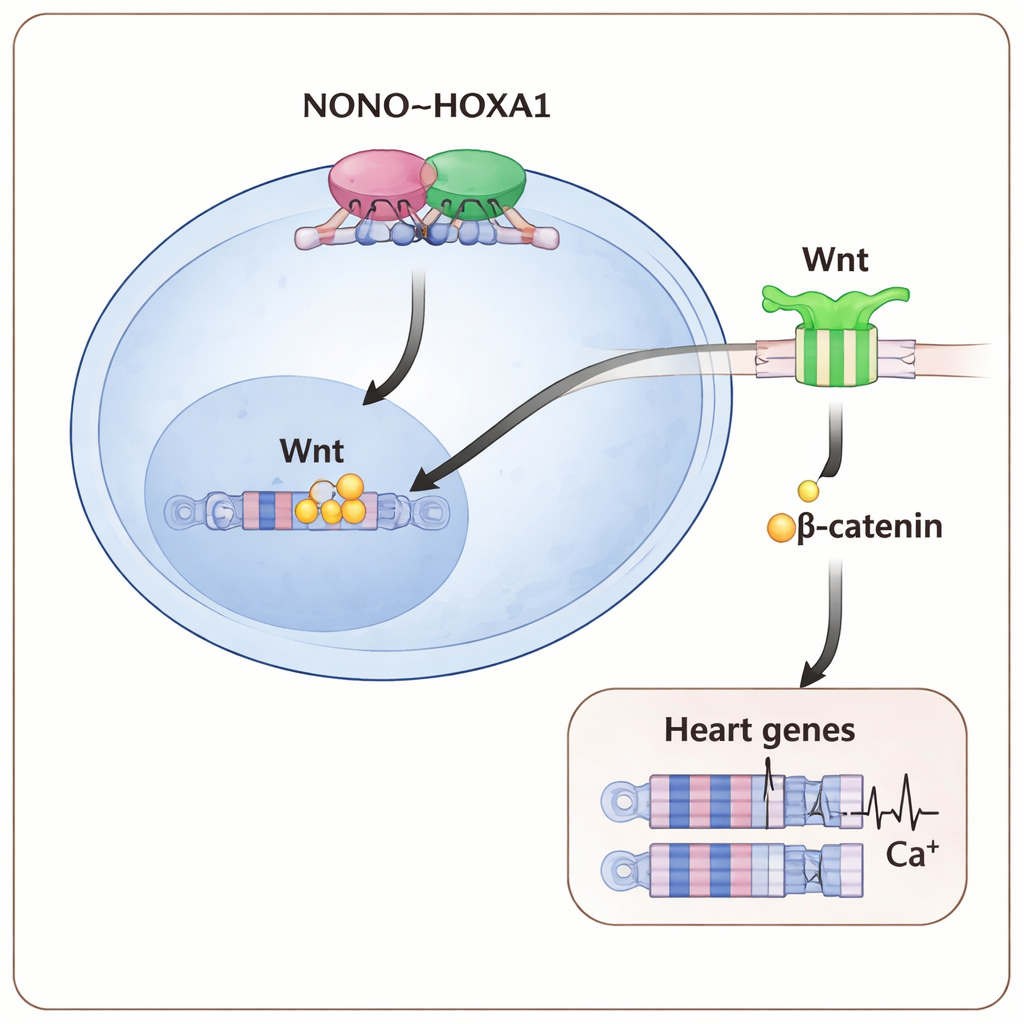
Cosa significa questo per comprendere i difetti alla nascita
Per i non specialisti, il messaggio centrale è che una piccola squadra molecolare — NONO che lavora fianco a fianco con HOXA1 per modulare finemente i segnali Wnt — agisce come un primo “controllore del traffico” che dice alle giovani cellule di diventare muscolo cardiaco e le prepara a battere correttamente. Quando una qualsiasi parte di questo asse NONO–HOXA1–Wnt è disturbata, le cellule esitano, i geni cardiaci chiave restano spenti e i cardiomiociti risultanti sono strutturalmente ed elettricamente fragili. Queste intuizioni offrono una spiegazione molecolare più chiara del perché mutazioni in NONO sono associate a cardiopatie congenite e indicano possibili modalità per manipolare questa via nei modelli con cellule staminali o, un giorno, in terapie mirate a prevenire o riparare malformazioni cardiache.
Citazione: Feng, Z., Gao, Y., Gao, H. et al. Essential role of NONO-HOXA1-Wnt axis in cardiomyocyte differentiation. Nat Commun 17, 2013 (2026). https://doi.org/10.1038/s41467-026-68760-2
Parole chiave: cardiopatia congenita, differenziazione dei cardiomiociti, segnalazione Wnt, modelli cardiaci con cellule staminali, regolazione genica