Clear Sky Science · it
Base strutturale per l’inversione della forcella e la regolazione di RAD51 dal complesso ligasi ubiquitina SCF dell’elica F-box 1
Come le cellule salvano una macchina di copiatura del DNA bloccata
Ogni volta che una cellula si divide, deve copiare miliardi di basi di DNA in modo rapido e accurato. Ma questa macchina di copiatura spesso incontra problemi: danni al DNA, sequenze difficili da duplicare o trattamenti farmacologici possono arrestarne il progresso. Quando ciò accade, le cellule si affidano a squadre di riparazione d’emergenza per stabilizzare e riavviare le forcelle di replicazione. Questo studio rivela, con dettagli strutturali senza precedenti, come uno di questi capi squadriglia — un complesso proteico costruito attorno all’elicasi FBH1 — rimodella il DNA bloccato e mantiene un altro importante fattore di riparazione, RAD51, strettamente controllato. Capire questa coreografia aiuta a spiegare come le cellule evitino rotture pericolose del genoma e perché le alterazioni di questi fattori siano collegate al cancro.
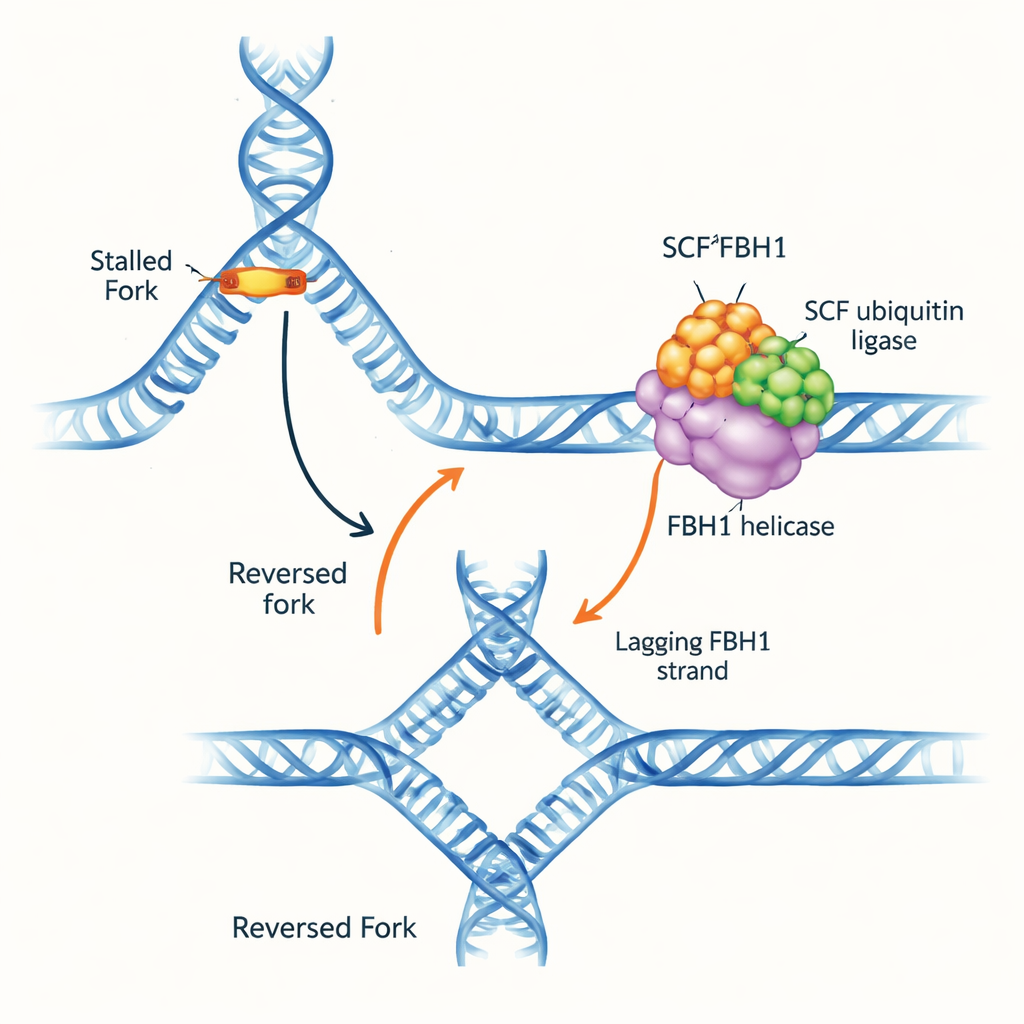
Un ingorgo sull’autostrada del DNA
Le forcelle di replicazione del DNA sono strutture a forma di Y dove la doppia elica viene srotolata e copiata. Quando la forcella incontra ostacoli, può invertirsi: i filamenti parentali si riappacificano e i filamenti neosintetizzati si appaiano tra loro, formando una giunzione a quattro vie. Questa “inversione della forcella” può guadagnare tempo per riparare il danno e riavviare la replicazione in sicurezza, ma se gestita male genera DNA fragile soggetto a rotture. Diversi motori molecolari sono noti per spingere le forcelle all’indietro afferrando il DNA a doppio filamento davanti alla forcella. FBH1, tuttavia, spiccava perché si comporta in modo diverso ed è frequentemente alterato nei tumori, suggerendo che agisca tramite una via distinta e di rilevanza medica.
Uno specialista delle forcelle con un lato preferito
Gli autori hanno purificato il complesso umano SCFFBH1, che combina l’elicasi FBH1 con un modulo per il marcataggio con ubiquitina (SCF). Hanno innanzitutto chiesto quali forme del DNA FBH1 preferisca. Usando saggi di legame e srotolamento, hanno mostrato che SCFFBH1 favorisce fortemente strutture davvero simili a forcelle, in particolare dove è presente un breve tratto di DNA a singolo filamento sul filamento stampo “in ritardo” — il lato copiato in piccoli frammenti. Su queste strutture, FBH1 srotola il DNA centinaia di volte più rapidamente che su una semplice estremità libera, indicando che un corretto aggancio alla giunzione della forcella sovralimenta l’attività del motore. Esperimenti a molecola singola con pinzette magnetiche hanno confermato che il complesso può srotolare e poi scorrere lungo il DNA a singolo filamento per migliaia di basi senza staccarsi, comportandosi come un motore potente e processivo.
Invertire la forcella tirando da dietro
Per capire come questo motore inverta effettivamente le forcelle, il gruppo ha testato substrati di forcella artificiali con o senza gap a singolo filamento. Diversamente da altri rimodellatori di forcella, SCFFBH1 non riusciva ad agire su una forcella completamente appaiata; richiedeva un gap sul filamento stampo in ritardo e si muoveva nella direzione 3′–5′ lungo quel filamento singolo. Questo movimento «tirando da dietro» spinge i filamenti parentali a ri-annealarsi mentre l’enzima resta bloccato alla giunzione della forcella. Una struttura ottenuta mediante crio-microscopia elettronica di SCFFBH1 legato a una forcella bloccata mostra il perché: una speciale patch carica positivamente, un «motivo di legame della giunzione» in un sottodominio di FBH1, si incunea proprio nel punto di biforcazione dove si incontrano i tre rami del DNA. Quando i ricercatori hanno mutato due amminoacidi chiave in questo motivo, l’inversione della forcella è diminuita di circa 25 volte in provetta, pur mantenendo abbastanza efficiente il nucleo di srotolamento. Nelle cellule, la stessa mutazione impediva il rallentamento normale delle forcelle di replicazione in risposta a un farmaco che induce stress, un segno distintivo del fallimento nell’invertire la forcella.
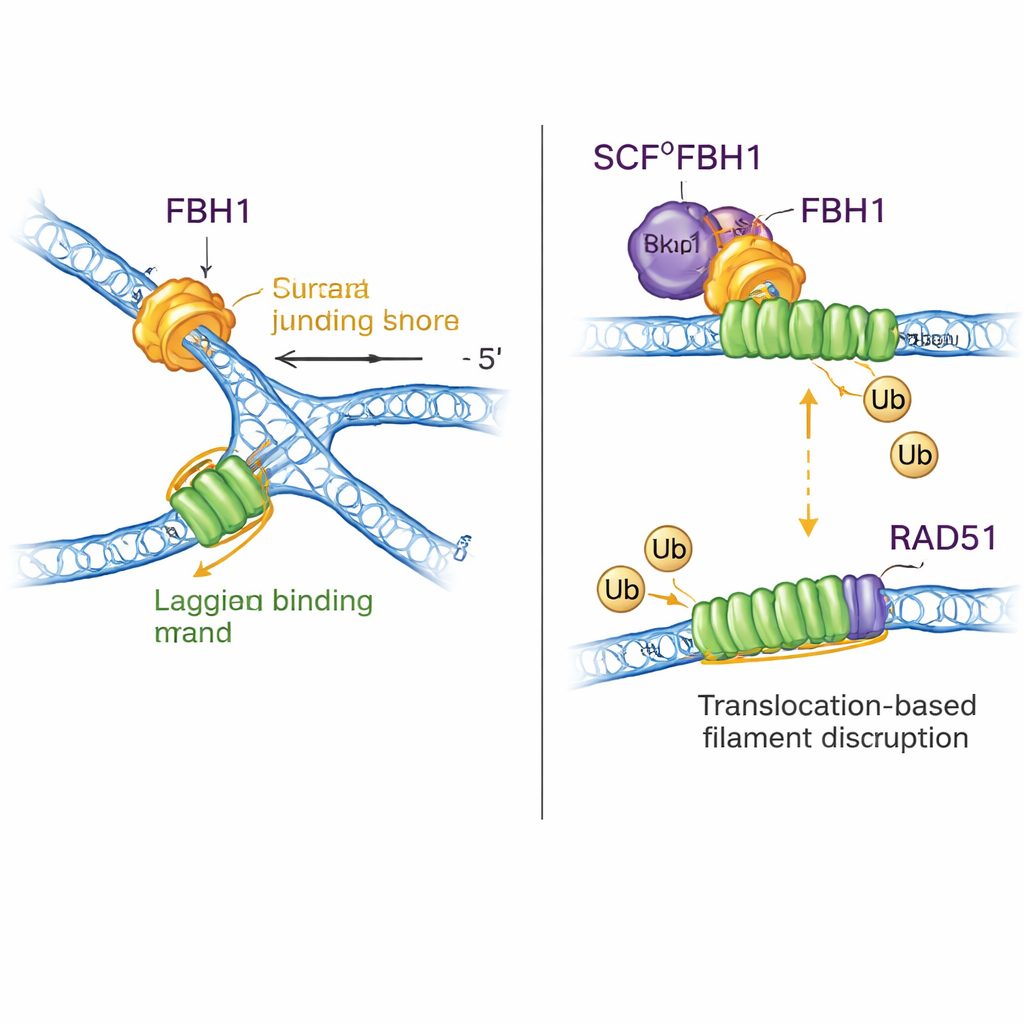
Ruolo doppio: rimodellare il DNA e rimuovere RAD51
FBH1 non è solo un motore; attraverso il complesso SCF aiuta anche ad attaccare piccole etichette di ubiquitina alle proteine. Le nuove strutture ricompongono quasi per intero il complesso SCFFBH1–DNA e mostrano che la «testa» che trasferisce l’ubiquitina della ligasi si trova a meno di 45 angstrom dal filamento in ritardo che emerge da FBH1. Inserendo per confronto strutture note di altre ligasi ubiquitina, gli autori propongono che questa geometria posizioni RAD51 — un enzima che forma filamenti sul DNA per promuovere la ricombinazione — proprio sulla linea di fuoco sul filamento in ritardo di una forcella bloccata. Lavori precedenti avevano dimostrato che FBH1 può meccanicamente rimuovere RAD51 dal DNA e anche marchiarlo con ubiquitina in modo che non rilegga facilmente. Il nuovo modello unifica queste idee: mentre FBH1 scorre lungo il filamento in ritardo per rimodellare la forcella, il vicino modulo SCF può etichettare le subunità di RAD51, contribuendo a smantellare o prevenire filamenti RAD51 eccessivi che altrimenti bloccherebbero un corretto processamento della forcella.
Cosa significa per la stabilità del genoma e il cancro
Nel complesso, lo studio dimostra che SCFFBH1 inverte le forcelle di replicazione bloccate usando un meccanismo distinto rispetto ad altri rimodellatori noti: afferra strettamente il punto di biforcazione mentre si trasla lungo il filamento stampo in ritardo da dietro, favorendo il riavvolgimento sicuro del DNA parentale senza formare una giunzione mobile a quattro vie di lunga durata. Allo stesso tempo, la sua ligasi ubiquitina integrata è strategicamente posizionata per rimuovere RAD51 dallo stesso filamento, prevenendo ricombinazione incontrollata durante lo stress di replicazione. Poiché FBH1 è frequentemente perso o mutato nei tumori, queste intuizioni strutturali e meccaniche aiutano a spiegare come tali neoplasie accumulino danni al DNA e perché possano rispondere in modo diverso a farmaci che inducono stress di replicazione o che prendono di mira vie correlate.
Citazione: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
Parole chiave: stress della replicazione del DNA, inversione della forcella, elicasi FBH1, regolazione di RAD51, stabilità del genoma