Clear Sky Science · it
Mappatura automatizzata della progressione della forcella di replicazione del DNA in cellule umane con ForkML
Perché è importante tracciare la velocità di copia del DNA
Ogni volta che una cellula umana si divide deve copiare più di tre miliardi di lettere del DNA in modo rapido e accurato. Se questo processo rallenta o si arresta, può danneggiare il genoma e contribuire a cancro e disturbi dello sviluppo. Tuttavia, fino ad ora, gli scienziati non disponevano di un metodo semplice per osservare esattamente a quale velocità le singole “macchine di copia” del DNA si muovono lungo tratti specifici del genoma umano. Questo articolo presenta ForkML, una nuova tecnica che sfrutta il sequenziamento nanopore e l’apprendimento automatico per automatizzare questo compito su scala senza precedenti.
Osservare le “macchine di copia” della cellula in tempo reale
Il DNA viene duplicato da piccole macchine molecolari chiamate forcelle di replicazione che si muovono lungo il doppio filamento formando nuove catene. ForkML consente ai ricercatori di osservare queste forcelle in modo indiretto aggiungendo un tag chimico innocuo, BrdU, nel DNA appena sintetizzato tramite due brevi impulsi separati da un intervallo di tempo noto. Poiché il BrdU è rilevabile su singole molecole di DNA dai sequenziatori nanopore, gli scienziati vedono due “strisce” marcate su ciascun filamento dove una forcella è passata durante i due impulsi. Misurando la distanza tra le strisce e dividendo per il tempo noto tra gli impulsi, possono calcolare la velocità con cui ogni forcella si è spostata in quella regione del genoma. 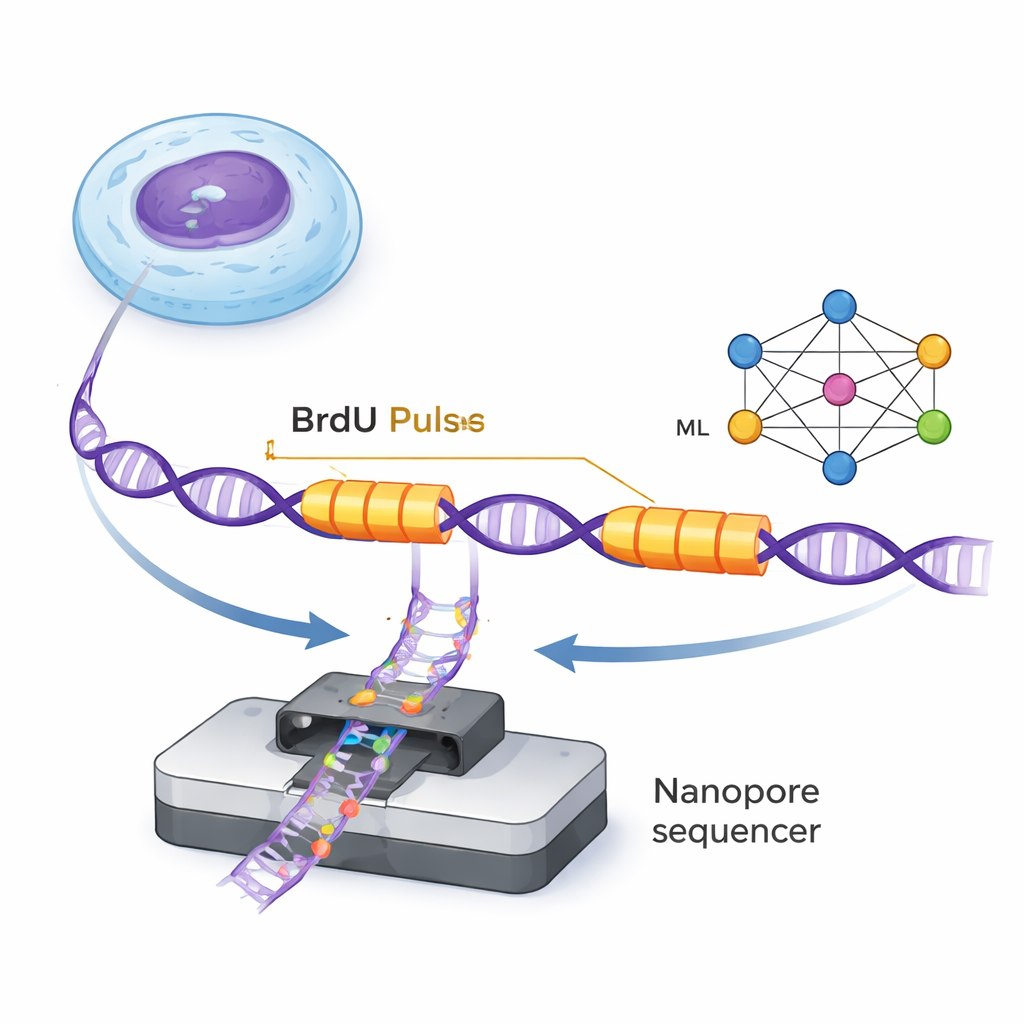
Insegnare a un computer a leggere le tracce chimiche
In lavori precedenti con lievito, gli autori potevano individuare queste tracce di BrdU con regole semplici, ma nelle cellule umane i segnali sono più deboli e complessi. Gli esperti umani riescono comunque a riconoscere il modello caratteristico—un aumento netto di BrdU all’inizio dell’impulso, seguito da un declino graduale al lavaggio—ma farlo a occhio per milioni di frammenti di DNA è impossibile. ForkML risolve questo addestrando una rete neurale, una forma di apprendimento automatico, su migliaia di esempi annotati manualmente. Il modello impara a classificare ogni tratto di DNA come sfondo oppure come forcella che si muove a destra o a sinistra, e a individuare con alta precisione l’inizio di ciascun impulso di BrdU. Questo permette la mappatura completamente automatizzata di migliaia di velocità di forcella individuali da una singola corsa di sequenziamento.
Misurare lo stress e le differenze lungo il genoma
Applicando ForkML a una linea cellulare di carcinoma del colon umano, il gruppo ha ottenuto oltre 2.000 misurazioni di velocità per esperimento e ha scoperto che la forcella tipica si muove a circa 1,2 kilobasi al minuto, coerente con metodi precedenti a minore rendimento. Quando le cellule sono state trattate con farmaci noti per rallentare la replicazione del DNA, ForkML ha rilevato chiaramente il rallentamento, dimostrando di misurare con sensibilità lo stress da replicazione. Poiché ogni forcella viene rimappata alla sua posizione nel genoma di riferimento, gli autori hanno potuto mettere in relazione la velocità con altre caratteristiche, come il timing di replicazione durante il ciclo cellulare, il grado di compattamento della cromatina e l’attività trascrizionale. 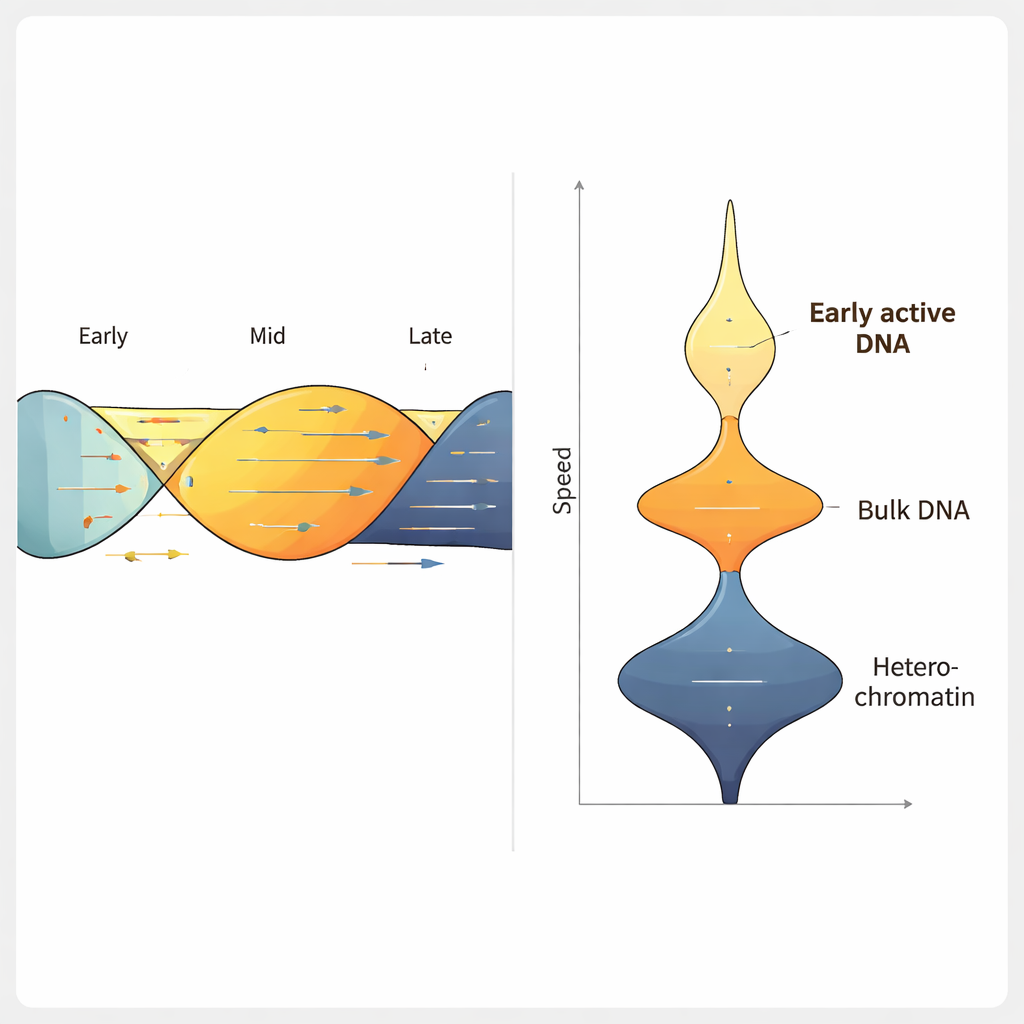
Rivelare dove inizia la copia del DNA e come i filamenti differiscono
Oltre alla velocità, ForkML identifica anche dove inizia e termina la replicazione del DNA, individuando i punti in cui le forcelle divergono o convergono sullo stesso frammento. Mappando più di 20.000 di questi siti di inizio, gli autori confermano che le cellule umane adottano una strategia mista: alcuni inizi avvengono in zone di inizio ben definite, ma la maggior parte degli inizi è sparsa lungo il genoma. Combinando la direzione delle forcelle con il filamento di DNA letto dal sequenziatore, ForkML può anche distinguere i tassi di sintesi del filamento leading e lagging, cosa che gli esperimenti classici basati sulle fibre non permettono. Test su sei diverse linee cellulari umane—sia normali che tumorali—mostrano che le stesse condizioni semplici di marcatura con BrdU funzionano in modo ampio e producono stime di velocità robuste in ciascun caso.
Un aggiornamento digitale di una tecnica classica
Per i non specialisti, ForkML può essere visto come una versione moderna e digitale del classico test delle fibre di DNA: usa uno schema di marcatura simile, ma sostituisce la microscopia manuale con il sequenziamento a letture lunghe e l’apprendimento automatico. Questo apporta un rendimento molto più elevato, il collocamento diretto di ogni misurazione sul genoma e informazioni più dettagliate su dove e quanto rapidamente il DNA viene copiato. Poiché il protocollo è semplice, compatibile con l’hardware nanopore attuale e adattabile ad altri organismi, ForkML è destinato a diventare uno strumento standard per lo studio della replicazione del DNA. In termini pratici, offre ai ricercatori un modo potente per collegare la velocità locale di copia del DNA—normale o sotto stress—all’attività genica, allo stato della cromatina e ai cambiamenti del genoma legati a malattie.
Citazione: Rojat, V., Ciardo, D., Tourancheau, A. et al. Automated mapping of DNA replication fork progression in human cells with ForkML. Nat Commun 17, 1975 (2026). https://doi.org/10.1038/s41467-026-68750-4
Parole chiave: Replicazione del DNA, velocità della forcella di replicazione, sequenziamento nanopore, marcatura con BrdU, apprendimento automatico in genomica