Clear Sky Science · it
Un atlante proteogenomico di 1032 metastasi cerebrali identifica sottotipi molecolari, paesaggi immunitari e vulnerabilità terapeutiche
Perché i tumori si diffondono nel cervello
Con il miglioramento delle cure oncologiche, sempre più persone vivono abbastanza a lungo perché i loro tumori si diffondano in sedi nuove, incluso il cervello. Queste metastasi cerebrali sono oggi una complicanza comune e spesso devastante, eppure i medici le trattano ancora in larga parte in base alla sede del tumore primario—polmone, mammella, pelle, colon—piuttosto che in base a come il cancro si è adattato alla vita nel cervello. Questo studio ha costruito un dettagliato “atlante” di oltre mille metastasi cerebrali per comprendere la loro biologia nascosta, come interagiscono con le cellule e il sistema immunitario cerebrale e dove potrebbero trovarsi nuove opportunità terapeutiche.
Costruire una mappa gigantesca dei tumori cerebrali
I ricercatori hanno raccolto dati da 1.032 metastasi cerebrali originate da diversi tumori primari, insieme a dozzine di tumori primari corrispondenti e ad alcuni tumori cerebrali primari aggressivi per confronto. Hanno combinato varie tecniche all’avanguardia: sequenziamento del DNA e dell’RNA, misurazioni su larga scala di proteine e metaboliti, mappature a singola cellula e spaziali di cellule tumorali e immunitarie, e organoidi derivati dal paziente coltivati in laboratorio. Integrando tutti questi livelli, l’obiettivo non era solo elencare geni, ma osservare come interi sistemi biologici si comportano all’interno delle metastasi cerebrali.
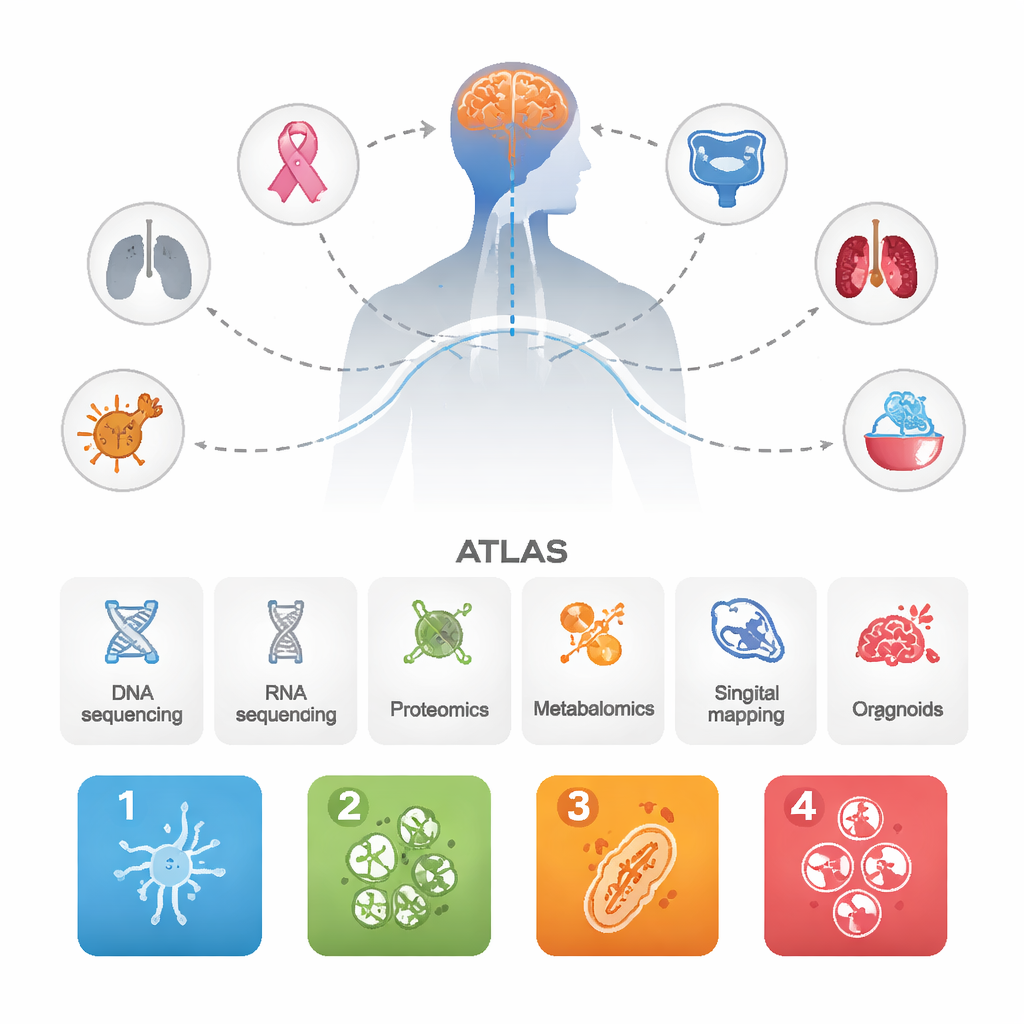
Quattro “personalità” ricorrenti delle metastasi cerebrali
Nonostante l’origine in molti organi diversi, le metastasi cerebrali si sono ripetutamente raggruppate in quattro sottotipi molecolari principali. Uno, chiamato BrMS1, appare “neuronale”: le cellule tumorali e il tessuto circostante esprimono molti programmi tipici del cervello e delle cellule nervose e mostrano una sorveglianza immunitaria relativamente attiva. BrMS2 è “infiltrato da cellule immunitarie”, ricco di cellule del sistema immunitario, in particolare linfociti T, e mostra un programma noto come transizione epitelio–mesenchimale, che allenta le adesioni cellulari e rimodella l’ambiente locale. BrMS3 è “metabolico”, dominato da cellule tumorali altamente attive che rimodellano il loro uso di energia—consumando carburante tramite vie come il metabolismo degli acidi grassi e la fosforilazione ossidativa. BrMS4 è “proliferativo”, caratterizzato da rapida divisione cellulare, tratti simili a cellule staminali e alta instabilità genomica, ma sorprendentemente povero di cellule immunitarie.
Cosa rivela l’ambiente del tumore
Zoomando a risoluzione singola e spaziale, il team ha mostrato che ogni sottotipo vive in un quartiere distinto all’interno del cervello. Le lesioni BrMS1 sono ricche di cellule di supporto cerebrale come astrociti e neuroni, suggerendo che il tumore imiti e co-opti strettamente il tessuto cerebrale normale. I tumori BrMS2, al contrario, sono punteggiati da densi ammassi di linfociti T, inclusi molti linfociti T “esausti” che esprimono molecole di checkpoint come PD-1, e presentano vasi sanguigni attivati e segnali infiammatori. Le lesioni BrMS3 si collocano in zone metabolicamente intense, mentre le lesioni BrMS4 formano isole di cellule in rapida divisione circondate da territorio relativamente povero di cellule immunitarie. In generale, lo studio ha rilevato che, nelle metastasi cerebrali—ma non nei tumori primari—la forte attivazione della transizione epitelio–mesenchimale tende a coincidere con un maggiore infiltrato di linfociti T, suggerendo che questo programma potrebbe favorire l’ingresso delle cellule immunitarie.
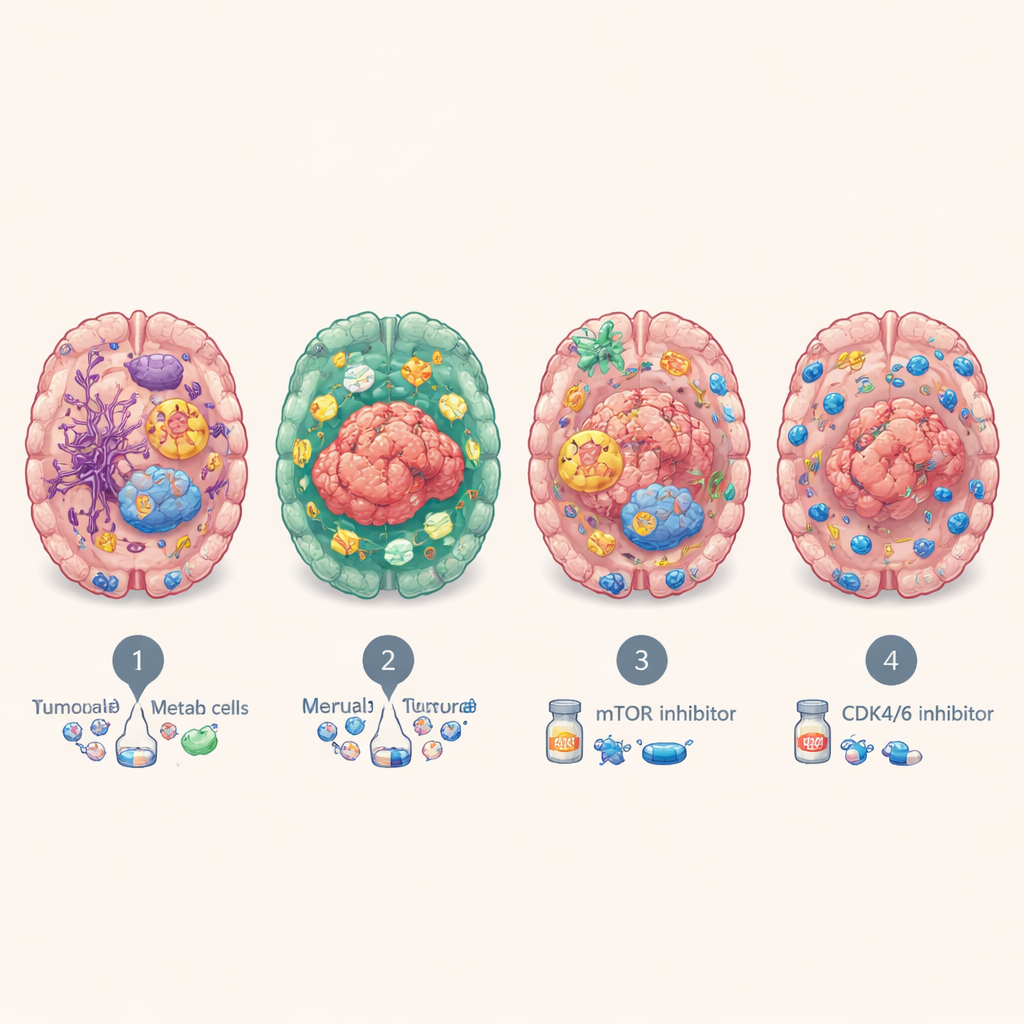
Indizi per il trattamento e l’esito dei pazienti
Queste personalità molecolari non erano solo teoriche. I pazienti con il sottotipo immune-infiltrato BrMS2 tendevano a vivere più a lungo rispetto a quelli con il sottotipo proliferativo BrMS4, che presentava costantemente i peggiori esiti. Testando farmaci su organoidi derivati dai pazienti, il team ha scoperto che i tumori metabolici BrMS3 erano particolarmente sensibili al blocco della via di segnalazione mTOR, che controlla crescita e metabolismo cellulare, e che i tumori a rapida divisione BrMS4 erano più vulnerabili agli inibitori di CDK4/6, farmaci che rallentano il ciclo cellulare. Analisi separate suggerivano che i tumori BrMS1 potrebbero rispondere meglio alla radioterapia, mentre l’ambiente infiammato e ricco di checkpoint di BrMS2 potrebbe renderlo più suscettibile a immunoterapie che rivitalizzano i linfociti T esausti—sebbene ciò richieda conferma diretta in pazienti con metastasi cerebrali.
Cosa significa per le persone con metastasi cerebrali
Questo atlante mostra che, una volta raggiunto il cervello, le cellule tumorali tendono a convergere in alcuni stati biologici condivisi che attraversano l’origine primitiva. Conoscere se la metastasi cerebrale di una persona è di tipo neuronale, ricca di cellule immunitarie, metabolica o altamente proliferativa potrebbe in futuro guidare trattamenti più personalizzati—ad esempio scegliendo tra radioterapia, immunoterapia o farmaci che mirano al metabolismo o alla divisione cellulare. Pur non cambiando ancora lo standard di cura, il lavoro fornisce una mappa dettagliata per la ricerca futura e per studi clinici mirati a trasformare queste vulnerabilità molecolari in terapie più efficaci e precise per i pazienti con metastasi cerebrali.
Citazione: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
Parole chiave: metastasi cerebrali, sottotipi tumorali, microambiente tumorale, immunoterapia oncologica, metabolismo del cancro