Clear Sky Science · it
La composizione dei fosfolipidi influenza fortemente l’assemblaggio delle proteine a β‑barile nelle membrane esterne batteriche purificate
Perché i rivestimenti batterici contano
I «superbatteri» resistenti ai farmaci rappresentano una minaccia crescente perché molti antibiotici semplicemente non riescono a superare le loro robuste difese esterne. Questo studio analizza in dettaglio una componente chiave di quella difesa nei batteri Gram‑negativi come E. coli: un involucro protettivo ricco di proteine a forma di barile e grassi specializzati. Facendo luce su come la miscela di questi lipidi controlli la costruzione del rivestimento esterno, gli autori individuano punti deboli che potrebbero essere sfruttati nella progettazione di futuri antibiotici.
Lo scudo a doppia parete
I batteri Gram‑negativi sono particolari perché possiedono due membrane. La membrana interna gestisce le funzioni cellulari quotidiane, mentre la membrana esterna funziona come un impermeabile robusto che impedisce l’ingresso di molte tossine e antibiotici. Questo strato esterno è composto da due tipi di lipidi: fosfolipidi comuni sul lato interno e uno zucchero‑grasso rigido chiamato lipopolisaccaride (LPS) sul lato esterno. Attraverso questo guscio sono infilate molte proteine a «beta‑barile» — cilindri cavi che formano pori e porte per i nutrienti. Una macchina molecolare chiamata BAM (dall’inglese barrel assembly machine) è responsabile del ripiegamento di queste proteine e della loro inserzione nella membrana esterna.
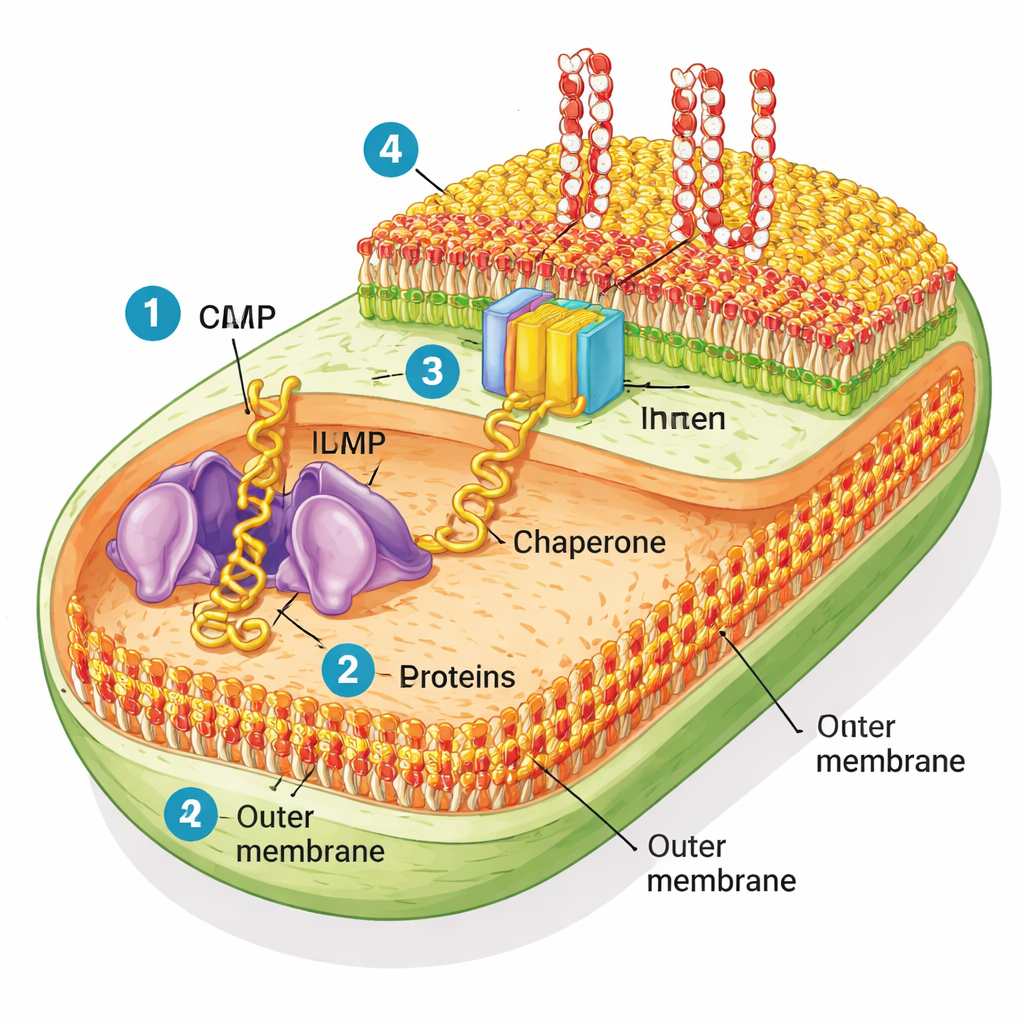
Ricreare il rivestimento batterico in provetta
Per verificare l’efficacia di BAM in un contesto realistico, i ricercatori hanno purificato parti della membrana esterna di E. coli, creando piccole bolle che chiamano «omicron native OMs». Diversamente dalle membrane artificiali semplici usate in molti studi di laboratorio, queste membrane native conservano l’intero mix di proteine e lipidi. Il team ha poi utilizzato una fabbrica proteica senza cellule per sintetizzare nuove proteine della membrana esterna da zero e ha osservato se BAM in queste bolle native riuscisse a ripiegarle e inserirle. Si sono concentrati su una proteina modello a beta‑barile chiamata EspP, insieme ad altre. In presenza della proteina helper SurA, BAM nelle membrane native ha ripiegato EspP in modo efficiente, e questo processo è stato bloccato da un noto antibiotico che prende di mira BAM chiamato darobactin — una prova evidente che la macchina naturale rimaneva attiva.
Quando la miscela lipidica va in tilt
Gli autori hanno poi chiesto cosa accade quando l’equilibrio lipidico della membrana esterna è disturbato. Hanno studiato ceppi mutanti di E. coli privi di sistemi chiave che normalmente correggono la presenza di fosfolipidi nella falda esterna. Un sistema, MlaA, riporta i fosfolipidi fuori posto verso la membrana interna; un altro, l’enzima PldA, li frammenta. Usando membrane native prelevate da questi mutanti, il gruppo ha scoperto che l’assemblaggio di EspP mediato da BAM diminuiva in modo evidente nei ceppi privi di MlaA ed era gravemente compromesso quando PldA era assente. Questi effetti non dipendevano dalla perdita di BAM stesso o di altre proteine principali, che erano ancora presenti a livelli normali, indicando invece l’ambiente lipidico alterato come causa del problema.
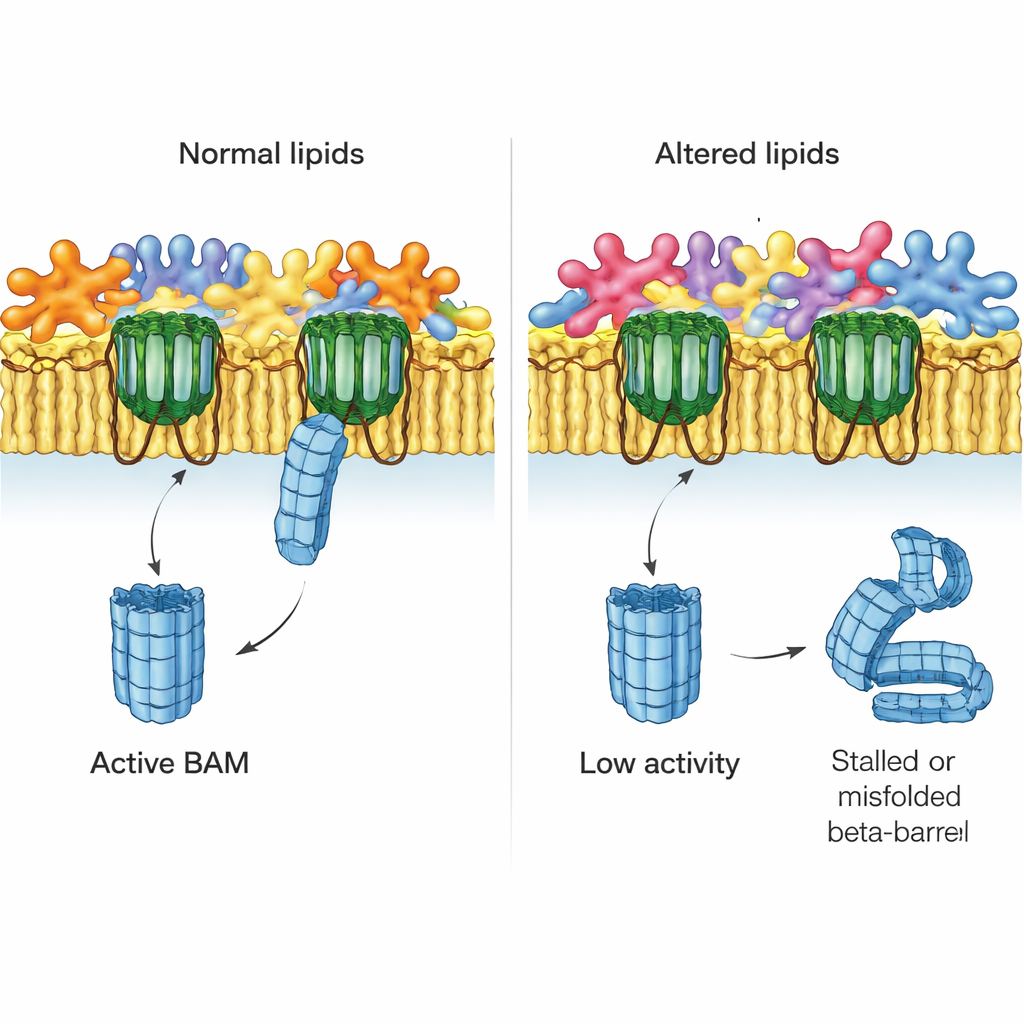
Mappare il paesaggio lipidico in dettaglio
Per collegare la funzione alla chimica, i ricercatori hanno sviluppato un metodo sensibile di spettrometria di massa per catalogare centinaia di fosfolipidi individuali nelle cellule intere e nelle membrane esterne purificate. In E. coli normale, hanno confermato che un tipo di lipide (fosfatidiletanolamina, o PE) è arricchito nella membrana esterna, mentre altri (fosfatidilglicerolo e cardiolipina) sono relativamente impoveriti lì. Hanno anche trovato che i «liso‑lipidi», che possiedono una sola coda grassa e tendono a curvare le membrane, sono sorprendentemente concentrati nella membrana esterna. Nei ceppi mutanti, soprattutto in quelli privi di PldA, questi schemi risultavano sconvolti: le differenze abituali tra membrana interna ed esterna si riducevano o addirittura si invertivano, e la lunghezza e il tipo delle code grasse cambiavano. I ceppi con i profili lipidici più alterati erano gli stessi in cui BAM funzionava peggio.
Implicazioni per le strategie antibiotiche
Nel complesso, il lavoro dimostra che la membrana esterna non è solo un’impalcatura passiva per le proteine. La sua precisa composizione di fosfolipidi influenza fortemente l’efficienza con cui BAM costruisce i pori a beta‑barile necessari alla sopravvivenza del batterio. Quando l’equilibrio lipidico è disturbato, meno complessi BAM funzionano correttamente e alcuni lavorano più lentamente. Sebbene i batteri vivi possano compensare tali cambiamenti in modi che un sistema in provetta non può riprodurre, questo studio mette in luce come modulare o disturbare specifici lipidi possa indebolire il rivestimento batterico. Questa intuizione apre nuove possibilità per farmaci che mirino direttamente a BAM o che sbilancino in modo sottile i lipidi della membrana esterna, rendendo anche i batteri Gram‑negativi più resistenti più vulnerabili.
Citazione: Nilaweera, T.D., Brandes, N.T., LaCroix, I.S. et al. Phospholipid composition strongly affects the assembly of β barrel proteins into purified bacterial outer membranes. Nat Commun 17, 1915 (2026). https://doi.org/10.1038/s41467-026-68743-3
Parole chiave: batteri Gram‑negativi, proteine della membrana esterna, assemblaggio a beta‑barile, lipidi batterici, resistenza agli antibiotici