Clear Sky Science · it
La chinurenina media la tossicità intestinale indotta dalla chemioterapia attraverso la modulazione del microbiota intestinale
Perché questo è importante per le persone in chemioterapia
La chemioterapia salva vite, ma spesso comporta effetti collaterali intestinali debilitanti — dolore, diarrea, perdita di peso — che possono costringere i medici a ridurre le dosi o interrompere il trattamento prematuramente. Questo studio scopre una catena di eventi nascosta tra una sostanza presente nel sangue, le cellule immunitarie e i microbi intestinali che aiuta a spiegare perché un farmaco antitumorale comune, l’oxaliplatino, può essere così aggressivo per l’intestino, e indica nuovi modi per proteggere i pazienti senza indebolire la terapia antitumorale.
Un legame chimico tra trattamento e danno intestinale
I ricercatori hanno iniziato dai pazienti con cancro colorettale trattati con chemioterapia a base di oxaliplatino. Hanno confrontato campioni di sangue di persone che svilupparono gravi effetti collaterali intestinali con quelli di chi tollerò meglio il trattamento. Attraverso un profilo chimico mirato, hanno scoperto che diversi prodotti di degradazione dell’amminoacido triptofano erano più alti nel gruppo ad alta tossicità, con una molecola — la L‑chinurenina — che emergeva come la più fortemente elevata. Nei pazienti con livelli più alti di L‑chinurenina nel sangue si osservavano anche maggiori segni di infiammazione e un numero inferiore di globuli bianchi, suggerendo che questa molecola potrebbe essere direttamente collegata al danno legato al trattamento.
Dimostrare causa ed effetto nei topi
Per andare oltre la correlazione, il team si è rivolto a modelli murini. Quando topi sani ricevettero alte dosi di oxaliplatino, svilupparono segni classici di lesione intestinale: perdita di peso, colon accorciati, edema della parete intestinale, riduzione delle cellule in divisione e aumento delle cellule morenti nel rivestimento intestinale. Anche in questi animali si osservò un netto aumento della L‑chinurenina nel sangue, rispecchiando i dati umani. Quando i ricercatori somministrarono L‑chinurenina aggiuntiva ai topi trattati con oxaliplatino, il danno intestinale peggiorò — pur senza ridurre l’efficacia del farmaco contro i tumori. Al contrario, rimuovendo o bloccando l’enzima IDO1, che converte il triptofano in L‑chinurenina, i topi divennero molto più resistenti alla tossicità intestinale mantenendo comunque i benefici della chemioterapia.
Cellule immunitarie e microbi intestinali nel mirino
Approfondendo, gli scienziati hanno investigato quali cellule fossero responsabili della produzione eccessiva di L‑chinurenina durante il trattamento. Hanno scoperto che l’oxaliplatino stimola alcune cellule immunitarie (linfociti T CD8) a rilasciare la proteina segnale interferone‑gamma, che a sua volta attiva IDO1 nelle cellule mieloidi vicine — una classe di globuli bianchi. Topi ingegnerizzati in cui solo le cellule mieloidi mancavano di IDO1 produssero molta meno L‑chinurenina e furono protetti dal danno intestinale, mentre eliminare IDO1 solo nelle cellule del rivestimento intestinale ebbe poco effetto. Allo stesso tempo, cambiò la composizione del microbiota intestinale. Nei topi normali, oxaliplatino e alti livelli di L‑chinurenina erano associati alla perdita di un batterio benefico, Lactobacillus johnsonii. Al contrario, i topi con L‑chinurenina ridotta mantennero livelli più alti di L. johnsonii. Quando i batteri intestinali furono azzerati con antibiotici, l’effetto protettivo della bassa L‑chinurenina svanì, e quando i batteri provenienti da topi a basso contenuto di chinurenina furono trapiantati in topi normali, i riceventi divennero più resistenti al danno intestinale indotto dall’oxaliplatino.
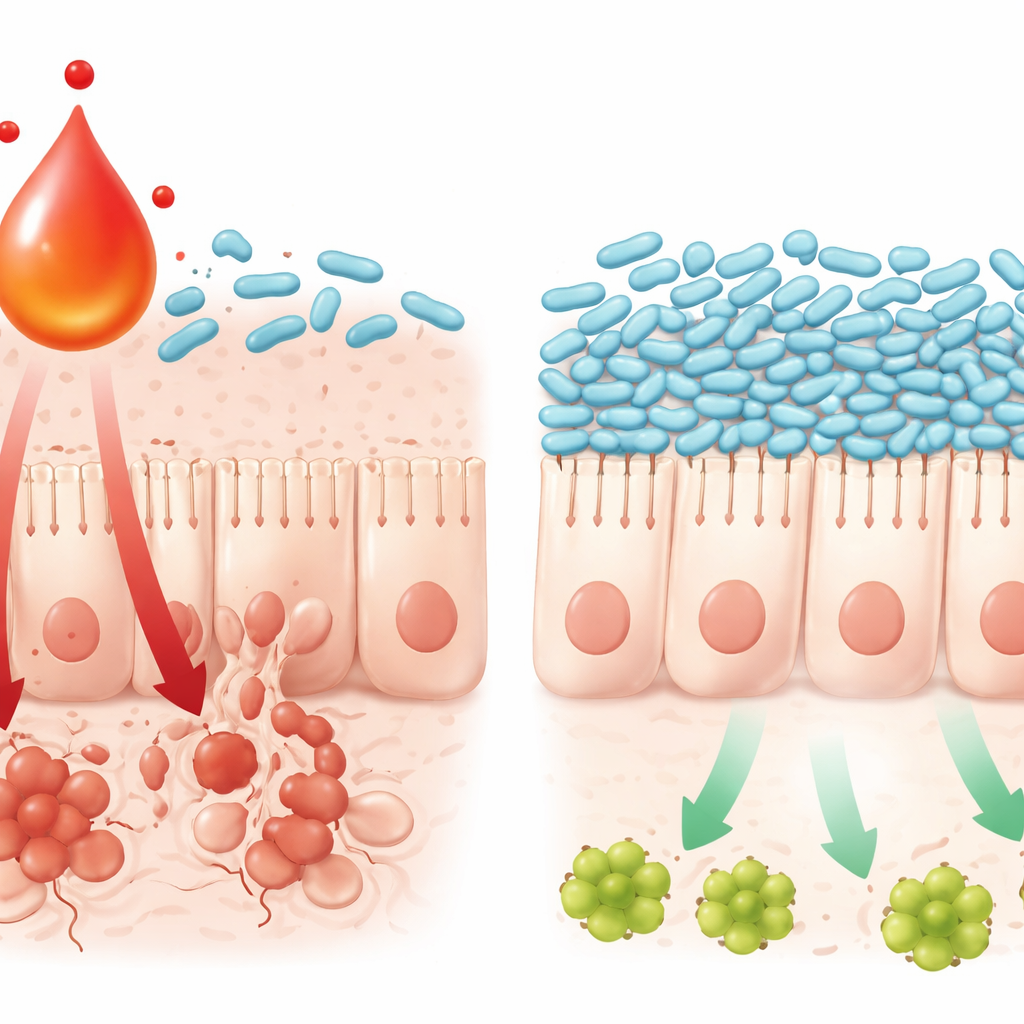
Come un metabolita induce la morte cellulare nell’intestino
Lo studio ha anche tracciato come questa interazione chimica‑microbica danneggi il rivestimento intestinale. Alti livelli di L‑chinurenina erano associati a una maggiore attività di una nota via infiammatoria nei tessuti intestinali, la via TNFα/JNK, che spinge le cellule verso la morte programmata. In colture cellulari, la combinazione di oxaliplatino e L‑chinurenina rese le cellule intestinali più inclini ad attivare questa via e a morire, mentre l’aggiunta del batterio L. johnsonii attenuò il segnale e preservò la sopravvivenza cellulare. La L‑chinurenina stessa poteva rallentare la crescita e compromettere i meccanismi di sopravvivenza di L. johnsonii in piastre di laboratorio, contribuendo a spiegare perché il batterio scompare quando il metabolita si accumula. Nel complesso, questi risultati delineano un circuito auto‑alimentante: la chemioterapia innesca segnali immunitari, le cellule immunitarie aumentano la L‑chinurenina, questa altera batteri amichevoli come L. johnsonii, e la comunità microbica modificata amplifica a sua volta segnali infiammatori che uccidono le cellule intestinali.
Nuove strategie per proteggere i pazienti durante il trattamento
È incoraggiante che il lavoro indichi anche strategie pratiche. Il trattamento dei topi con un farmaco chiamato Epacadostat, che inibisce IDO1, ridusse i livelli di L‑chinurenina e attenuò nettamente le lesioni intestinali indotte dall’oxaliplatino senza diminuire il controllo tumorale. In un approccio complementare, il team ha ingegnerizzato un ceppo innocuo di E. coli per sovraprodurre un enzima che degrada la L‑chinurenina nell’intestino. I topi a cui furono somministrati questi batteri ingegnerizzati furono protetti allo stesso modo dalla tossicità intestinale, sempre senza compromettere gli effetti antitumorali della chemioterapia. Anche la somministrazione di L. johnsonii alleviò i sintomi e preservò la struttura intestinale.
Cosa significa per le persone con il cancro
Nel complesso, questo studio rivela che un singolo metabolita indotto dal trattamento — la L‑chinurenina — agisce come un tassello chiave tra chemioterapia, sistema immunitario, microbi intestinali e lesione intestinale. Dimostrando che bloccarne la produzione, favorirne la degradazione o ripristinare batteri protettivi può attenuare l’impatto della chemioterapia sull’intestino, la ricerca apre la strada a terapie di supporto che mantengano i pazienti più forti e più a loro agio durante la lotta contro il cancro.
Citazione: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
Parole chiave: effetti collaterali della chemioterapia, microbioma intestinale, metabolismo del triptofano, L-chinurenina, cancro colorettale