Clear Sky Science · it
Riduzione elettrochimica del CO2 a livello di ampere verso ossigenati multi‑carbonio in elettrolita acido mediante ricostruzione del microambiente superficiale
Trasformare un problema climatico in liquidi utili
Il biossido di carbonio derivante dalla combustione di combustibili fossili riscalda il pianeta, ma rappresenta anche una possibile materia prima. Questo studio esplora come convertire il CO2 in prodotti chimici liquidi di valore, come etanolo e acido acetico, usando elettricità. I ricercatori dimostrano che riprogettando con attenzione l’ambiente immediato di un elettrodo di rame è possibile rendere questa trasformazione più rapida, efficiente e compatibile con condizioni acide severe che normalmente ostacolano tali reazioni.
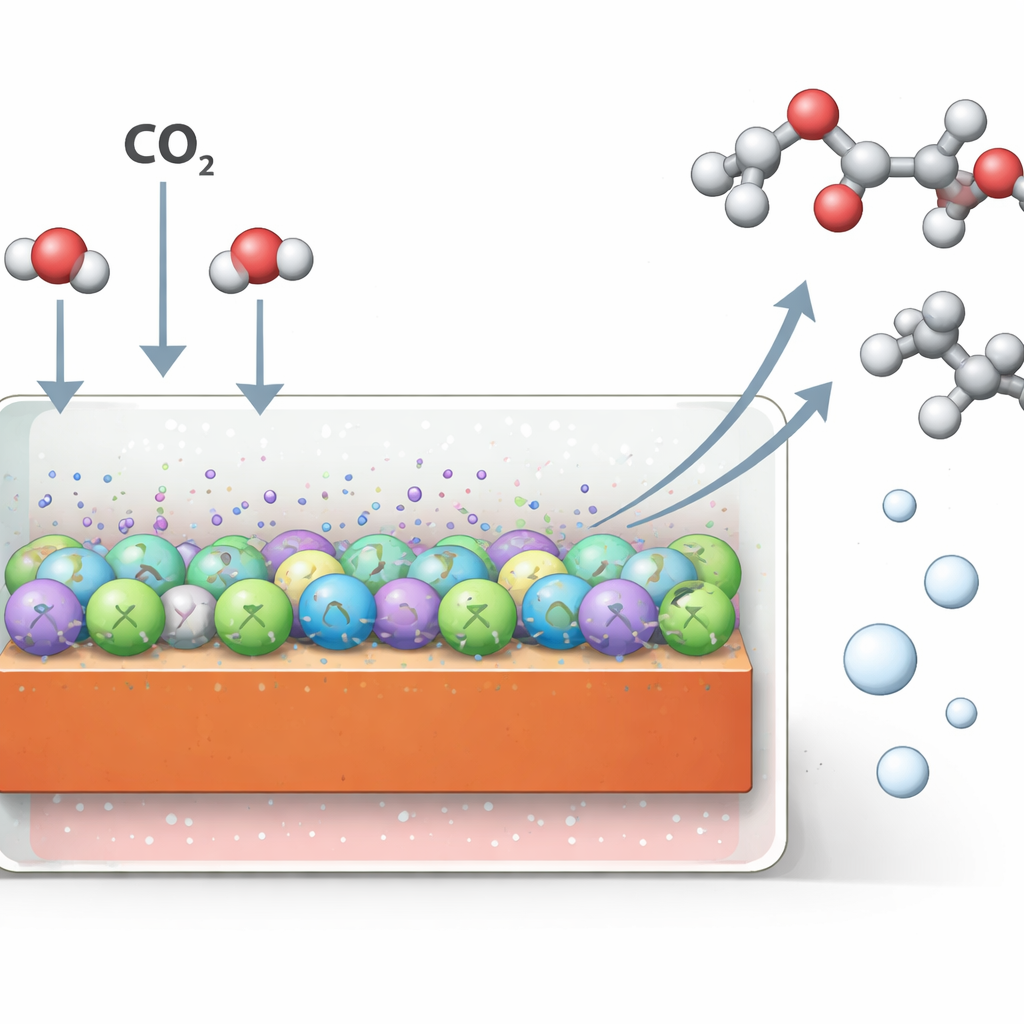
Perché è difficile produrre combustibili liquidi dal CO2
Gli scienziati sognano da tempo di usare elettricità rinnovabile in eccesso per convertire il CO2 in prodotti ad elevato contenuto energetico, immagazzinando sole e vento in forma chimica. Il rame è uno dei pochi materiali in grado di unire il CO2 in molecole multi‑carbonio, inclusi alcoli e acidi già impiegati dall’industria. Gran parte dei progressi finora, tuttavia, ha sfruttato liquidi alcalini (basici), che fanno disperdere il CO2 in carbonati invisibili e intasare i dispositivi con sali. I liquidi acidi evitano questi problemi, ma in tali condizioni il rame tende a privare di ossigeno intermedi promettenti, favorendo gas semplici come etilene e idrogeno invece di liquidi contenenti ossigeno.
Costruire una superficie di rame più intelligente
Per superare questo compromesso, il team ha creato un elettrodo di rame modificato che chiamano IL@Cu. Lo hanno ottenuto riducendo l’ossido di rame in una soluzione acquosa contenente un liquido ionico appositamente selezionato, un sale che è liquido vicino alla temperatura ambiente. Componenti cariche positivamente di questo liquido ionico, basate su una molecola chiamata Bmim, si legano in modo uniforme a piccolissimi nanoparticelle di rame, conferendo alla superficie una lieve carica positiva. Microscopia avanzata e tecniche a raggi X hanno confermato che il rame sottostante rimane metallico mentre il liquido ionico forma uno strato sottile e ben ancorato che modifica l’organizzazione di altri ioni e dell’acqua all’interfaccia dove avviene la conversione del CO2.
Portare le prestazioni a livelli industriali
Quando i ricercatori hanno testato IL@Cu in una soluzione acida fluente di solfato di potassio, hanno ottenuto correnti elettriche molto elevate—fino a due ampere per centimetro quadrato, paragonabili all’elettrolisi industriale. In queste condizioni impegnative, il rame modificato ha prodotto prodotti multi‑carbonio con un’efficienza faradica di circa l’83%, cioè la maggior parte degli elettroni è stata usata per formare le molecole desiderate anziché reazioni laterali inutili. Ancora più impressionante, circa il 60% della corrente è andato specificamente a prodotti liquidi contenenti ossigeno, e l’etanolo da solo ha rappresentato circa la metà di questa frazione. Il dispositivo ha anche impiegato il CO2 in ingresso in modo molto efficace: quasi quattro quinti del gas che lo attraversava venivano convertiti in un unico passaggio, e il catalizzatore ha mantenuto attività e struttura per oltre 100 ore di funzionamento.
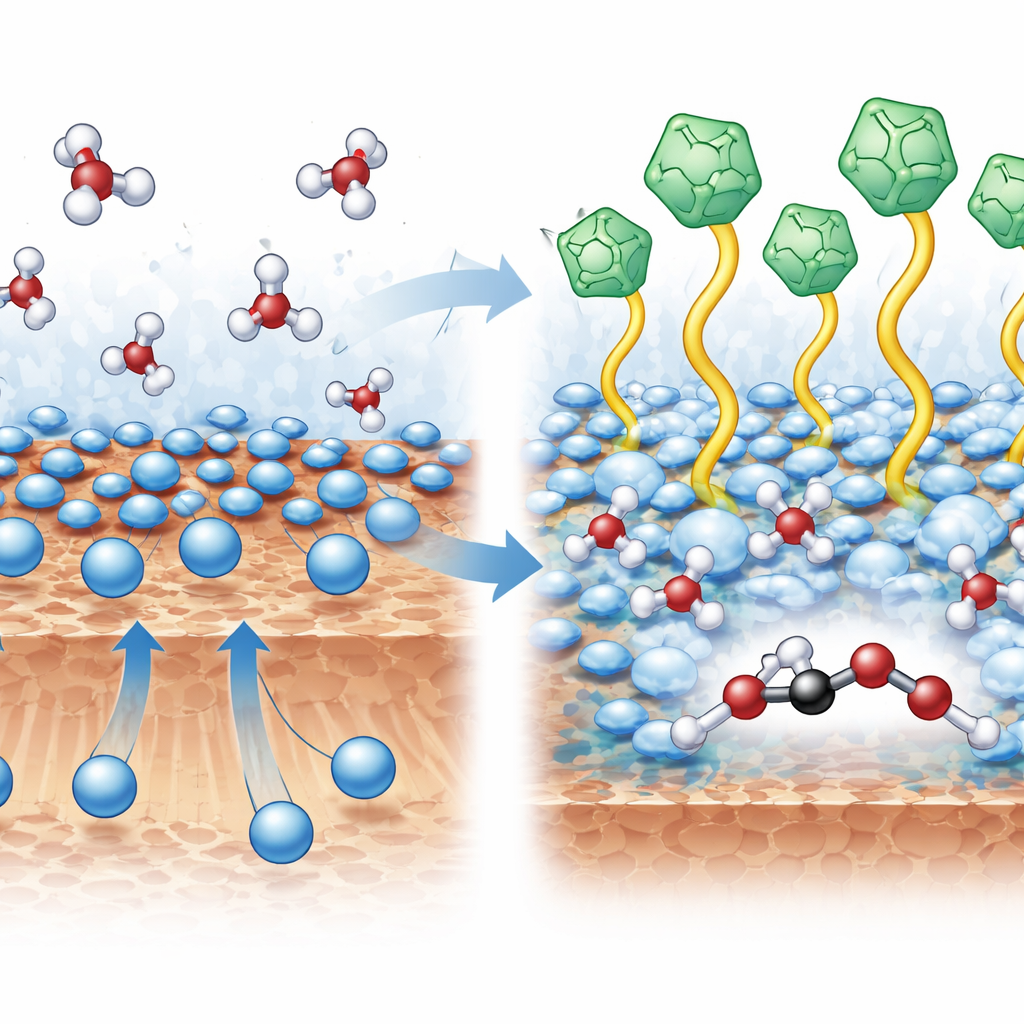
Riorganizzare acqua e ioni sulla superficie
Il cuore del progresso risiede nella disposizione microscopica di ioni e acqua nel luogo in cui avviene la reazione. Misure spettroscopiche e simulazioni al computer hanno rivelato che i cationi del liquido ionico respingono gli ioni potassio vicini dalla superficie del rame. Questo apre spazio perché le molecole d’acqua si avvicinino e formino una rete di legami a idrogeno più connessa attorno ai principali intermedi a due carboni. Con il potassio tenuto a una distanza ottimale, i frammenti contenenti carbonio possono più facilmente accoppiarsi tra loro anziché staccarsi come monossido di carbonio. Allo stesso tempo, la rete d’acqua circostante aiuta a preservare l’ossigeno nelle molecole in crescita invece di permettere la rottura dei legami e il rilascio di etilene gassoso. Calcoli quantomeccanici hanno mostrato che questo ambiente riorganizzato abbassa la barriera energetica per la formazione del legame carbonio–carbonio e inclina il percorso di reazione verso liquidi ricchi di ossigeno come l’etanolo.
Progettare lo strato invisibile che conta
In sostanza, lo studio dimostra che controllare il “microambiente”—l’assetto su scala nanometrica di ioni e acqua su un elettrodo—può essere importante tanto quanto scegliere il metallo giusto. Legando molecole di liquido ionico al rame, gli autori aumentano simultaneamente la velocità di conversione del CO2, favoriscono prodotti multi‑carbonio più facili da immagazzinare e trasportare e mantengono il dispositivo stabile in soluzioni acide più pratiche per l’uso a lungo termine. Questa strategia di riprogettare il sottile e invisibile strato in cui avvengono le reazioni può guidare lo sviluppo di sistemi di nuova generazione che trasformano il CO2 di scarto in prodotti chimici e combustibili utili a scale rilevanti per mitigare il cambiamento climatico.
Citazione: Yin, Y., Ling, Z., Liu, S. et al. Ampere-level CO2 electroreduction to multi-carbon oxygenates in acidic electrolyte through surface microenvironment reconstruction. Nat Commun 17, 2353 (2026). https://doi.org/10.1038/s41467-026-68739-z
Parole chiave: riduzione elettrochimica del CO2, catalizzatore di rame, liquidi ionici, produzione di etanolo, riciclo elettrochimico del CO2