Clear Sky Science · it
Determinazione basata sul click dell’accumulo di molecole in Escherichia coli
Perché le piccole molecole faticano a raggiungere batteri pericolosi
La medicina moderna dipende dagli antibiotici, ma alcuni dei batteri più pericolosi sono oggi protetti da pareti esterne robuste che impediscono l’ingresso di molti farmaci. I batteri Gram‑negativi come Escherichia coli possiedono una barriera di membrana esterna particolarmente efficace, che rende difficile progettare molecole in grado di entrare e raggiungere i bersagli intracellulari. Questo articolo presenta un nuovo test di laboratorio, chiamato saggio CHAMP, che permette agli scienziati di misurare rapidamente quanto bene migliaia di piccole molecole riescono a oltrepassare queste difese e ad accumularsi all’interno di cellule viventi di E. coli.
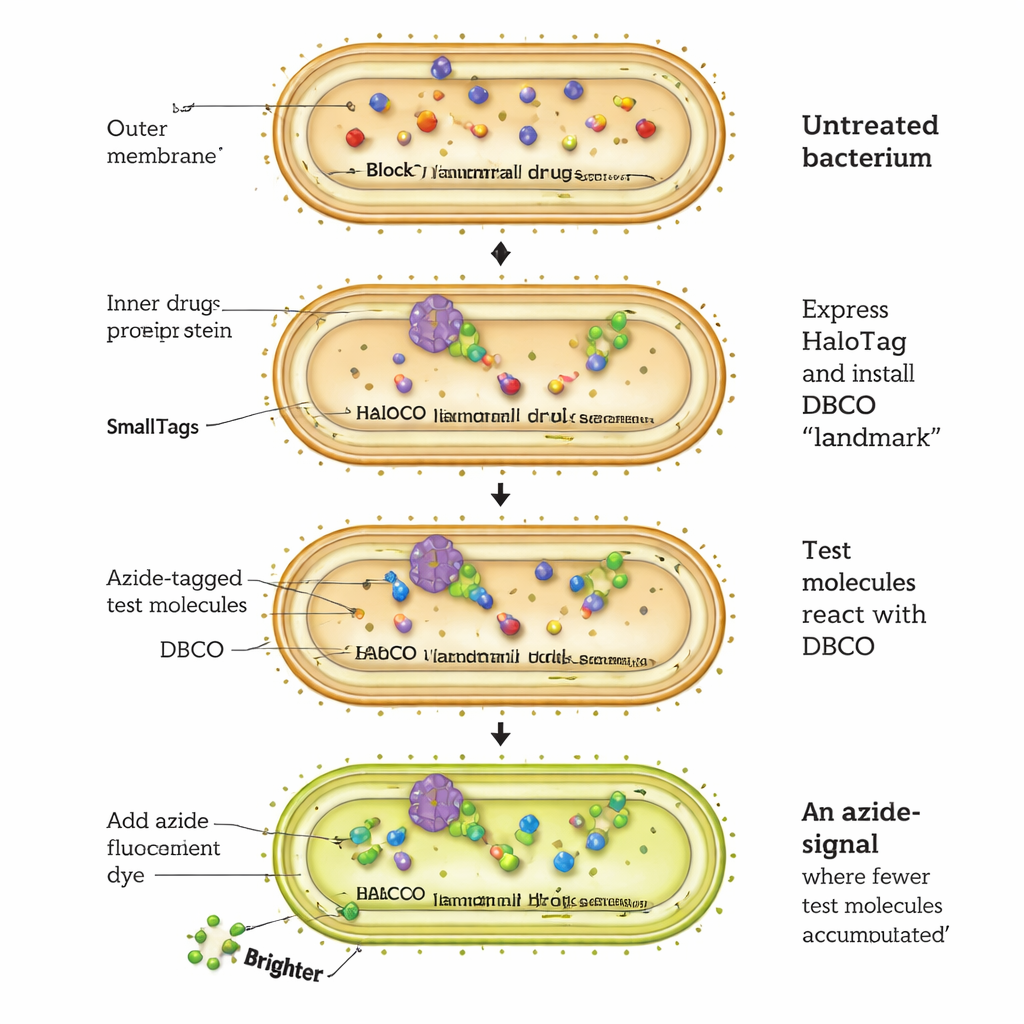
Un nuovo modo per osservare i farmaci entrare nelle cellule batteriche
La scoperta tradizionale di antibiotici si basava su composti naturali e test di crescita semplici per vedere se i batteri sopravvivevano o meno. Questi test non rivelano però quanto farmaco sia effettivamente entrato nella cellula, né dove sia andato una volta all’interno. Gli autori hanno voluto sviluppare un metodo diretto e ampiamente utilizzabile per tracciare l’ingresso dei farmaci nel citosol batterico — il fluido interno dove risiedono molti bersagli antibiotici. L’obiettivo era superare letture grezze come la concentrazione minima inibente, che mescolano effetti di assorbimento, legame al bersaglio e processi biologici a valle, ottenendo invece una misura pulita dell’accumulo intracellulare.
Trasformare i batteri in piccoli registratori chimici
Il saggio CHAMP funziona riprogettando una proteina batterica chiamata HaloTag in una sorta di piattaforma molecolare. Le cellule di E. coli sono ingegnerizzate per produrre HaloTag nel citosol. I ricercatori prima legano a HaloTag una particolare maniglia chimica, un alchino "stressato" chiamato DBCO, tramite un breve linker cloroalchano. Quindi esponendo i batteri a molecole di prova, ciascuna dotata di un piccolo tag azido, solo quelle molecole che attraversano la membrana esterna, passano la membrana interna e raggiungono il citosol possono reagire con la maniglia DBCO in una reazione di “click” altamente selettiva, marcando permanentemente HaloTag. Infine, le cellule vengono trattate con un colorante fluorescente con tag azido che può legarsi solo ai DBCO rimasti liberi. Più intensa è la fluorescenza, meno molecole di prova sono arrivate nel citosol; cellule più deboli indicano un accumulo maggiore.
Indagare come chimica e biologia modellano l’ingresso dei farmaci
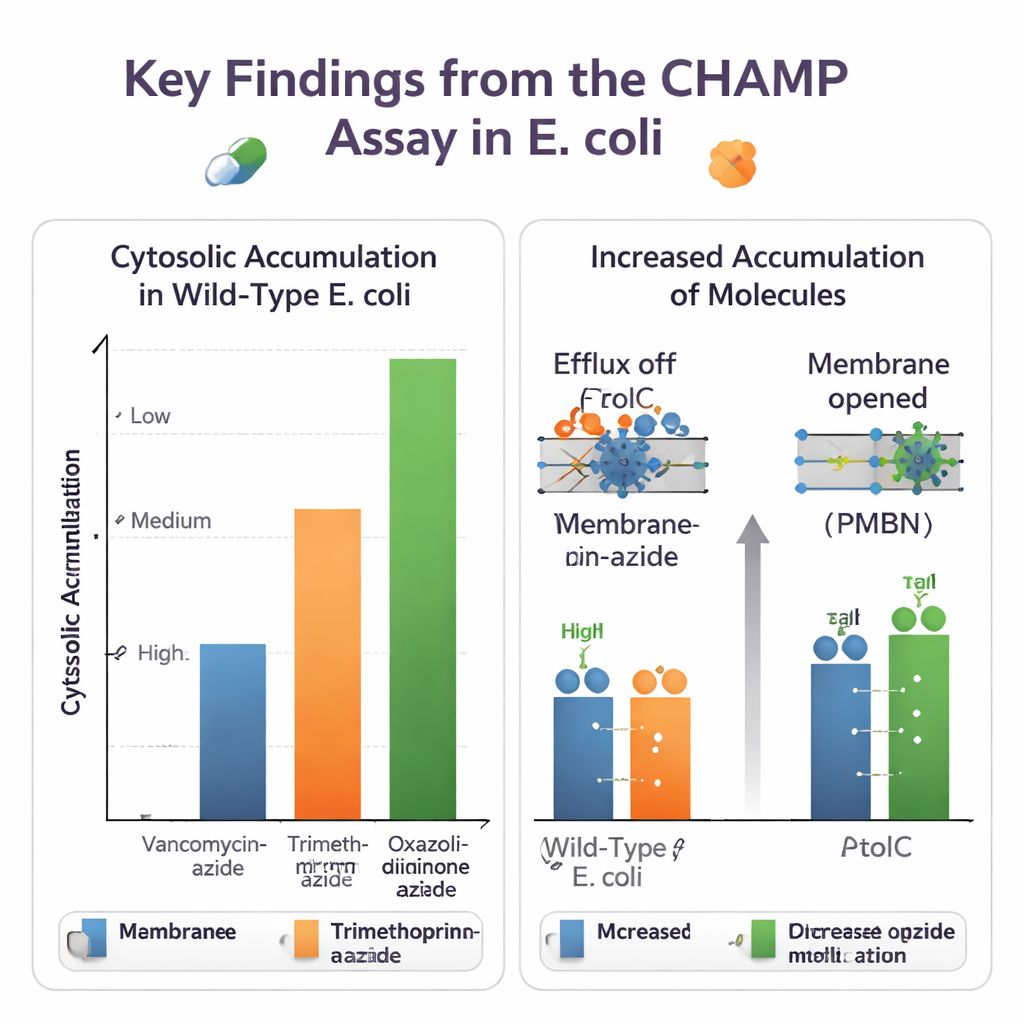
Utilizzando CHAMP, il gruppo ha prima ottimizzato l’espressione di HaloTag, la quantità di ancoraggio DBCO e la scelta dei coloranti fluorescenti per ottenere una finestra di segnale ampia e affidabile. Poi hanno usato insiemi di piccole molecole strettamente correlate per vedere come piccole modifiche chimiche influenzano l’ingresso. La conversione di acidi carbossilici in ammidi e l’aggiunta o rimozione di gruppi amminici basici possono cambiare sensibilmente i livelli citosolici. In molti casi le ammine primarie hanno aumentato l’accumulo, rispecchiando le regole “eNTRy” sviluppate indipendentemente da altri gruppi. Il saggio ha gestito anche versioni azido‑taggate di antibiotici reali, rivelando grandi differenze: farmaci ingombranti come la vancomicina raggiungevano a malapena il citosol, mentre antibiotici più piccoli come derivati del trimethoprim e alcuni oxazolidinoni penetravano molto più facilmente.
Smascherare le difese batteriche che espellono i farmaci
Poiché il metodo si esegue in batteri vivi e geneticamente programmabili, può districare i ruoli delle diverse difese cellulari. Gli autori hanno confrontato E. coli normale con ceppi privi di TolC, un componente chiave di una grande pompa di efflusso multidroghe, o con cellule trattate con un inibitore di TolC di piccole dimensioni. Per novobiocina e diversi altri antibiotici azido‑taggati, CHAMP ha mostrato chiaramente un maggiore accumulo citosolico quando TolC era disabilitato, confermando che questi composti sono substrati dell’efflusso. Hanno anche testato modi per allentare la barriera della membrana esterna, chimicamente con il peptide PMBN o geneticamente sovraesprimendo un poro ampio aperto. Molte molecole che in precedenza si accumulavano poco hanno mostrato grandi aumenti quando la membrana è stata permeabilizzata, evidenziando come ingresso ed efflusso cooperino per determinare i livelli interni di farmaco.
Scalare fino a migliaia di molecole per individuare modelli e regole
Per dimostrare il vero alto rendimento, i ricercatori hanno schermato un set commerciale di 404 composti azido‑taggati e una libreria personalizzata di 1.152 molecole con gruppo azido. Hanno misurato l’accumulo in diversi contesti batterici, incluse cellule non trattate, cellule trattate con PMBN, cellule iperporinate e cellule iperporinate prive di TolC. Confrontando la stessa molecola attraverso queste condizioni, hanno potuto distinguere quali cambiamenti dipendevano dalla biologia cellulare piuttosto che da differenze nella velocità della reazione di click. Combinando i dati CHAMP con analisi computazionali, hanno collegato certe caratteristiche fisico‑chimiche — come area superficiale polare, capacità di formare legami a idrogeno e specifici impalcature ad anello — a una maggiore riconoscibilità da parte dell’efflusso mediato da TolC. Questo tipo di profilazione su larga scala inizia a delineare regole di progetto per molecole che o eludono le pompe o sfruttano meglio i pori.
Cosa significa per i futuri antibiotici
In termini semplici, questo lavoro trasforma E. coli in un sensore ad alto rendimento che riporta esattamente quanto di un composto di prova entra nella parte della cellula dove risiedono molti bersagli farmacologici. CHAMP non sostituisce i test che verificano se i batteri vengono uccisi, ma colma un vuoto cruciale separando il “riuscire a entrare” dall’“esercitare l’effetto”. Con la capacità di misurare oltre mille molecole in ceppi mutanti o chimicamente alterati in pochi giorni, i ricercatori possono ora imparare sistematicamente quali caratteristiche chimiche favoriscono l’ingresso, riducono l’efflusso o traggono vantaggio da partner che disturbano la membrana. Queste conoscenze dovrebbero accelerare la progettazione di nuovi antibiotici e di farmaci ausiliari in grado di oltrepassare le formidabili difese dei patogeni Gram‑negativi prima che la resistenza consumi altre parti dell’arsenale antibiotico.
Citazione: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
Parole chiave: resistenza agli antibiotici, Escherichia coli, permeabilità dei farmaci, pompe di efflusso, chimica click