Clear Sky Science · it
Microscopia a illuminazione strutturata cieca ad alta velocità tramite unrolling algoritmico non supervisionato
Filmati più nitidi della vita all'interno delle cellule
La biologia moderna dipende spesso dall'osservare cellule vive in azione, ma molte strutture chiave sono semplicemente troppo piccole e troppo rapide perché i microscopi ordinari le catturino con chiarezza. Questo articolo presenta un nuovo metodo per trasformare immagini sfocate e acquisite rapidamente in filmati nitidi e super-dettagliati in tempo reale, senza la necessità di hardware perfettamente tarato. Il metodo, chiamato unrolled blind structured illumination microscopy (UBSIM), promette di rendere l'imaging cellulare avanzato e ad alta velocità più accessibile ai laboratori biologici di uso quotidiano.
Perché i microscopi convenzionali non bastano
I microscopi ottici tradizionali sono limitati dalla diffrazione, una proprietà fondamentale della luce che sfoca i dettagli fini più piccoli di qualche centinaio di nanometri. La microscopia a illuminazione strutturata (SIM) affronta questo problema irradiando il campione con luce a pattern e sfruttando le interferenze risultanti per estrarre dettagli aggiuntivi, raddoppiando grosso modo la risoluzione. Tuttavia, la SIM classica richiede pattern di illuminazione conosciuti con precisione e una calibrazione accurata, che possono essere costosi e fragili. Una variante più recente, la blind‑SIM, allenta questi vincoli hardware consentendo pattern casuali e risolvendo simultaneamente il campione e l'illuminazione a partire dai dati stessi. Lo svantaggio è che questo processo di risoluzione è lento e iterativo, richiedendo secondi o minuti per fotogramma — troppo lento per filmati in tempo reale di cellule vive.
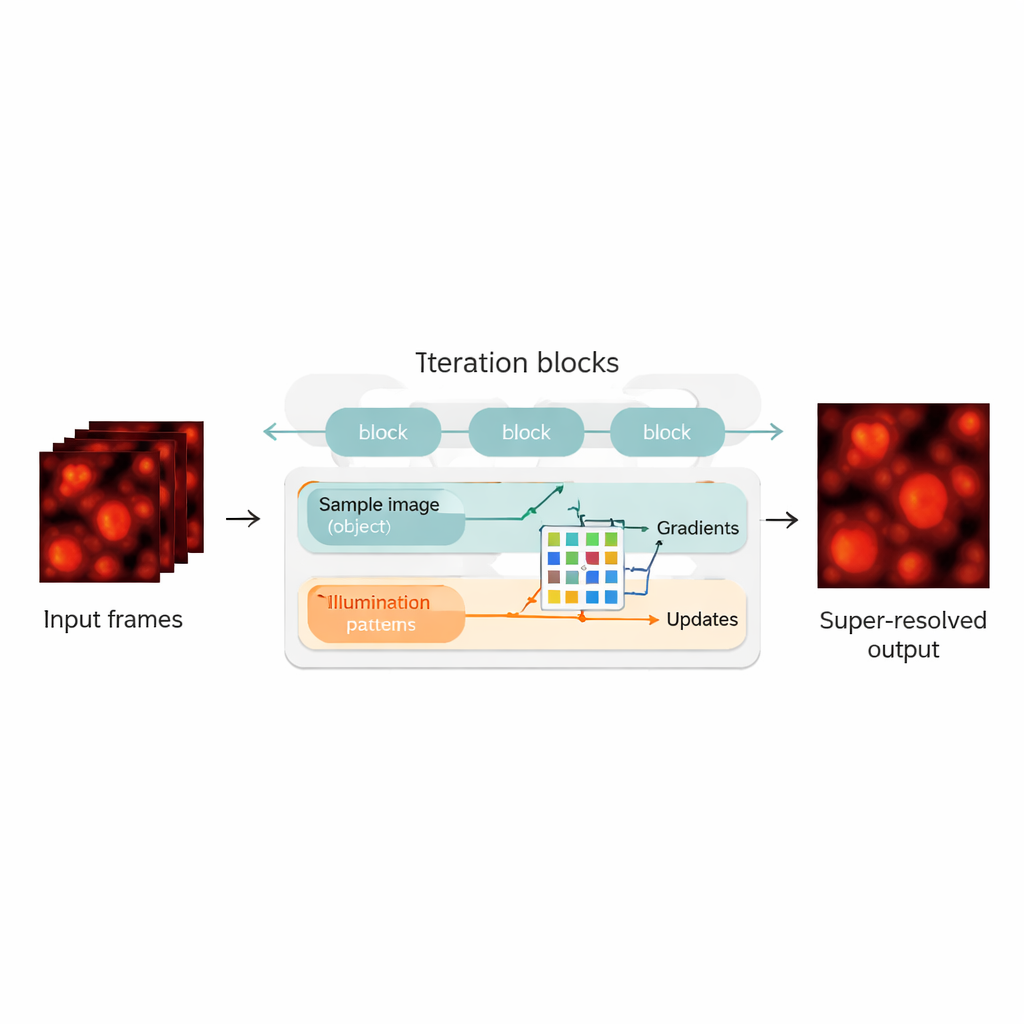
Fondere la fisica con le reti neurali
Gli autori colmano questo divario riprogettando la ricostruzione blind‑SIM come un ibrido tra un modello basato sulla fisica e una rete neurale. «Srotolano» l'algoritmo iterativo originale — ogni iterazione diventa uno strato in una rete neurale, formando una catena di blocchi di aggiornamento. All'interno di ciascun blocco, il metodo valuta quanto l'attuale ipotesi del campione e dell'illuminazione spieghi le immagini misurate, calcola gradienti (direzioni di miglioramento) e poi li fornisce a una compatta rete neurale convoluzionale. Questa rete impara come effettuare passi di correzione più intelligenti, svolgendo un ruolo simile a un acceleratore automaticamente ottimizzato per l'algoritmo originale. Crucialmente, UBSIM è addestrato in modo non supervisionato: invece di aver bisogno di immagini di esempio perfette come verità di riferimento, richiede solo il modello fisico di come la luce attraversa il microscopio. Ciò riduce il rischio che la rete «allucini» strutture dall'aspetto plausibile ma errate.
Veloce, accurato e meno soggetto a supposizioni
Per testare UBSIM, il team ha prima usato immagini microscopiche simulate in cui le strutture sottostanti sono note. Hanno mostrato che UBSIM recupera circa il doppio della risoluzione rispetto alle immagini widefield ordinarie, paragonabile alla blind‑SIM standard, ma funziona da due a tre ordini di grandezza più velocemente — un'immagine 256×256 può essere ricostruita in circa 10 millisecondi invece di secondi. Le misure di qualità dell'immagine, inclusi errore, similarità e rapporto segnale‑rumore, sono migliorate nettamente rispetto alle immagini convenzionali. UBSIM si è inoltre dimostrato più affidabile rispetto a popolari reti di deep learning per la super‑risoluzione quando è stato messo di fronte a dati non familiari. Mentre le reti standard addestrate su un tipo di struttura tendevano a imporre quel pattern su campioni nuovi e diversi — introducendo artefatti sottili ma fuorvianti — UBSIM manteneva una fedeltà coerente, perché è ancorato alla fisica dell'imaging piuttosto che solo a esempi visivi.
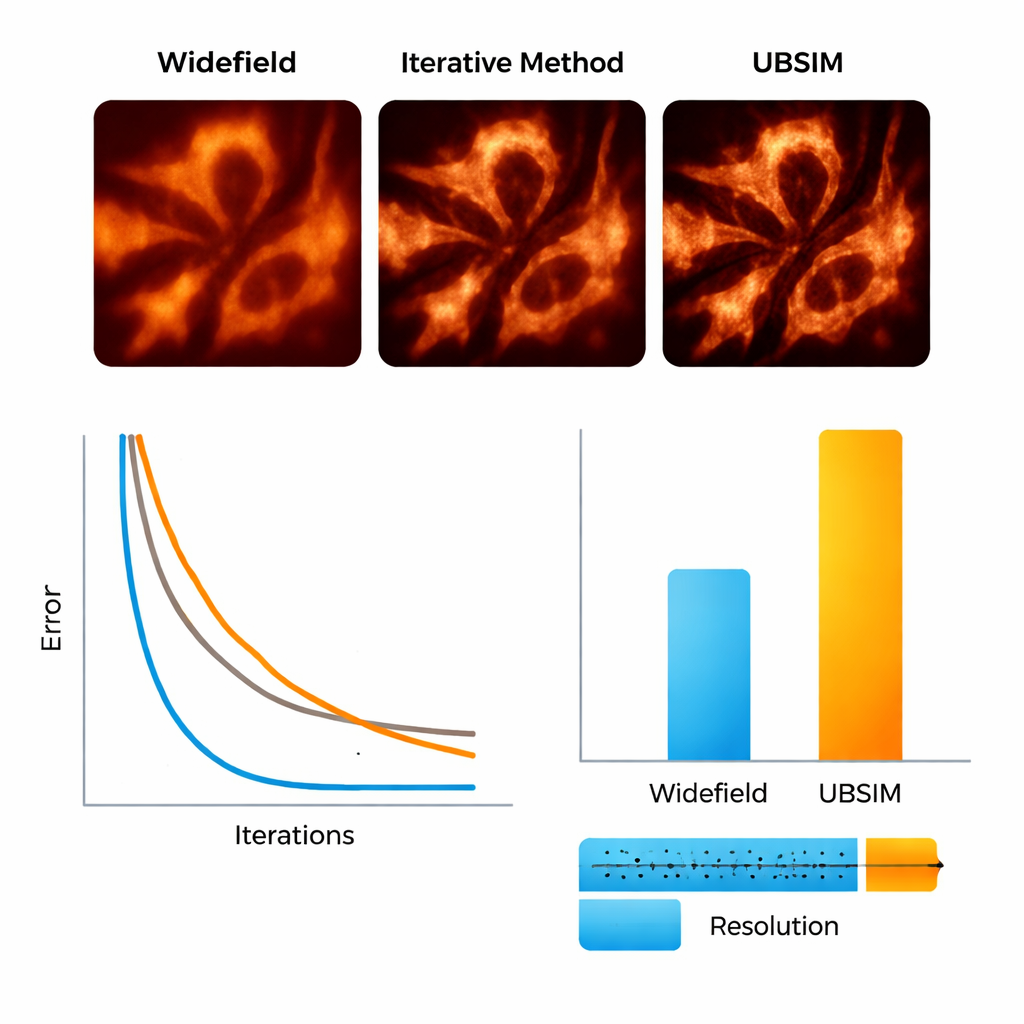
Vedere scheletri e membrane cellulari in movimento
I ricercatori sono poi passati a campioni biologici reali. Utilizzando un setup flessibile che proietta pattern di speckle casuali su cellule vive, hanno imagingato filamenti di actina — lo «scheletro» proteico all'interno delle cellule — e il reticolo endoplasmatico (RE), una rete lamellare ramificata coinvolta nella produzione proteica e nelle risposte allo stress cellulare. Con UBSIM, le fibre di actina che apparivano come bande sfocate nelle immagini ordinarie sono diventate filamenti nettamente separati, con una risoluzione che è migliorata da circa 300 nanometri a circa 150 nanometri. Ancora più notevole, UBSIM ha permesso super‑risoluzione a velocità video: acquisendo dati grezzi fino a 100 fotogrammi al secondo e ricostruendo fino a 50 fotogrammi super‑risolti al secondo, il team ha potuto osservare i tubuli del RE crescere, collassare e riorganizzarsi in tempo reale. Queste dinamiche, che avvengono in frazioni di secondo fino a pochi secondi, sono normalmente difficili da visualizzare con dettaglio sufficiente.
Cosa significa per il futuro dell'imaging cellulare
Per i non specialisti, il punto chiave è che UBSIM rende molto più pratico osservare strutture cellulari minute in movimento, in tempo reale, con chiarezza oltre i limiti normali dei microscopi ottici — il tutto senza richiedere calibrazioni hardware perfette o enormi set di dati di addestramento. Combinando l'affidabilità dei modelli basati sulla fisica con la velocità delle reti neurali moderne, questo approccio trasforma pile di immagini rumorose e patternate in filmati ultra‑nitidi e affidabili, abbastanza rapidi per esperimenti di routine. Man mano che il metodo verrà ulteriormente perfezionato e abbinato a strategie di illuminazione migliori, potrebbe aiutare i ricercatori a esplorare come gli organelli come il RE rispondono allo stress, come gli scheletri cellulari si riorganizzano durante il movimento o la divisione, e come le malattie alterano l'architettura cellulare a scala nanometrica.
Citazione: Burns, Z., Zhao, J., Sahan, A.Z. et al. High-speed blind structured illumination microscopy via unsupervised algorithm unrolling. Nat Commun 17, 1967 (2026). https://doi.org/10.1038/s41467-026-68693-w
Parole chiave: microscopia a super-risoluzione, illuminazione strutturata, deep learning, imaging di cellule vive, dinamiche del reticolo endoplasmatico