Clear Sky Science · it
Approfondimenti funzionali e strutturali sulle interazioni tra β-Arrestina 1 e Gαs o Gαi1
Perché questo conta per la salute e la medicina
Molti dei farmaci attuali, dagli antistaminici ai cardiologici e ai trattamenti psichiatrici, agiscono su una vasta famiglia di proteine di superficie cellulare chiamate recettori accoppiati a proteine G, o GPCR. Questi recettori trasmettono messaggi all’interno della cellula usando due aiutanti principali: le proteine G e le beta-arrestine. Questo studio esamina come una beta-arrestina (beta-arrestina 1) dialoghi direttamente con due tipi di proteine G all’interno della cellula. Comprendere questa conversazione nascosta potrebbe aiutare i ricercatori a progettare farmaci più precisi e con meno effetti collaterali, modulando con maggiore finezza il flusso di segnali nelle nostre cellule.
Due principali messaggeri all’interno delle nostre cellule
Quando un ormone o un farmaco si lega a un GPCR sulla superficie cellulare, si attivano due ampie vie di comunicazione. Una via utilizza le proteine G, che si accendono e si spengono come timer molecolari scambiando una piccola molecola (GDP) con un’altra (GTP). L’altra via coinvolge le beta-arrestine, che possono sia spegnere la segnalazione mediata dalle proteine G sia avviare percorsi di segnalazione propri. Per molto tempo gli scienziati hanno studiato principalmente come i recettori comunicano separatamente con le proteine G o con le beta-arrestine. lavori più recenti hanno suggerito che proteine G e beta-arrestine potrebbero anche legarsi tra loro o perfino formare grandi “mega-complessi” con il recettore. Ma i dettagli di come queste proteine si connettano e cosa ciò significhi per la segnalazione sono rimasti poco chiari.
Misurare chi si lega a chi
In questo studio i ricercatori si sono concentrati su beta-arrestina 1 e su due sottounità alfa delle proteine G: Gαs, che di solito stimola l’attività cellulare, e Gαi1, che generalmente la attenua. Utilizzando una tecnica sensibile per misurare il legame, hanno testato quanto fortemente la beta-arrestina 1 purificata e ciascuna proteina G si associano in diverse condizioni. Hanno scoperto che il fattore chiave non è se la proteina G sia “accesa” o “spenta”, ma se la beta-arrestina 1 si trovi in una forma più attiva e flessibile. Una versione di beta-arrestina 1 priva della coda — che si comporta come un insieme di conformazioni libere e attive — si legava con forza sia a Gαs sia a Gαi1. Al contrario, la forma a riposo di beta-arrestina 1, o una forma bloccata da un peptide simile alla coda del recettore, si legava debolmente o per nulla. Questo suggerisce che le proteine G riconoscano preferenzialmente la beta-arrestina 1 quando essa esplora forme simili a quelle attive che possono esistere dopo l’attivazione del recettore. 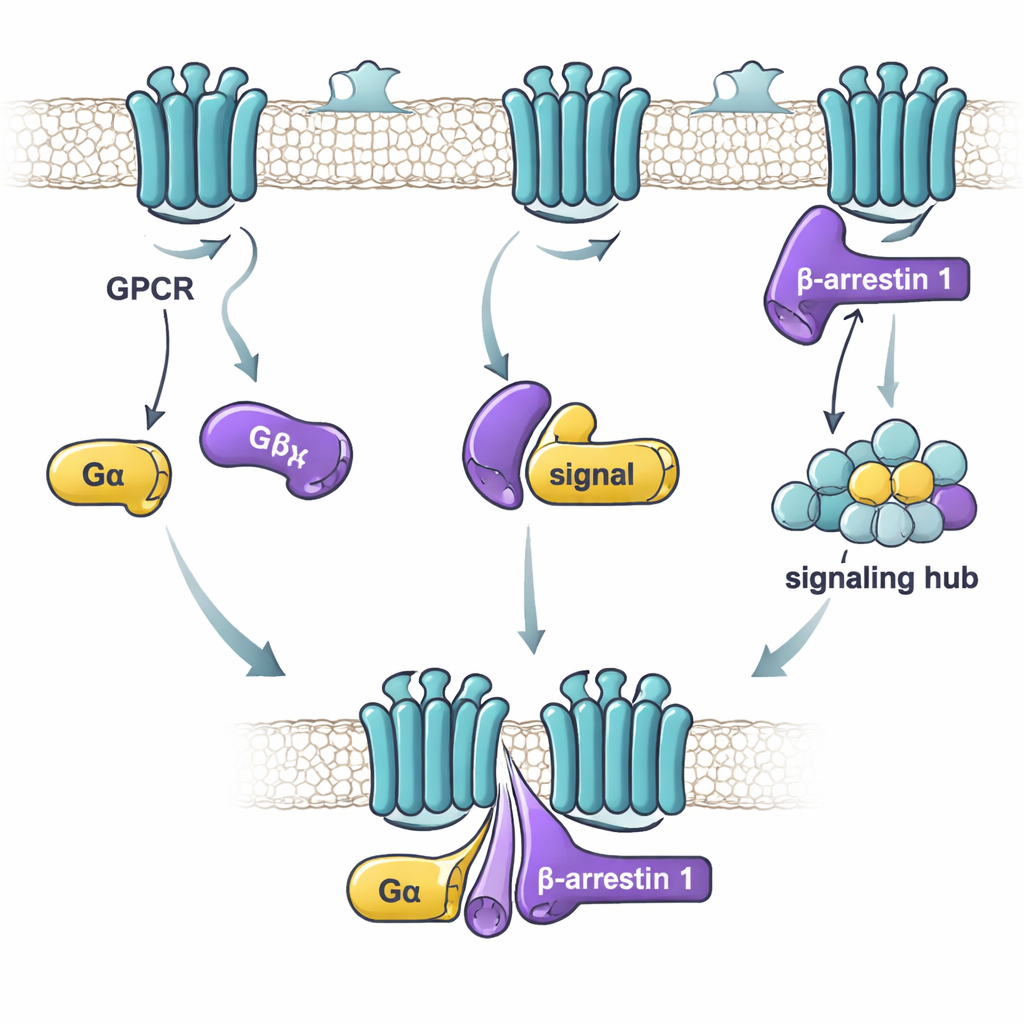
Osservare cambiamenti sottili di forma
Per vedere come il legame influenzi la conformazione delle proteine, il gruppo ha usato un metodo che monitora quanto rapidamente gli atomi di idrogeno sullo scheletro proteico si scambiano con l’idrogeno pesante dal solvente. Uno scambio più lento indica generalmente che una regione è diventata più protetta o rigida; uno scambio più veloce indica che è diventata più flessibile o esposta. Quando il frammento di beta-arrestina 1 in forma attiva si è legato a Gαs o Gαi1, entrambe le proteine G hanno mostrato chiari cambiamenti di pattern in diverse regioni, indicando che si rimodellavano attorno al complesso. Al contrario, la beta-arrestina 1 ha cambiato la propria struttura solo in misura lieve, principalmente in loop flessibili. Lavorando con domini isolati delle proteine G, i ricercatori hanno anche dimostrato che sia la porzione catalitica principale “simile a Ras” sia la porzione elicoidale alfa circostante contribuiscono al legame. Per Gαs, la regione elicoidale svolge un ruolo particolarmente rilevante; per Gαi1, entrambe le regioni contano in modo approssimativamente equivalente.
Funzione senza azionare l’interruttore principale
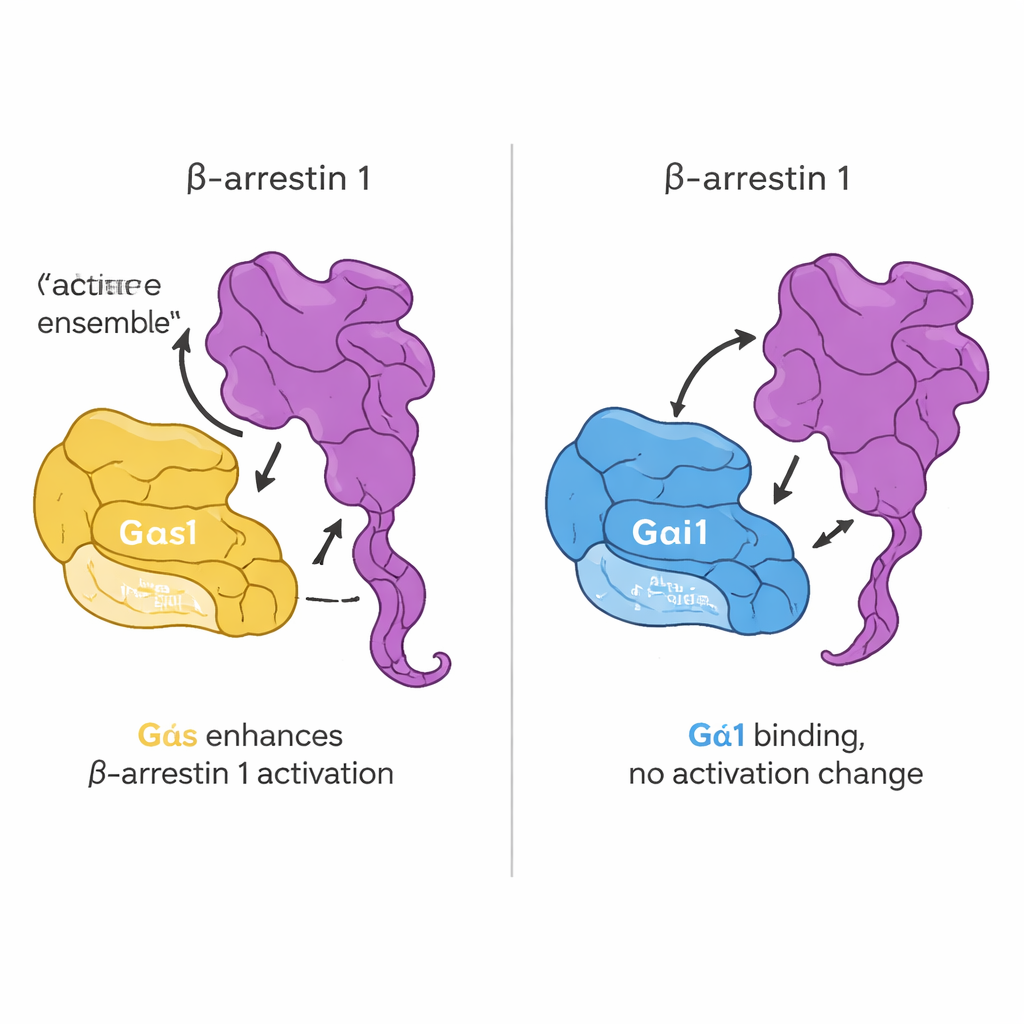
La domanda successiva era se questo contatto diretto altersse il modo in cui le proteine G si attivano. Il team ha usato una sonda fluorescente che imita il GTP e che si illumina quando una proteina G passa da GDP a GTP, una misura standard dell’attivazione. Sorprendentemente, l’aggiunta di beta-arrestina 1 non ha cambiato la velocità o l’entità di questo scambio nucleotidico né per Gαs né per Gαi1. In altre parole, la beta-arrestina 1 non agisce come una classica enzima “accendi” per le proteine G. Piuttosto, la sua influenza si manifesta sulla propria struttura. Usando una beta-arrestina 1 ingegnerizzata in modo che il movimento della coda potesse essere seguito mediante fluorescenza, hanno scoperto che Gαs attivo, ma non Gαi1, favorisce il distacco della coda C-terminale della beta-arrestina quando è presente un peptide derivato dal recettore. In cellule vive, ulteriori esperimenti di imaging e sensori di trasferimento di energia hanno confermato che Gαs e beta-arrestina 1 si avvicinano dopo la stimolazione ormonale e che Gαs contribuisce a spingere la beta-arrestina 1 verso una conformazione più attiva.
Un nuovo livello di controllo nella segnalazione cellulare
Mettendo insieme questi risultati, lo studio propone che Gαs e Gαi1 si leghino direttamente a beta-arrestina 1, ma in modi leggermente diversi e con conseguenze distinte. Nessuna delle due proteine G vede alterato il proprio comportamento principale di “on/off” a seguito di questo contatto. Piuttosto, soprattutto per Gαs, l’interazione agisce più come una manopola di regolazione fine sulla beta-arrestina 1, spingendola o stabilizzandola in una forma più attiva con coda rilasciata. Questo aggiunge uno strato finora poco apprezzato alla segnalazione mediata dai GPCR: non solo i recettori possono coordinare proteine G e beta-arrestine, ma proteine G e beta-arrestine possono anche modulare direttamente l’una l’altra. A lungo termine, mappare queste interazioni sottili potrebbe aiutare i progettisti di farmaci a indirizzare la segnalazione lungo percorsi vantaggiosi—potenziando vie utili ed evitando quelle che causano effetti collaterali.
Citazione: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
Parole chiave: Recettori accoppiati a proteine G, beta-arrestina, segnalazione delle proteine G, meccanismi di segnalazione cellulare, biologia strutturale