Clear Sky Science · it
Analisi sull’epigenoma identifica la metilazione del DNA come mediatore del rischio cardiometabolico correlato al trattamento in sopravvissuti al cancro infantile
Perché gli effetti collaterali del cancro persistono nell’organismo
Grazie a trattamenti migliori, la maggior parte dei bambini con cancro oggi raggiunge l’età adulta. Tuttavia molti di questi sopravvissuti affrontano nuovi problemi di salute a distanza di decenni, tra cui obesità, ipertensione e condizioni simili al diabete. Questo studio indaga una questione urgente: come fanno i trattamenti somministrati in età pediatrica a lasciare tali conseguenze a lungo termine sul cuore e sul metabolismo? Esaminando i marcatori chimici sul DNA nelle cellule del sangue, i ricercatori individuano indizi che chemioterapia e radioterapia passate possano “riprogrammare” l’organismo in modi che aumentano il rischio cardiometabolico nel lungo periodo.
Monitorare i rischi nascosti nei sopravvissuti adulti
Il gruppo ha studiato quasi 3.000 adulti sopravvissuti al cancro infantile e seguiti nella coorte a lungo termine St. Jude Lifetime Cohort. Questi sopravvissuti avevano ricevuto da bambini vari trattamenti chemioterapici e radioterapie alla testa o al tronco (torace, addome, pelvi) e si sono presentati anni dopo per controlli sanitari dettagliati e prelievi di sangue. Gli scienziati si sono concentrati su cinque problemi cardiometabolici chiave noti per aumentare il rischio di malattie cardiache e di morte prematura: obesità, alterazioni della glicemia, trigliceridi elevati, colesterolo alto e ipertensione. Confrontando i sopravvissuti con e senza queste condizioni, hanno cercato milioni di posizioni nel genoma in cui la metilazione del DNA—piccoli interruttori chimici che contribuiscono a regolare l’attivazione dei geni—presentava differenze.
I marcatori chimici sul DNA come memoria del trattamento
Nel genoma i ricercatori hanno trovato quasi 1.900 siti di DNA la cui metilazione era associata ad almeno una delle cinque condizioni cardiometaboliche. La maggior parte di questi siti era collegata a un singolo problema, ma un piccolo gruppo è emerso come “hub” connessi a più condizioni. Cinque siti chiave, collocati vicino a due geni denominati CPT1A e LMNA, risultavano associati simultaneamente a tutti e cinque i rischi cardiometabolici. Questi geni sono noti per influenzare il metabolismo dei grassi e la manutenzione della struttura cellulare, suggerendo che il trattamento possa disturbare vie metaboliche e cardiovascolari condivise. Molti dei cambiamenti di metilazione sovrapponevano segnali già osservati nella popolazione generale, in particolare quelli legati all’infiammazione, mentre altri sembravano esclusivi dei sopravvissuti al cancro—il che suggerisce che il trattamento lascia un’impronta biologica distintiva.
Collegare terapia, cambiamenti del DNA e malattia
Il passo successivo è stato verificare se questi cambiamenti di metilazione contribuissero effettivamente a spiegare il percorso dal trattamento alla malattia, e non fossero soltanto un marcatore accessorio. I ricercatori si sono concentrati su problemi cardiometabolici nuovi o in peggioramento insorti dopo il prelievo di sangue, preservando così la sequenza temporale dal trattamento al cambiamento del DNA fino alla malattia. Attraverso analisi statistiche di mediazione, hanno identificato 24 siti di metilazione che nel loro insieme spiegavano fino a circa un quarto del legame tra trattamenti specifici e successivi problemi cardiometabolici. La radioterapia alla testa e al tronco ha mostrato schemi particolarmente forti: gruppi di siti di metilazione insieme spiegavano grosso modo il 10–20% dell’impatto di queste radioterapie sulle alterazioni della glicemia. Un sito particolarmente significativo, vicino al gene ANTXR2, sembrava mediare circa il 20% dell’effetto della radioterapia al tronco sui successivi problemi glicemici.
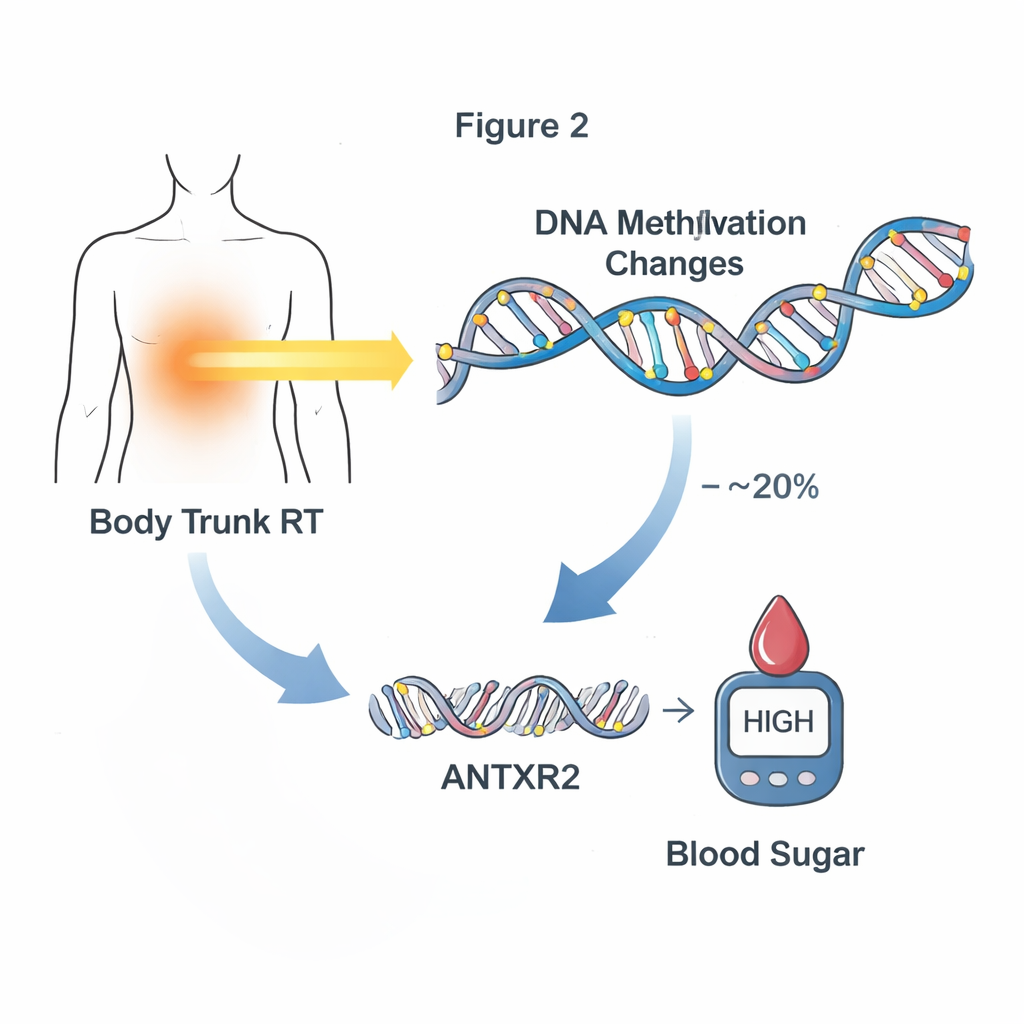
Dai segni sul DNA all’attività genica
Per capire come questi marchi di metilazione potessero alterare la biologia, il team ha esaminato l’espressione genica in un sottoinsieme di sopravvissuti per i quali erano disponibili sia dati sul DNA sia sull’RNA da sangue. Hanno trovato decine di siti di metilazione in cui un aumento o una diminuzione della metilazione era correlata a variazioni nell’espressione genica vicina. Tra questi c’era il sito mediatore chiave vicino a ANTXR2, dove i livelli di metilazione erano fortemente legati alla quantità di espressione di questo gene, specialmente nei sopravvissuti che avevano ricevuto radioterapia al tronco. ANTXR2 contribuisce a regolare i vasi sanguigni e l’impalcatura tissutale circostante—sistemi che influenzano come glucosio e insulina circolano nell’organismo. Questo schema suggerisce una catena di eventi in cui la radioterapia modifica la metilazione, che altera l’attività genica, e questo a sua volta può spostare l’equilibrio verso alterazioni della glicemia.
Cosa significa per i sopravvissuti e per le cure future
Per i non specialisti, il messaggio centrale è che i trattamenti per il cancro infantile non si limitano a danneggiare i tessuti nel momento in cui vengono somministrati; possono anche lasciare “appunti” duraturi sul DNA che influenzano la salute per decenni. In questo studio, alcuni di quegli appunti—cambiamenti nella metilazione del DNA—aiutano a spiegare perché alcuni sopravvissuti sono più a rischio di sviluppare obesità, livelli elevati di grassi nel sangue o problemi glicemici collegati a diabete e malattie cardiache. Pur rappresentando solo una parte della storia, questi marcatori chimici potrebbero in futuro fungere da biomarcatori nel sangue per identificare i sopravvissuti a più alto rischio e per testare se cambiamenti nello stile di vita o nuove terapie possano riscrivere in sicurezza parte di questa storia epigenetica. Il lavoro avvicina la medicina della survivorship a un approccio di precisione: usare le impronte molecolari del trattamento passato per guidare una prevenzione più precoce e personalizzata delle malattie cardiache e metaboliche.
Citazione: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
Parole chiave: sopravvissuti al cancro infantile, metilazione del DNA, rischio cardiometabolico, radioterapia, epigenetica