Clear Sky Science · it
Determinazione cotraduttiva delle strutture quaternarie nelle «fabbriche» di chaperoni
Come le “linee di montaggio” cellulari tengono in forma le grandi macchine
All’interno di ciascuna cellula migliaia di parti proteiche devono combinarsi per formare complesse macchine molecolari, dagli enzimi che copiano il DNA alle «fabbriche» che costruiscono altri RNA. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: come decidono le cellule, in tempo reale, quali proteine aiutanti accompagneranno ogni nuova parte mentre viene sintetizzata e come mantengono questo processo organizzato nel caos del citoplasma?
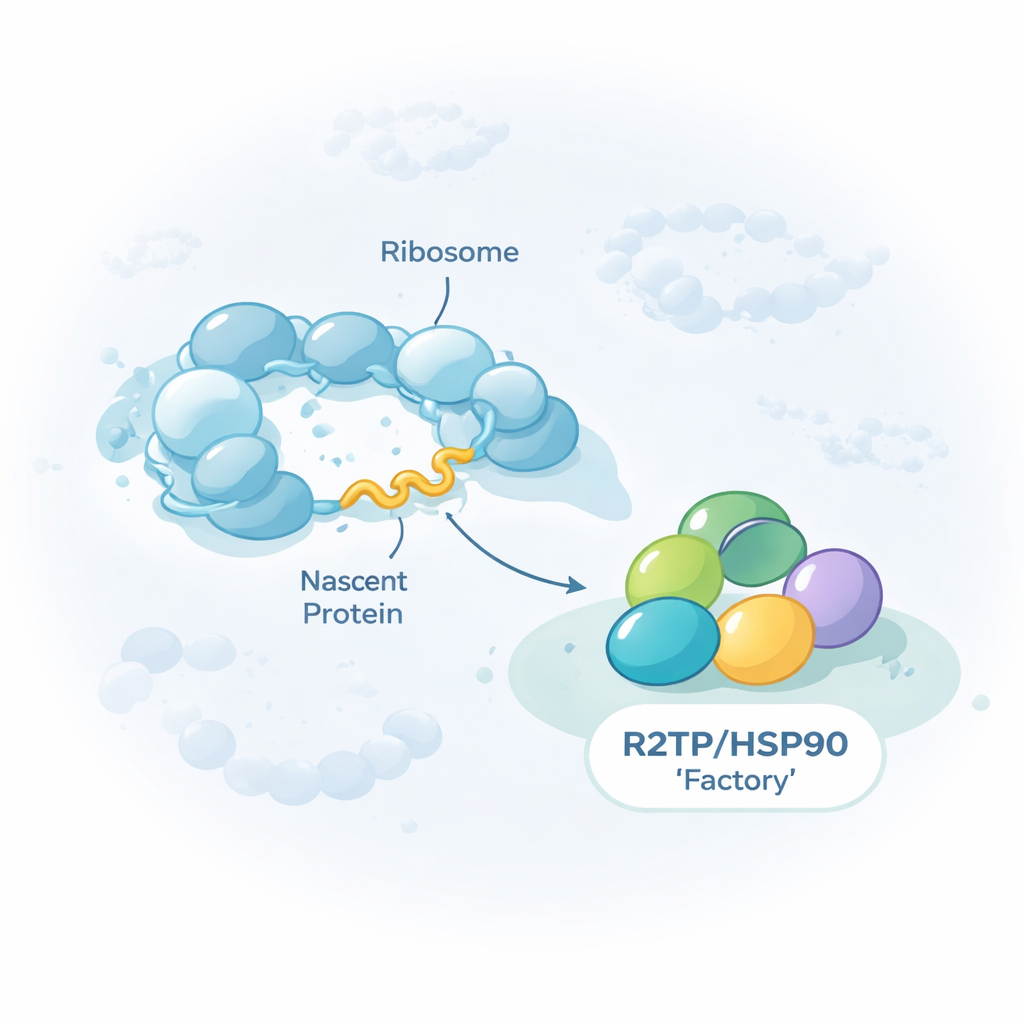
Un aiuto generale per le mega-macchine cellulari
Il lavoro si concentra su un gruppo di proteine aiutanti, o chaperoni, note come HSP90/R2TP. Piuttosto che occupare il loro ruolo solo nel ripiegamento di singole proteine, questo chaperone è specializzato nell’assemblaggio di grandi complessi multiproteici, incluse le tre RNA polimerasi nucleari che trascrivono il DNA in RNA, certi complessi ribonucleoproteici e grandi macchine di rimodellamento della cromatina. Gli autori mostrano che R2TP non incontra questi clienti solo una volta completati. Spesso si attacca mentre ciascun cliente è ancora in fase di sintesi sui ribosomi, le macchine che producono proteine nella cellula. Tirando giù R2TP da cellule umane e sequenziando gli RNA associati, hanno trovato circa 150 mRNA i cui prodotti proteici sono contattati da R2TP durante la loro traduzione.
Aiutanti che accompagnano le catene proteiche in crescita
Per verificare se questo legame avviene effettivamente durante la sintesi proteica, il gruppo ha usato farmaci che bloccano o perturbano la traduzione. Quando hanno impiegato composti che staccano le catene proteiche nascenti dai ribosomi, la maggior parte degli mRNA è scomparsa dall’associazione con R2TP. Ma quando hanno usato un farmaco che semplicemente mette in pausa i ribosomi lasciando le catene nascenti attaccate, il legame con R2TP è aumentato. RNA reporter ingegnerizzati hanno confermato questo risultato: se la traduzione veniva arrestata artificialmente in anticipo, il chaperone non legava più il messaggio. Nel complesso, questi risultati indicano una chiara regola d’ingaggio: R2TP riconosce i suoi clienti principalmente attraverso la catena proteica emergente che fuoriesce dal ribosoma, più che tramite la sequenza dell’RNA.
“Fabbriche” costruite dai chaperoni che raggruppano messaggi specifici
Utilizzando avanzate tecniche di imaging a singola molecola, gli autori hanno quindi fatto una scoperta sorprendente. Invece di osservare molti messaggi diversi dispersi casualmente, hanno visto che alcuni messaggi chiave—soprattutto quelli che codificano sottounità principali della RNA polimerasi II e un grande fattore di splicing chiamato PRPF8—spesso si raggruppavano in focolai luminosi nel citoplasma. Questi focolai erano arricchiti in R2TP e nel suo partner HSP90, così come in componenti ribosomiali e nelle stesse proteine in corso di sintesi, dimostrando che sono siti di traduzione attivi. Quando la traduzione o l’attività ATPasica, energivora, di R2TP o HSP90 venivano bloccate, questi focolai si dissolvevano. Gli autori chiamano queste strutture «fabbriche R2TP»: condensati specializzati dove particolari mRNA e chaperoni sono concentrati per favorire un contatto tempestivo e protettivo tra le catene proteiche emergenti e i loro assistenti d’assemblaggio.
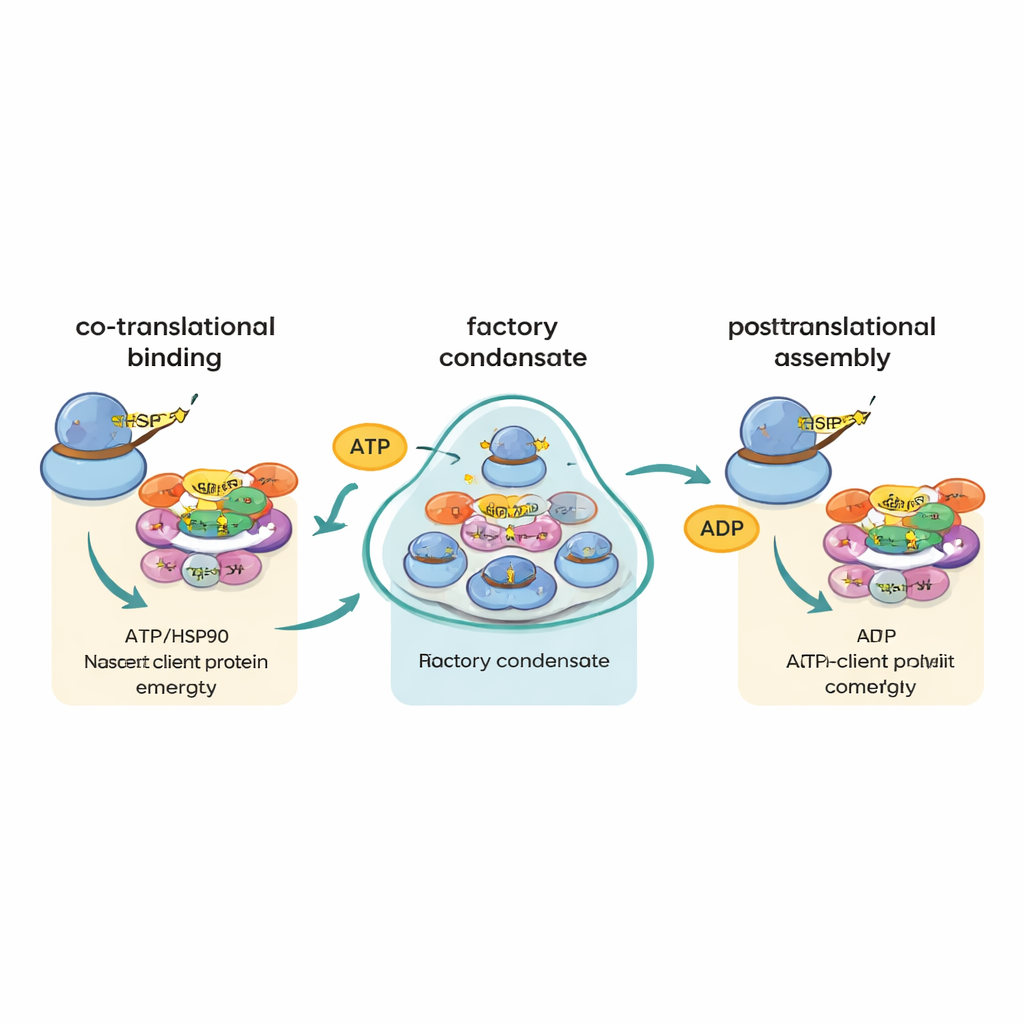
Instradare le parti senza far combaciare i loro progetti
Un’idea precedente sosteneva che messaggi che codificano parti diverse dello stesso complesso potessero incontrarsi e venire tradotti fianco a fianco, consentendo ai loro prodotti proteici di assemblarsi immediatamente. Il nuovo lavoro esclude in larga misura questo modello della «blueprint co-localizzata». Anche per coppie di proteine note per unirsi nello stesso complesso, i rispettivi mRNA raramente comparivano insieme. I dati supportano invece una strategia diversa che gli autori definiscono «canalizzazione cotraduttiva dei chaperoni», o «cha-cha». In questo schema, quando ciascuna proteina grande o incline all’assemblaggio inizia a emergere dal ribosoma, R2TP e HSP90 si attaccano e ne determinano il destino, guidandola attraverso i passi successivi dell’assemblaggio. Le fabbriche stesse non agiscono principalmente portando insieme messaggi corrispondenti; piuttosto, aumentano la probabilità che proteine appena sintetizzate e vulnerabili incontrino rapidamente il chaperone giusto.
Perché questa organizzazione nascosta conta per salute e malattia
Rivelando che R2TP e HSP90 non solo proteggono parti proteiche fragili ma influenzano anche dove e come vengono tradotte, questo studio mette in luce un livello inaspettato di organizzazione intracellulare. Il meccanismo cha-cha aiuta a spiegare come le cellule costruiscano in modo affidabile complessi molecolari enormi, pur quando i messaggi per le loro parti raramente condividono lo stesso indirizzo. Suggerisce inoltre perché difetti nei chaperoni o nei loro cicli energetici possano destabilizzare macchine vitali come le RNA polimerasi e i fattori di splicing, con conseguenze che vanno da disturbi dello sviluppo al cancro. In sostanza, il lavoro mostra che le cellule fanno affidamento su «fabbriche» di chaperoni dinamiche per instradare le parti appena fatte verso gli assemblaggi corretti, mantenendo la loro macchina interna efficiente e ordinata.
Citazione: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
Parole chiave: chaperoni proteici, assemblaggio cotraduttivo, macchine molecolari, RNA polimerasi, controllo qualità cellulare