Clear Sky Science · it
ProteoAutoNet: analisi ad alto rendimento delle proteine co-eluite con robotica e apprendimento automatico
Perché è importante comprendere le collaborazioni tra proteine
All’interno di ogni cellula, le proteine raramente agiscono da sole. Si associano in alleanze dinamiche per costruire strutture, copiare il DNA, eliminare parti danneggiate e sostenere la crescita. Molti tumori sfruttano queste collaborazioni, ma mappare i dettagli è stato finora un lavoro lento e meticoloso. Questo studio presenta ProteoAutoNet, un sistema potenziato da robotica e apprendimento automatico che accelera notevolmente il processo di scoperta delle collaborazioni proteiche nelle cellule, e mostra come questo approccio possa rivelare punti deboli nascosti nei carcinomi tiroidei.
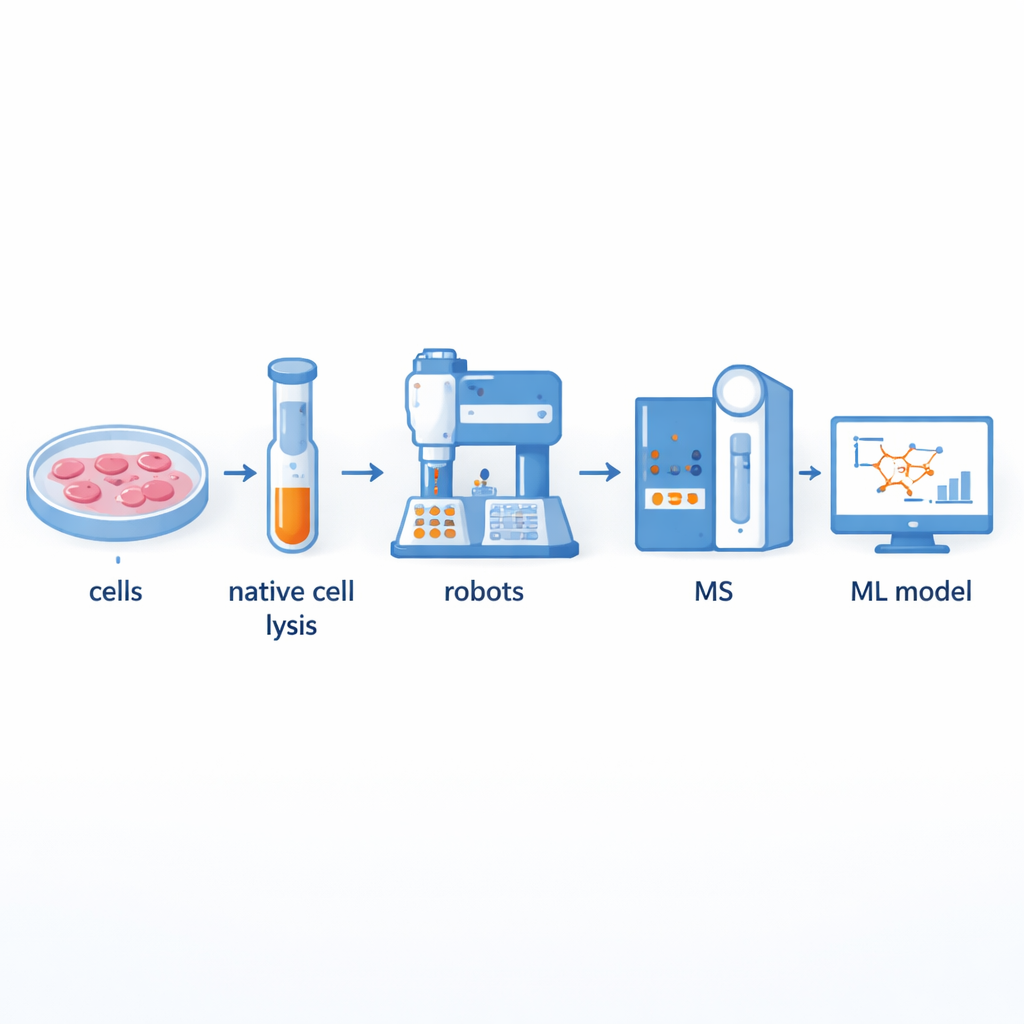
Costruire una linea di produzione più rapida per le partnership proteiche
Tradizionalmente, gli scienziati usano un metodo chiamato spettrometria di massa con co-frazionamento per separare grandi complessi proteici e identificarne i componenti. Pur essendo potente, questo approccio è laborioso e a basso rendimento: preparare manualmente centinaia di frazioni può richiedere molti giorni. Gli autori hanno sviluppato una piattaforma assistita da robot che automatizza gran parte del flusso di lavoro. Il contenuto cellulare viene prima liscato delicatamente per mantenere intatti i complessi proteici naturali, quindi passato attraverso colonne che separano in base alle dimensioni dividendolo in dozzine di frazioni. Robot per la manipolazione dei liquidi e bracci robotici subentrano poi per aggiungere reagenti, digerire le proteine in pezzi più piccoli, purificare i campioni e consegnarli allo spettrometro di massa per la misura. Questa configurazione può elaborare fino a 540 frazioni provenienti da più linee cellulari tiroidee in soli due o tre giorni, raddoppiando circa il rendimento rispetto ai sistemi precedenti semi-automatizzati.
Robot non solo più veloci, ma anche più affidabili
La velocità da sola non basta se i risultati sono rumorosi o incoerenti. Il team ha verificato accuratamente se la pipeline robotica corrispondeva o superasse la qualità del processamento manuale tradizionale. Usando campioni di controllo qualità, hanno dimostrato che il sistema automatizzato identificava ripetutamente quasi 3.000 proteine per linea cellulare tiroidea con un’elevata sovrapposizione tra repliche e forte concordanza nelle quantità rilevate. Nel confronto diretto tra processamento robotico e manuale degli stessi campioni, entrambi gli approcci hanno rilevato numeri simili di proteine, ma il metodo robotico ha mostrato una variazione leggermente inferiore nei conteggi e misure di abbondanza proteica più stabili. Ciò significa che la nuova piattaforma non solo riduce tempo e lavoro, ma supporta esperimenti più riproducibili — un requisito cruciale per studi su larga scala e applicazioni cliniche.
Insegnare ai computer a riconoscere connessioni significative
Anche con strumenti veloci, rimane una sfida centrale: decidere quali proteine interagiscono realmente e quali si ritrovano insieme per caso. Per affrontare questo problema, gli autori hanno combinato banche dati curate di complessi proteici con un modello di apprendimento automatico basato sull’algoritmo XGBoost. Hanno prima pulito e fuso tre risorse principali sui complessi proteici, ottenendo 96.635 interazioni proteina–proteina note. Hanno poi usato i profili di presenza delle proteine attraverso le frazioni come caratteristiche di input, e etichettato le coppie come partner probabili o non partner in base alle banche dati. Poiché le interazioni vere ad alta affidabilità sono relativamente rare, hanno adottato una strategia mirata di aumento dei dati: hanno creato molte versioni leggermente perturbate di esempi positivi noti per insegnare al modello a riconoscere pattern robusti piuttosto che memorizzare tracce specifiche. Allenato su decine di milioni di esempi di questo tipo provenienti da tre linee cellulari tiroidee, il modello ha raggiunto ottime prestazioni, classificando le interazioni vere ben al di sopra del caso sia nei test interni sia in una linea cellulare di validazione indipendente.
Nuove prospettive sulla macchina cellulare del cancro
Con questo flusso di lavoro, i ricercatori hanno mappato le reti di interazione in una linea cellulare tiroidea normale e in due linee tumorali: una di carcinoma papillare e una di carcinoma follicolare metastatico ai polmoni. In queste cellule hanno identificato oltre 25.000 probabili interazioni proteiche e rilevato segnali netti da macchine cellulari ben note come i ribosomi (che assemblano le proteine) e i proteasomi (che le degradano), confermando che il metodo recupera biologia consolidata. Confrontando i tumori con la linea normale, hanno individuato reti potenziate nella malattia. Nelle cellule di carcinoma follicolare metastatico, sia i componenti del proteasoma sia un complesso chaperone chiamato prefoldina risultavano decisamente più connessi e abbondanti. Alcune subunità della prefoldina erano già state associate ad altri tumori, ma i sondaggi proteici globali avevano perso il loro comportamento coordinato nel carcinoma tiroideo, forse perché queste proteine sono strettamente regolate tramite degradazione. L’approccio di co-frazionamento ha messo in luce i loro cambiamenti coordinati a livello di complesso.
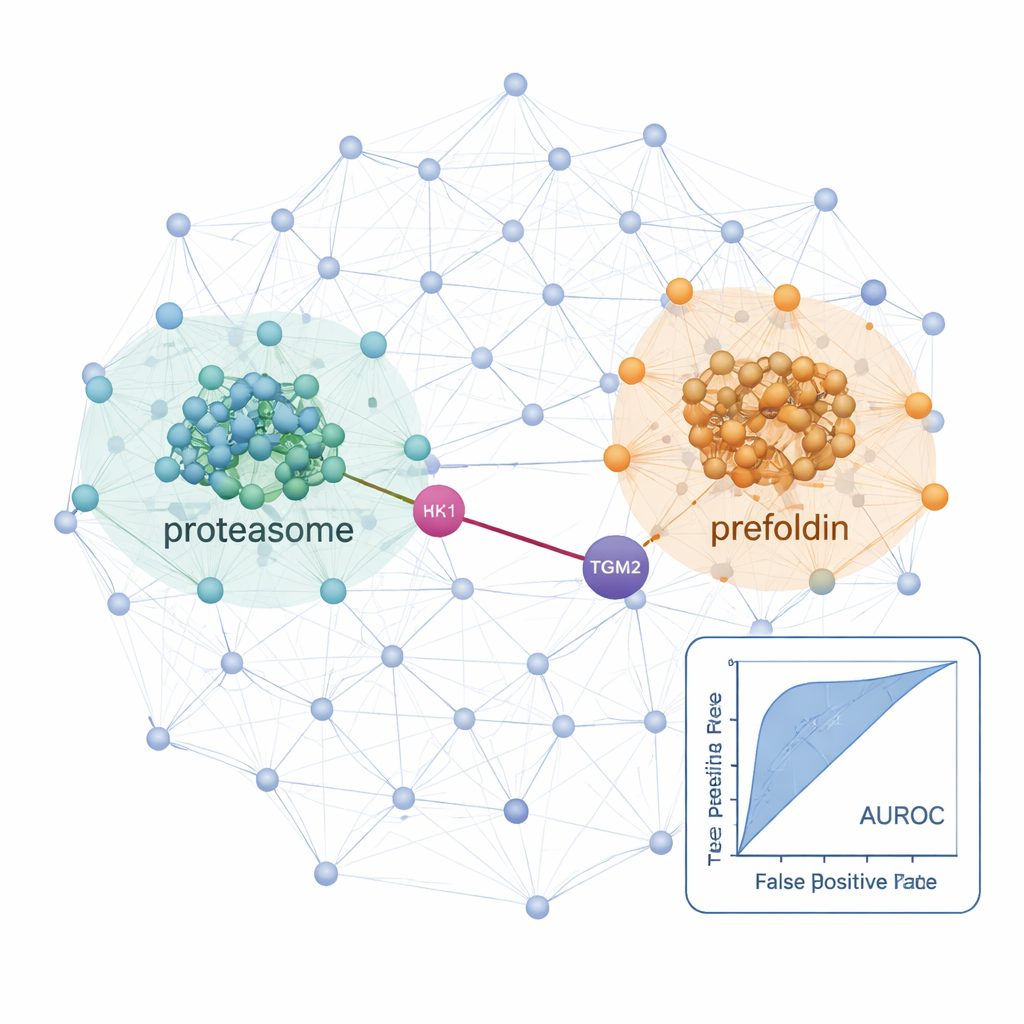
Legami nascosti che potrebbero indirizzare futuri trattamenti
Lo studio ha anche evidenziato interazioni specifiche che potrebbero essere rilevanti per la crescita e la diffusione dei tumori tiroidei. Un esempio è una partnership predetta tra HK1, un enzima che avvia il principale percorso di combustione dello zucchero della cellula, e TGM2, una proteina nota per favorire invasione e metastasi nei tumori tiroidei. Questa connessione HK1–TGM2, assente dalle banche dati di interazione esistenti, è stata supportata da modellizzazione strutturale ed era particolarmente attiva nella linea di carcinoma papillare, suggerendo che la riorganizzazione metabolica e il comportamento invasivo possano essere collegati fisicamente. In sintesi, ProteoAutoNet dimostra come la combinazione di robotica e apprendimento automatico possa trasformare la mappatura delle reti proteiche da un compito lento riservato agli esperti in un processo più scalabile. Per i non specialisti, il messaggio chiave è che questa tecnologia può scoprire sia ampi spostamenti nella macchina cellulare sia partnership proteiche inattese che un giorno potrebbero aiutare i medici a prevedere meglio quali carcinomi tiroidei si comporteranno in modo aggressivo e suggerire nuovi bersagli terapeutici.
Citazione: Lyu, M., Hu, P., Zhang, G. et al. ProteoAutoNet: high-throughput co-eluted protein analysis with robotics and machine learning. Nat Commun 17, 1949 (2026). https://doi.org/10.1038/s41467-026-68686-9
Parole chiave: interazioni proteiche, spettrometria di massa, apprendimento automatico in biologia, carcinoma tiroideo, proteasoma e prefoldina