Clear Sky Science · it
Disgregazione differenziale dei lipidi di membrana da parte di lipopeptidi antibiotici: colistina e turnerciclamicine
Perché questo conta per gli antibiotici del futuro
Le infezioni resistenti ai farmaci sono destinate a causare decine di milioni di morti ogni anno entro la metà del secolo, e alcuni dei responsabili più letali sono batteri Gram-negativi che già ignorano molti antibiotici. La colistina è uno dei pochi farmaci rimasti in grado di trattare queste infezioni, ma ha effetti collaterali pesanti sui pazienti e i batteri stanno sempre più imparando a eluderla. Questo studio analizza come agisce la colistina rispetto a una nuova famiglia di antibiotici naturali chiamati turnerciclamicine, rivelando che piccole modifiche chimiche possono generare modi molto diversi di uccidere i batteri — e potenzialmente farmaci più sicuri.
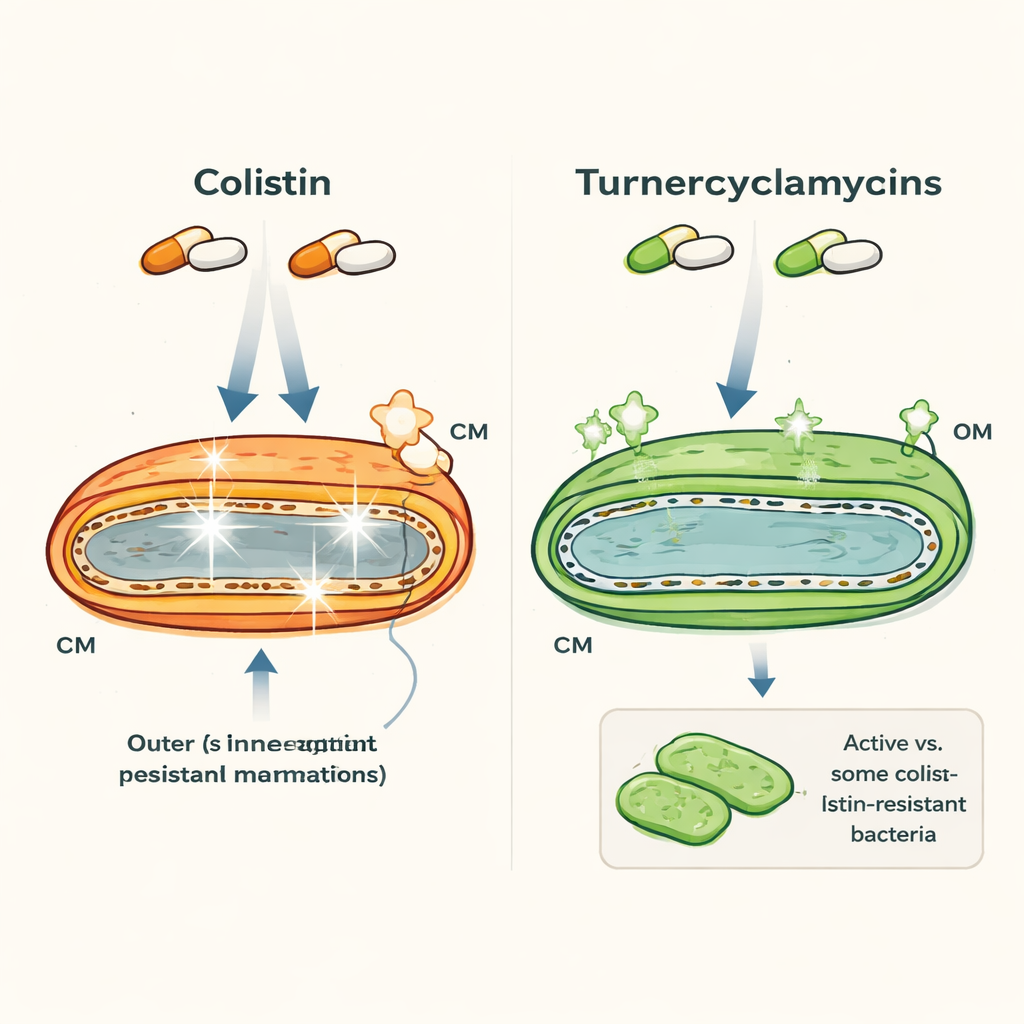
Due farmaci dall’aspetto simile ma con comportamenti molto diversi
Colistina e turnerciclamicine sono entrambe lipopeptidi — molecole che combinano una coda grassa con un anello peptidico — e entrambe sono dirette contro batteri Gram-negativi come Escherichia coli e Acinetobacter. A prima vista sembrano simili, eppure le loro proprietà divergono nettamente. La colistina è un farmaco di ultima istanza che agisce rapidamente ma può danneggiare reni e nervi umani, e i batteri portano sempre più spesso geni di resistenza come mcr-1. Le turnerciclamicine, scoperte in batteri associati ai teredini (shipworm), possono uccidere molti degli stessi patogeni, incluse alcune ceppi resistenti alla colistina, ma mostrano molta meno tossicità nei test di laboratorio. È interessante che due versioni che differiscono solo per una piccola estensione della coda grassa mostrino già pattern di resistenza diversi, suggerendo che caratteristiche strutturali molto sottili sono rilevanti.
Come la colistina apre buchi e le turnerciclamicine agiscono con più calma
Gli autori hanno usato coloranti fluorescenti, esperimenti di uccisione nel tempo e microscopia elettronica per osservare come questi farmaci influenzano le membrane batteriche nel tempo. La colistina rende rapidamente permeabili sia la membrana esterna sia la membrana citoplasmatica interna, portando a una morte cellulare veloce entro poche ore. Le turnerciclamicine, al contrario, uccidono più lentamente — impiegando 6-10 ore per eliminare completamente le colture — e disturbano principalmente la membrana esterna. I coloranti che si illuminano quando la membrana interna viene violata hanno dato segnali forti per la colistina ma solo segnali modesti e ritardati per le turnerciclamicine, e immagini ad alta risoluzione hanno confermato pochi danni visibili alla membrana interna anche quando le cellule stavano morendo. Questo indica che le turnerciclamicine non uccidono tramite la classica via di formazione di pori usata da molti antibiotici che mirano alle membrane.
I mattoni lipidici come manopole di controllo nascoste
Entrambe le famiglie di farmaci dipendono in ultima analisi da un componente batterico chiamato lipopolisaccaride (LPS), che viene costruito nella membrana interna e di solito esportato sulla superficie esterna. Quando i ricercatori hanno disattivato le prime fasi della biosintesi del LPS, sia la colistina sia le turnerciclamicine hanno perso attività; ma quando hanno bloccato la macchina di trasporto che sposta l’LPS verso l’esterno, i farmaci hanno continuato a funzionare. Ciò significa che l’esistenza dei precursori dell’LPS è essenziale, ma la loro destinazione finale non lo è. È emersa una differenza chiave quando il legame è stato misurato direttamente: la colistina si lega all’LPS purificato con forza micromolare, mentre le turnerciclamicine non hanno mostrato un legame misurabile. Invece, le turnerciclamicine risultavano fortemente influenzate da altri lipidi di membrana. Alcuni fosfolipidi, in particolare la fosfatidilglicerolo, potevano attenuare o modulare la loro attività, e i farmaci venivano facilmente catturati da vescicole della membrana esterna — piccole bolle lipidiche rilasciate dai batteri.
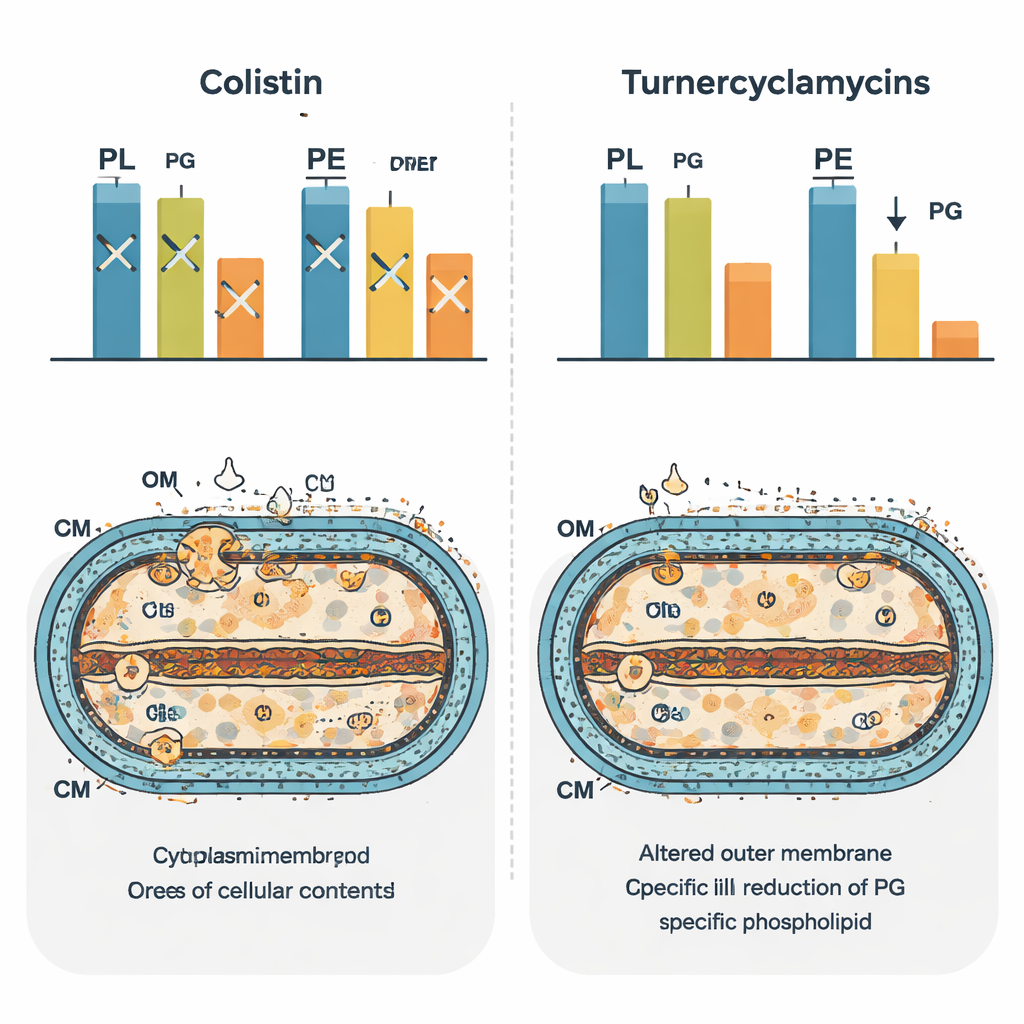
Riprogrammare il panorama lipidico batterico
Per vedere l’impatto più ampio sulla cellula, il gruppo ha utilizzato una “fosfolipidomica” basata su spettrometria di massa per catalogare centinaia di specie lipidiche dopo il trattamento. La colistina ha prodotto un modello distintivo di cambiamenti, riflettendo la sua ampia perturbazione dell’omeostasi delle membrane. Le turnerciclamicine hanno generato una firma diversa che somigliava molto a quella di batteri privi di una proteina trasportatrice di lipidi chiamata MlaA. In queste cellule, alcuni lipidi diacilici risultavano impoveriti e le forme monoaciliche aumentate, suggerendo che il normale ciclo e rimodellamento dei fosfolipidi tra le membrane era stato alterato. In particolare, i livelli di fosfatidilglicerolo sono diminuiti nelle cellule trattate con turnerciclamicine, rafforzando l’idea che questo lipide sia direttamente legato alla loro potenza. Gli autori propongono che le turnerciclamicine possano agire come imitatori molecolari che bloccano i percorsi che collegano la sintesi o il trasporto degli acidi grassi, dell’LPS e della fosfatidilglicerolo.
Cosa significa per progettare farmaci migliori
In termini semplici, lo studio mostra che la colistina uccide strappando rapidamente entrambe le barriere protettive di un batterio Gram-negativo, favorita da un forte legame con l’LPS, mentre le turnerciclamicine agiscono più come sabotatori della catena di approvvigionamento lipidico della cellula. Si inseriscono nella membrana esterna, disturbano gradualmente come vengono prodotti e riciclati specifici lipidi e alla fine fanno cedere l’involucro cellulare — senza danneggiare pesantemente la membrana interna. Poiché questo meccanismo più delicato e mirato è legato a minore tossicità e a un profilo di resistenza diverso, comprenderlo offre una mappa per progettare lipopeptidi di nuova generazione. Modificando con cura caratteristiche come la lunghezza e il grado di saturazione della coda grassa, i chimici potrebbero riuscire a costruire farmaci che risparmiano i tessuti umani, conservano attività contro ceppi resistenti alla colistina e restano un passo avanti nella corsa agli armamenti contro i batteri resistenti agli antibiotici.
Citazione: Lim, A.L., Miller, B.W., Fisher, M.A. et al. Differential membrane lipid disruption by lipopeptide antibiotics, colistin and turnercyclamycins. Nat Commun 17, 1880 (2026). https://doi.org/10.1038/s41467-026-68681-0
Parole chiave: resistenza agli antibiotici, batteri Gram-negativi, colistina, antibiotici lipopeptidici, lipidi di membrana