Clear Sky Science · it
Base strutturale delle conformazioni dinamiche di AP-4 e della sua associazione con ARF1
Come le cellule smistano e spediscono il loro carico
Ogni cellula è un magazzino in fermento, che smista e spedisce continuamente migliaia di “pacchetti” proteici verso le destinazioni corrette. Quando questo sistema di consegna fallisce nei neuroni, le conseguenze possono essere gravi disturbi cerebrali e del movimento. Questo studio svela come una delle macchine di spedizione chiave, chiamata AP-4, cambi forma e si coordini con una proteina regolatrice, ARF1, per caricare proteine nei piccoli sacchetti di trasporto e perché la sua flessibilità sia così importante per la salute neuronale.
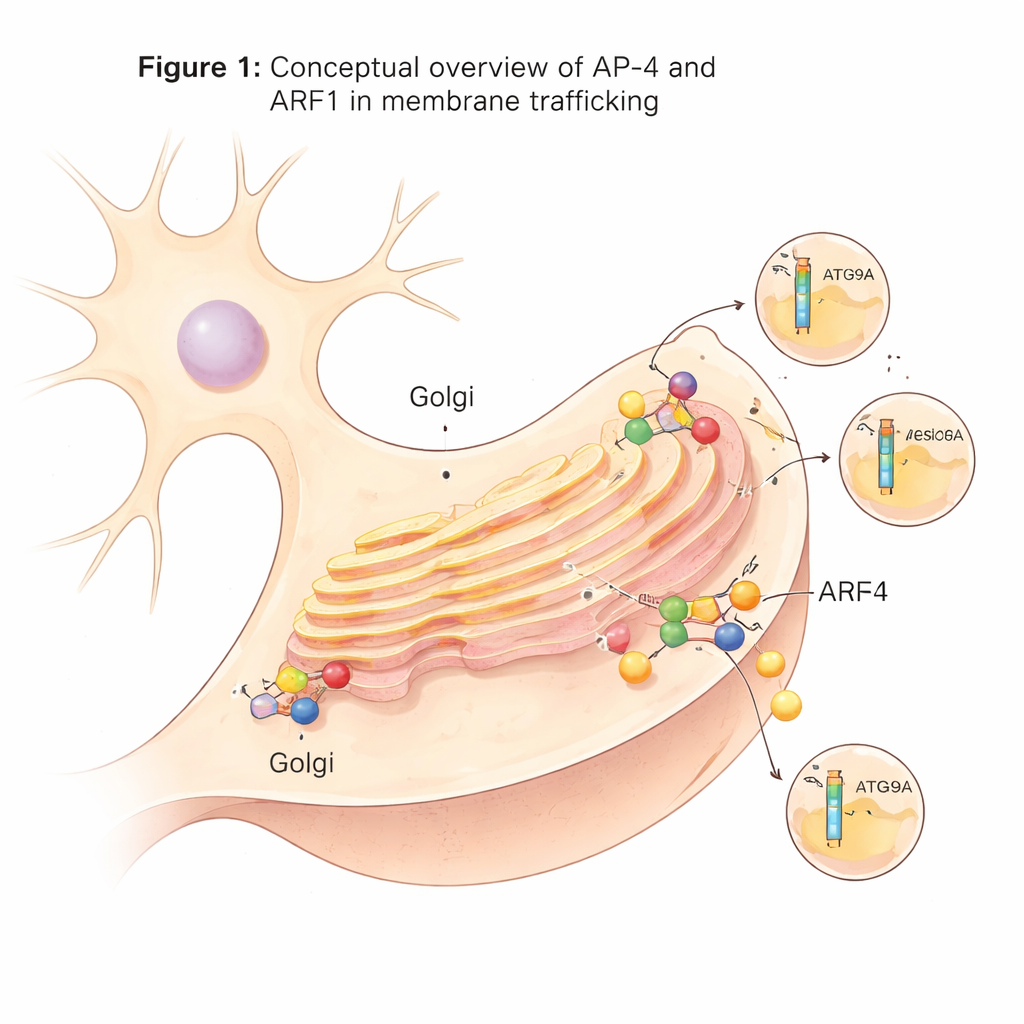
Una macchina di spedizione specializzata nei neuroni
All’interno delle cellule, molte vescicole di trasporto si staccano da una stazione di smistamento centrale nota come network trans-Golgi. Queste vescicole si avvalgono di complessi adattatori proteici, o complessi AP, che funzionano come punti di carico: riconoscono le proteine cargo e aiutano a formare vescicole rivestite attorno a esse. AP-4 è uno di questi adattatori ed è particolare perché, a differenza di molti altri, non utilizza la proteina impalcatura comune clatrina. Anche se AP-4 è prodotto in molti tessuti, svolge un ruolo particolarmente importante nei neuroni. Quando AP-4 è assente o difettoso negli esseri umani, carichi cruciali come la proteina correlata all’autofagia ATG9A e alcuni recettori del glutammato non vengono trasportati correttamente, provocando una grave condizione neuroevolutiva nota come sindrome da carenza di AP-4.
Un complesso che cambia forma a riposo
Gli autori hanno usato la crio-microscopia elettronica, una potente tecnica di imaging che può visualizzare grandi assemblaggi proteici, per determinare la struttura tridimensionale del “nucleo” del complesso AP-4 in soluzione. AP-4 è costituito da quattro subunità che insieme formano una struttura a cupola. Hanno scoperto che AP-4 non si trova in un’unica forma rigida. Invece, oscilla naturalmente fra una forma “chiusa”, in cui una subunità (il dominio C-terminale della subunità media) è ripiegata al centro della cupola, e una forma “aperta”, in cui questo elemento si apre ed è altamente flessibile. Ulteriori esperimenti di fluorescenza a singola molecola hanno mostrato che questa subunità campiona in realtà almeno tre posizioni — chiusa, parzialmente aperta e completamente aperta — rivelando che AP-4 è intrinsecamente dinamico già prima di legarsi alle membrane.
Il ruolo di ARF1: reclutatore, non interruttore principale
Molti complessi adattatori correlati vengono attivati passando da una forma inattiva a una attiva mediante il legame con piccole proteine regolatrici chiamate ARF. Per capire come avvenga questo per AP-4, i ricercatori hanno risolto le strutture di AP-4 legato ad ARF1, una piccola proteina legante GTP che si ancora alle membrane. Hanno riscontrato che ARF1 si attacca principalmente a una delle grandi subunità di AP-4 vicino al suo N-terminale, in modo simile ad altri complessi AP. Sorprendentemente, il legame con ARF1 non provoca una drammatica riorganizzazione strutturale di AP-4. Le forme chiuse e aperte coesistono ancora e l’architettura complessiva del complesso rimane in gran parte invariata. Test biochimici hanno confermato che punti di contatto specifici tra ARF1 e AP-4 sono essenziali per il reclutamento alle membrane, ma ARF1 da solo non blocca AP-4 in un unico stato attivo.
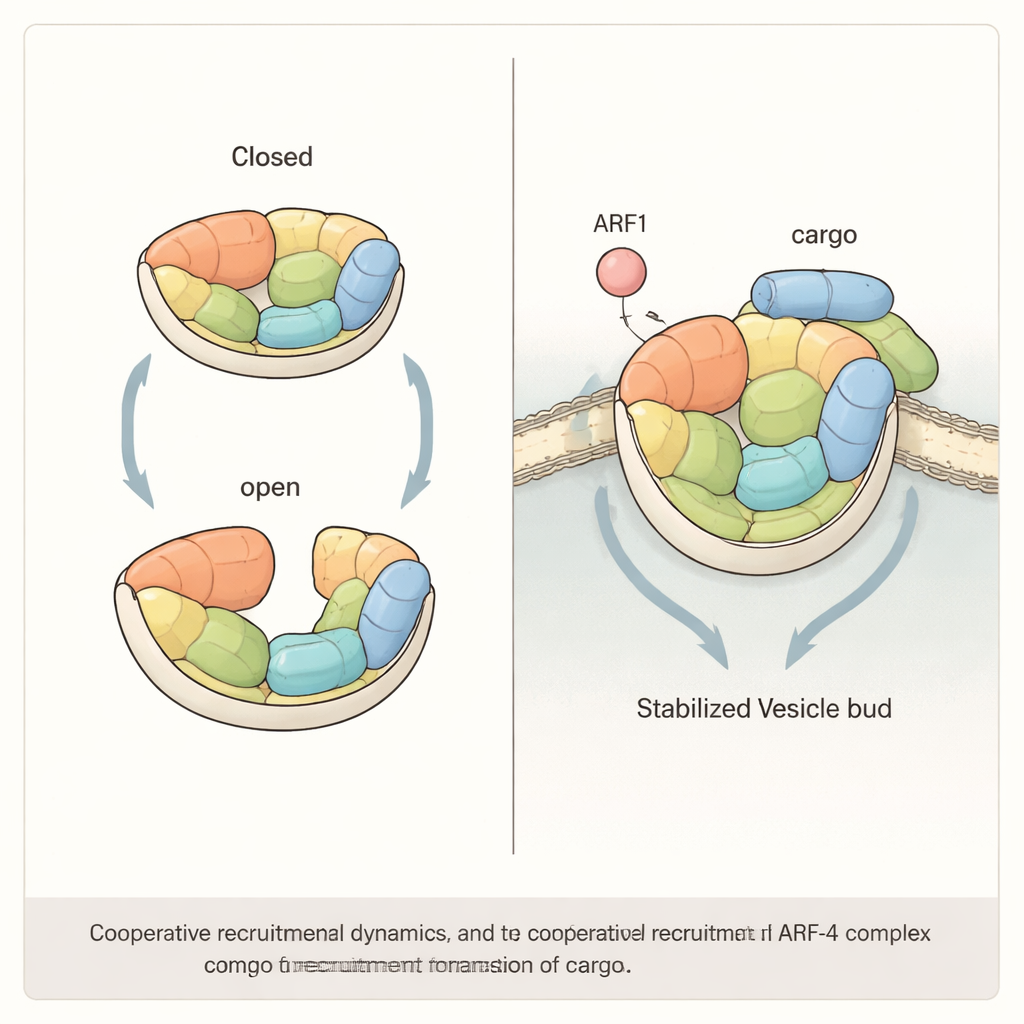
Cooperazione tra regolatore e cargo
Lo studio mostra inoltre che il reclutamento efficiente di AP-4 alle membrane richiede probabilmente la cooperazione tra ARF1 e le proteine cargo stesse. Ricostruendo il sistema su sfere artificiali e liposomi, gli autori hanno trovato che sia ARF1 sia una breve coda del cargo ATG9A possono attrarre AP-4, ma quando entrambi sono presenti insieme richiamano molto più AP-4 di quanto ci si aspetterebbe dalla semplice somma dei loro effetti individuali. Quando i ricercatori hanno introdotto mutazioni che irrigidiscono la struttura di AP-4 — riducendone la capacità di muoversi tra gli stati aperto e chiuso — questo effetto sinergico è scomparso. In cellule umane prive di una subunità chiave di AP-4, ripristinare solo versioni “rigide” mutanti del complesso non è riuscito a ripristinare il normale traffico di ATG9A dal Golgi, sottolineando che la flessibilità di AP-4 non è solo una curiosità ma un requisito funzionale.
Perché la flessibilità è importante per la salute cerebrale
Nel complesso, il lavoro ritrae AP-4 come un adattatore che cambia forma, campionando molte conformazioni in soluzione e sulle membrane. Piuttosto che funzionare come un interruttore acceso/spento, ARF1 agisce come un reclutatore basato sulla membrana che opera insieme alle proteine cargo per stabilizzare AP-4 in configurazioni produttive per la formazione di vescicole. Alterare questo equilibrio — indebolendo il legame con ARF1 o con i cargo o congelando AP-4 in una sola forma — compromette l’esportazione dei cargo dal Golgi e può contribuire a malattie neuroevolutive. Rivelando la base strutturale del comportamento dinamico di AP-4, questo studio offre un quadro per comprendere i disturbi correlati ad AP-4 e suggerisce possibili strategie future per ripristinare il traffico corretto nei neuroni affetti.
Citazione: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
Parole chiave: traffico di membrana, complesso adattatore AP-4, ARF1, formazione di vescicole, disturbo dello sviluppo neurologico