Clear Sky Science · it
Cellule NK ZNF683+ regolano la sensibilità alla chemioterapia nell'HPSCC avanzato rimodellando il microambiente immunitario
Perché alcuni trattamenti chemioterapici funzionano meglio in certi tumori della gola
Le persone con carcinoma ipofaringeo avanzato — un tumore nascosto in profondità nella gola — spesso affrontano regimi chemioterapici pesanti con risultati incerti. Alcuni tumori si riducono significativamente, mentre altri cambiano poco o niente. Questo studio pone una domanda semplice ma cruciale: che cosa è diverso all’interno dei tumori che rispondono bene? Esaminando le singole cellule immunitarie una a una, i ricercatori identificano un tipo particolare di cellula “custode” che può ribaltare l’esito tra successo e insuccesso della chemioterapia standard.
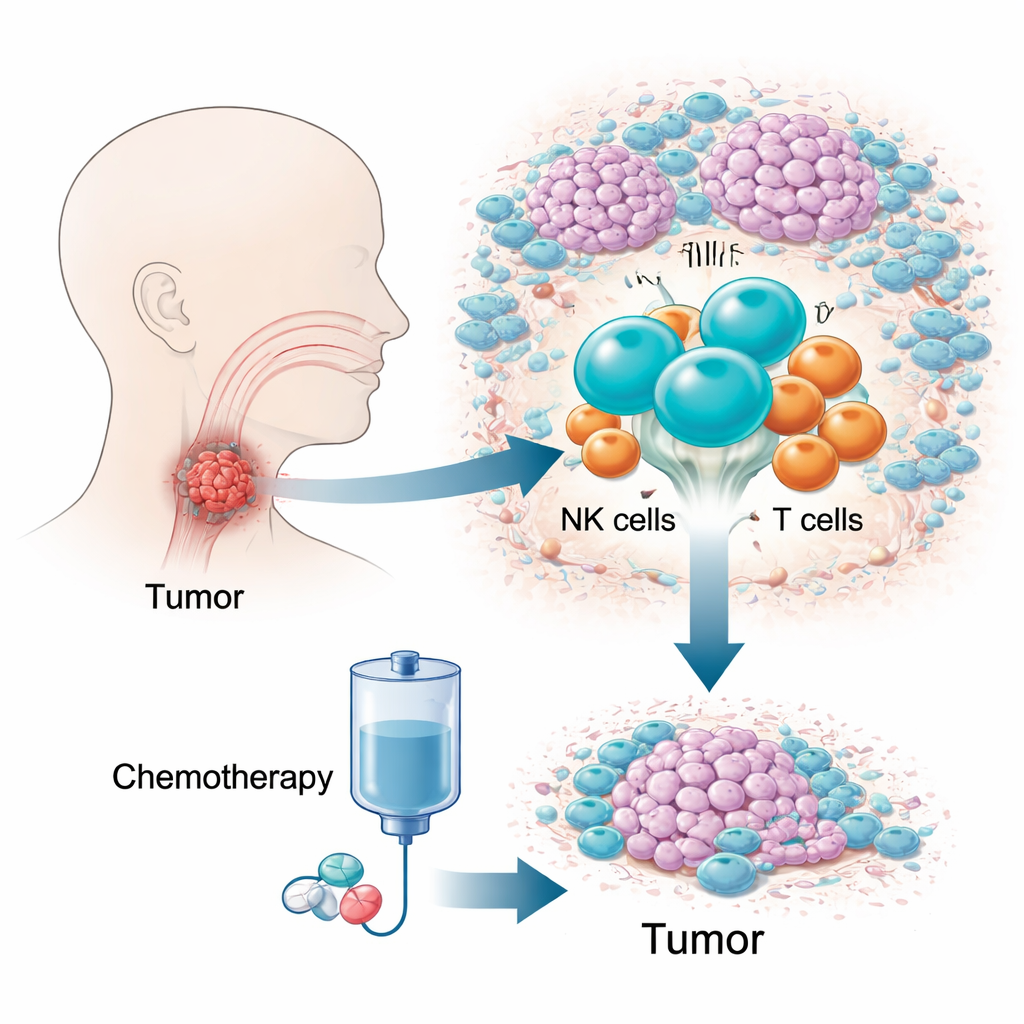
La sfida di un tumore nascosto e difficile da curare
Il carcinoma squamoso dell’ipofaringe è uno dei tumori testa-collo più letali, in parte perché cresce in un’area angusta e difficile da esplorare e causa pochi sintomi nelle fasi iniziali. Molti pazienti vengono diagnosticati tardivamente, quando le opzioni sono limitate e la sopravvivenza a cinque anni è bassa. Una combinazione di farmaci nota come chemioterapia TPF è ampiamente usata perché può controllare la malattia preservando la laringe. Tuttavia il 10–20% dei pazienti risponde poco o per nulla, perdendo tempo prezioso. I test genetici tradizionali, che mediamente rilevano segnali su milioni di cellule, hanno faticato a spiegare questa variabilità, spingendo gli autori a concentrarsi invece sull’ecosistema vivo di cellule immunitarie del tumore.
Leggere il paesaggio immunitario del tumore cellula per cellula
I ricercatori hanno seguito 12 pazienti nel tempo, raccogliendo campioni tumorali prima e dopo due cicli di chemioterapia TPF e profilando oltre 150.000 cellule immunitarie a risoluzione single-cell. Hanno inoltre esaminato altri 41 pazienti per confermare le osservazioni chiave mediante imaging e citometria a flusso. Mappando l’attività genica e il tipo di ciascuna cellula, hanno costruito un atlante dettagliato del microambiente tumorale: cellule T, B, macrofagi, cellule dendritiche, mastociti, neutrofili e cellule natural killer (NK). Tra tutti questi attori, è emerso un modello evidente. Prima del trattamento, i tumori che in seguito si ridussero contenevano molte più cellule NK rispetto a quelli resistenti alla terapia, e maggiore era la frazione di NK, maggiore risultava la regressione tumorale finale.
Un sottoinsieme speciale di NK prepara le cellule T al successo
Approfondendo, il team ha suddiviso le cellule NK in tre gruppi basati sulle loro caratteristiche molecolari. Solo uno di questi, contraddistinto dal fattore di trascrizione ZNF683 e localizzato prevalentemente nei tessuti circostanti i nest tumorali, si correlava fortemente con una buona risposta alla chemioterapia. I pazienti i cui tumori presentavano più cellule NK ZNF683+ al basale avevano molte più probabilità di beneficiare della TPF. In esperimenti su topo, la rimozione delle NK annullava quasi completamente il beneficio della chemioterapia, confermando che l’attività delle NK non è solo un marcatore ma una condizione necessaria per un trattamento efficace. In modo interessante, queste NK non si comportavano semplicemente da killer diretti delle cellule tumorali; i loro programmi genici risultavano invece arricchiti per funzioni di guida e attivazione delle cellule T.
Come le NK autorizzano potenti cellule T che uccidono il tumore
Per capire quali cellule T fossero determinanti, gli scienziati hanno seguito singoli cloni del recettore delle cellule T prima e dopo il trattamento. Hanno scoperto che nei responder un gruppo specifico di cellule T CD8 “effector memory”, arricchite per la molecola GZMK, si espandeva in modo marcato dopo la chemioterapia. Queste cellule T producevano alti livelli delle citochine tossiche TNF e interferone-gamma senza mostrare segni di esaurimento profondo, rendendole killer potenti e duraturi. L’imaging spaziale ha rivelato che, dopo il trattamento, queste cellule CD8 GZMK+ si aggregavano intensamente nei tumori dei responder ma non nei non-responder. In test di co-coltura in vitro con cellule umane, il contatto diretto con NK ZNF683+ favoriva la crescita di questo sottogruppo di CD8 GZMK+; l’effetto spariva quando le cellule venivano separate da una barriera fisica.
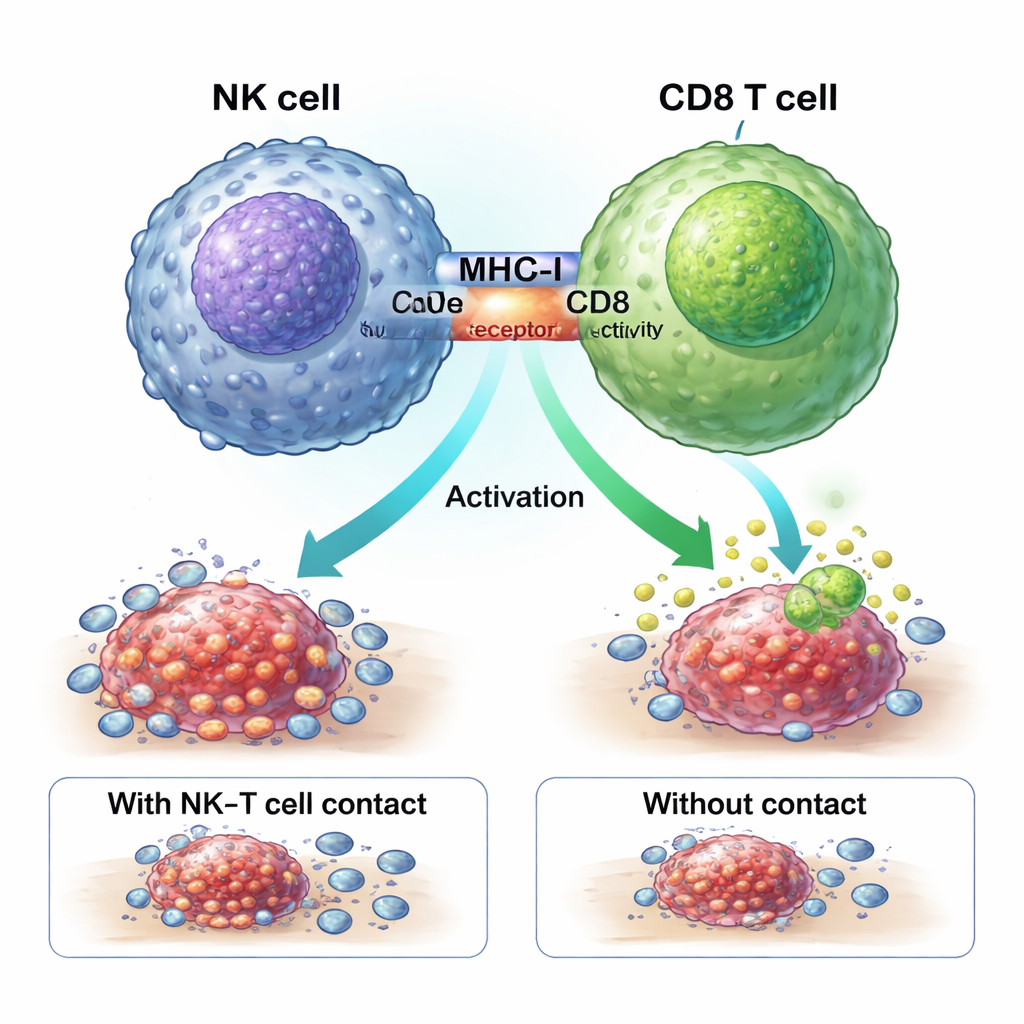
Una stretta di mano fisica che attiva i combattenti anti-tumorali
Lo studio mostra che le NK ZNF683+ potenziano la risposta alla chemioterapia tramite una “stretta di mano” fisica con le cellule T CD8. Molecole chiamate MHC-I sulla superficie delle NK si legano ai recettori CD8 sulle cellule T in una zona di contatto ravvicinato, la sinapsi immunitaria. Il blocco di MHC-I impediva alle NK di generare le potenti CD8 GZMK+. In topi ingegnerizzati privi di ZNF683 solo nelle NK, queste cellule esprimevano meno MHC-I ed erano molto meno efficaci nell’attivare le CD8, rafforzando l’idea che ZNF683 programmi le NK a diventare allenatori efficaci delle cellule T piuttosto che semplici esecutrici.
Cosa significa questo per i pazienti
Per i lettori non specialisti, il messaggio chiave è che non tutte le cellule immunitarie in un tumore sono uguali. Questo lavoro identifica un sottoinsieme specifico di NK come esploratore avanzato che prepara il campo di battaglia prima dell’avvio della chemioterapia. I tumori ricchi di queste cellule sono pronti a scatenare ondate di forti cellule T CD8 una volta somministrati i farmaci, portando a una riduzione tumorale molto maggiore. Misurare l’abbondanza di questo asse NK–T prima del trattamento potrebbe aiutare i medici a prevedere chi trarrà beneficio dalla chemioterapia TPF e chi potrebbe aver bisogno di terapie alternative o aggiuntive. In futuro, trattamenti che potenziano o mimano queste NK ZNF683+ potrebbero trasformare carcinomi ipofaringei resistenti in tumori molto più sensibili alla chemioterapia standard.
Citazione: Li, G., Xiao, W., Wu, H. et al. ZNF683+ NK cells govern chemotherapy sensitivity in advanced HPSCC via reshaping immune microenvironment. Nat Commun 17, 2069 (2026). https://doi.org/10.1038/s41467-026-68676-x
Parole chiave: carcinoma ipofaringeo, resistenza alla chemioterapia, cellule natural killer, microambiente immunitario tumorale, cellule T CD8