Clear Sky Science · it
Costruzione selettiva del legame N–N indotta dalla luce tramite rilascio e trasferimento di nitreni
Illuminare una nuova via per unire atomi di azoto
Gli atomi di azoto sono al centro di molti farmaci, agenti per la protezione delle colture e materiali avanzati. I chimici sono abili nell’attaccare l’azoto al carbonio, ma collegare direttamente due atomi di azoto è molto più difficile. Questo studio presenta un metodo senza metalli, alimentato dalla luce, per unire gli atomi di azoto in modo controllato, aprendo una via più semplice verso un’ampia gamma di molecole utili.
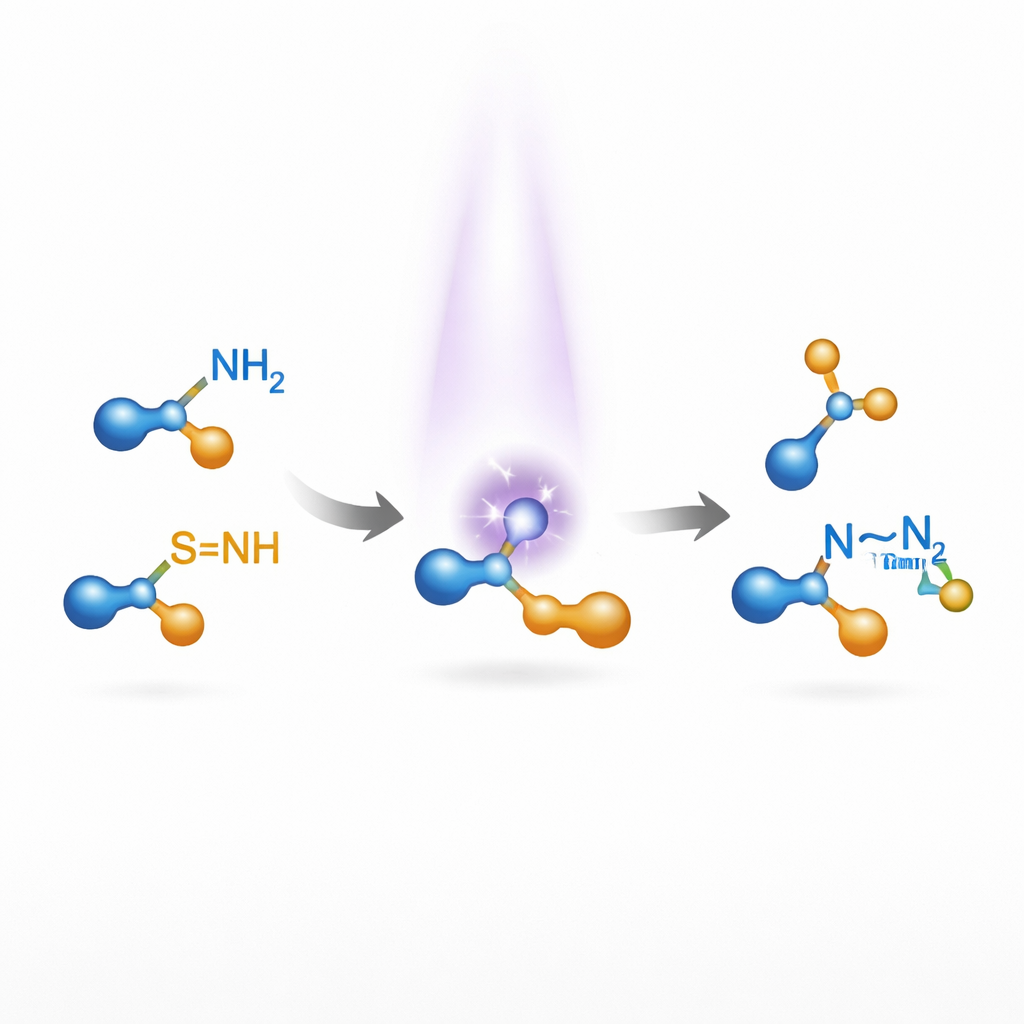
Perché è difficile collegare l’azoto all’azoto
Molti prodotti naturali e farmaci contengono coppie di atomi di azoto legati tra loro, uno schema che può modulare il comportamento di una molecola nell’organismo o nei materiali. I metodi esistenti per costruire unità N–N partono di solito da frammenti preformati contenenti azoto–azoto, come idrazine o composti diazo, e li modificano passo dopo passo. Forgiare direttamente il legame N–N a partire da ammine semplici è attraente ma difficile: l’azoto è relativamente elettronegativo, quindi due atomi di azoto non formano naturalmente un legame stabile e non polare. I successi passati hanno fatto largo uso di catalizzatori a base di metalli di transizione e funzionano spesso solo per famiglie ristrette di molecole, limitandone l’utilità nella chimica di scoperta.
Usare la luce per domare un intermediario reattivo
Gli autori si sono rivolti ai nitreni—specie di azoto altamente reattive e di breve durata che possono, in principio, inserirsi in altri legami. La chimica tradizionale dei nitreni richiede tipicamente catalizzatori metallici e può soffrire di reazioni laterali a causa dell’elevata energia dei nitreni. Il gruppo si è chiesto se fosse possibile generare nitreni in modo più delicato e controllato usando la luce, senza metalli, e quindi impiegarli per collegare ammine semplici in prodotti contenenti N–N. L’idea chiave è stata utilizzare i sulfilimini, una famiglia di molecole facili da modificare e che assorbono la luce ultravioletta e vicina al visibile. Se illuminate, queste sulfilimine possono rompersi liberando un frammento nitrene e generando come sottoprodotto un residuo contenente zolfo relativamente innocuo.
Una ricetta ampia e senza metalli per coppie di azoto
Dopo test sistematici, i ricercatori hanno identificato una particolare sulfilimina che, sotto luce a 365 nanometri in cloroformio, reagisce in modo efficiente con molte ammine per dare prodotti idrazidi—molecole con un nuovo legame N–N adiacente a un gruppo carbonilico. Hanno ottimizzato fattori come la struttura della sulfilimina, il solvente e l’intensità luminosa per favorire il prodotto desiderato rispetto a sottoprodotti comuni come le uree. In queste condizioni miti, un’ampia varietà di ammine, incluse tipologie aromatiche, alifatiche e cicliche, si è accoppiata con successo. Hanno inoltre mostrato che molte diverse sulfilimine, portatrici sia di gruppi acilici aromatici sia alifatici e di gruppi sulfonilici, partecipano bene, fornendo decine di prodotti distinti contenenti N–N. È importante che il metodo sia applicabile anche in fasi avanzate di una sintesi per modificare molecole complesse e bioattive, come comuni farmaci antinfiammatori e blocchi costruttivi chirali, dimostrando la praticità per la chimica farmaceutica e dei materiali.
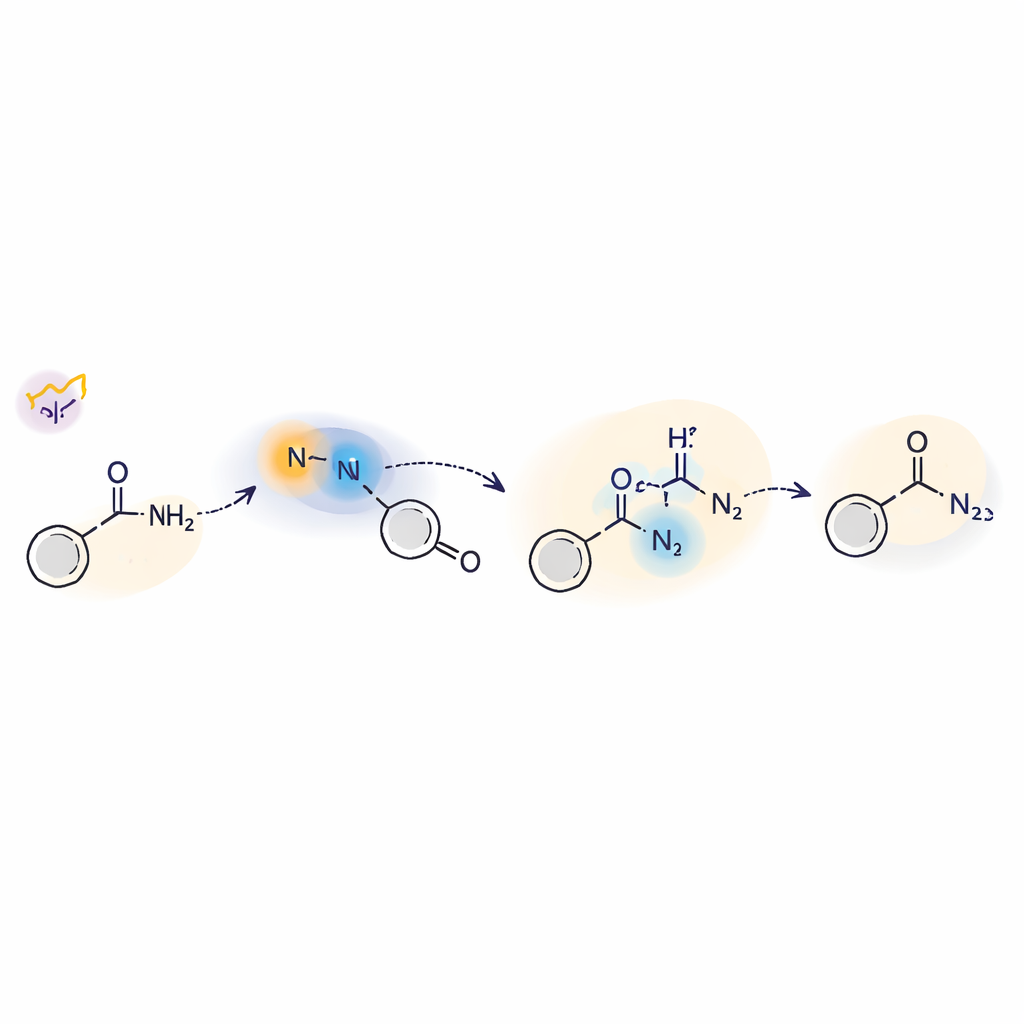
Dare uno sguardo al meccanismo della fase indotta dalla luce
Per capire come funziona questa chimica attivata dalla luce, il team ha combinato esperimenti e teoria. Hanno usato trappole radicaliche, marcatura isotopica ed risonanza paramagnetica elettronica per dimostrare che durante la reazione compaiono intermedi nitrene liberi e radicali centrati sull’azoto. La spettroscopia laser risolta nel tempo ha rivelato due forme chiave del nitrene: uno stato tripletto di breve durata e uno stato singoletto più duraturo. La forma singoletto reagisce direttamente con le ammine mediante una specie di attacco nucleofilo, mentre il tripletto può partecipare a passaggi di trasferimento di atomi di idrogeno. I calcoli al computer hanno supportato un meccanismo in cui la luce eccita la sulfilimina, il legame zolfo–azoto si scinde e il nitrene risultante interagisce con l’ammina attraverso percorsi sia singoletto sia tripletto prima di evolvere nella struttura finale dell’idrazide.
Cosa significa per le molecole del futuro
Questo lavoro mostra che sulfilimine progettate con cura possono agire come “serbatoi di nitreni” che rilasciano unità reattive di azoto su richiesta sotto luce, senza l’ausilio di metalli. Sfruttando entrambe le caratteristiche singoletto e tripletto dei nitreni mantenendo però la loro concentrazione bassa, il metodo raggiunge la formazione selettiva di legami N–N su una vasta gamma di mattoni molecolari. Per i non specialisti, il messaggio è che i chimici dispongono ora di un modo più semplice, pulito e flessibile per unire atomi di azoto, che potrebbe accelerare la scoperta di nuovi farmaci, agrochimici e materiali ricchi di azoto.
Citazione: Yu, M., Feng, J., Wang, X. et al. Photo-induced selective N-N bond construction via harnessing nitrene release and transfer. Nat Commun 17, 2084 (2026). https://doi.org/10.1038/s41467-026-68674-z
Parole chiave: chimica dei nitreni, reazioni indotte dalla luce, formazione del legame N–N, sulfilimine, idrazidi