Clear Sky Science · it
Fotosintesi della glicina tramite accoppiamento C−N di plastica di scarto e nitrato su catalizzatore diatomico Pd−B
Trasformare i rifiuti nei mattoni della vita
Bottiglie di plastica, contenitori per alimenti e capi in poliestere sono ovunque — e lo sono anche i rifiuti che lasciano. Allo stesso tempo, molte fabbriche scaricano acque reflue ricche di nitrati che possono inquinare fiumi e mari. Questo studio mostra come affrontare entrambi i problemi contemporaneamente: usando la luce solare e un catalizzatore appositamente progettato per trasformare plastica scartata e nitrato in glicina, un amminoacido semplice ampiamente impiegato in alimenti, medicina e agricoltura.
Perché la glicina e i rifiuti contano
La glicina è uno dei mattoni fondamentali delle proteine ed è prodotta su scala di centinaia di migliaia di tonnellate all’anno. I metodi industriali convenzionali, in particolare il classico processo di Strecker, fanno affidamento su composti cianurati tossici e condizioni di reazione severe, sollevando preoccupazioni di sicurezza e ambientali. Nel frattempo, la produzione globale di PET — usato in bottiglie, tessuti e imballaggi — supera i 100 milioni di tonnellate annue, e oltre l’80% finisce in discarica o nell’ambiente. Quando il PET viene depolimerizzato chimicamente, uno dei prodotti è l’etilenglicole, un liquido di scarso valore difficile da purificare. Gli autori pongono una domanda semplice: invece di trattare etilenglicole e nitrato come rifiuti, non potrebbero diventare materie prime per produrre glicina usando solo la luce solare?
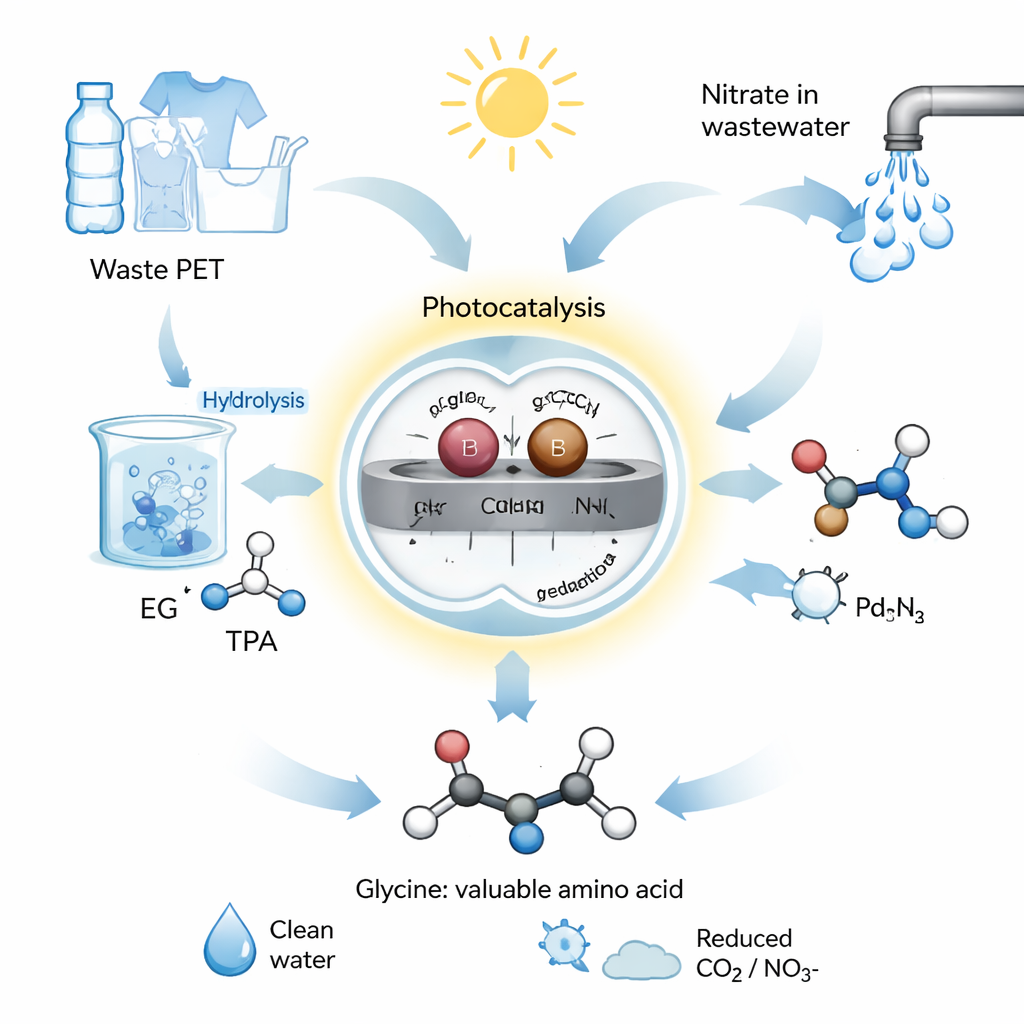
Un percorso chimico guidato dal sole
Il team ha progettato un sistema fotocatalitico, cioè che usa la luce per guidare reazioni chimiche. Hanno costruito un catalizzatore partendo da nitruro di carbonio grafitico, un semiconduttore, e hanno ancorato coppie di singoli atomi di palladio (Pd) e boro (B) sulla sua superficie. Queste coppie atomiche agiscono come una squadra microscopica di due elementi, ciascuno occupandosi di una metà diversa della chimica. Nel loro processo, i rifiuti di PET sono prima idrolizzati — scissi in acqua alcalina — per rilasciare etilenglicole. Questo etilenglicole e i nitrati provenienti dalle acque reflue vengono quindi messi in acqua con il catalizzatore Pd–B ed esposti a luce solare simulata o naturale. In queste condizioni miti, il sistema converte la miscela in glicina con un rendimento elevato e una selettività superiore al 92%, cioè si formano pochissimi sottoprodotti indesiderati.
Come funziona il duo atomico
Il successo del catalizzatore dipende da come gestisce gli intermedi di reazione a vita breve. I siti di boro sulla superficie sono "ricchi di lacune" (hole‑rich), il che significa che accettano facilmente carica positiva quando il materiale assorbe luce. In questi siti B, l’etilenglicole viene ossidato con delicatezza — privato di idrogeno — per formare glicolaldeide, una molecola instabile che normalmente tende a sovra‑ossidarsi in acidi o perfino anidride carbonica. I siti di palladio, al contrario, sono "ricchi di elettroni". Essi utilizzano gli elettroni generati dalla luce per ridurre i nitrati passo dopo passo fino ad ammonio o ammoniaca. Il passaggio chiave è un accoppiamento carbonio–azoto tra la glicolaldeide e queste specie azotate per formare etanolammina, che viene poi ulteriormente ossidata, di nuovo principalmente nei siti B, per dare glicina. Stabilizzando la glicolaldeide il tempo necessario perché reagisca, e mantenendo elettroni e lacune spazialmente separati, la coppia Pd–B indirizza la chimica lontano da reazioni collaterali inutili e verso l’amminoacido desiderato.
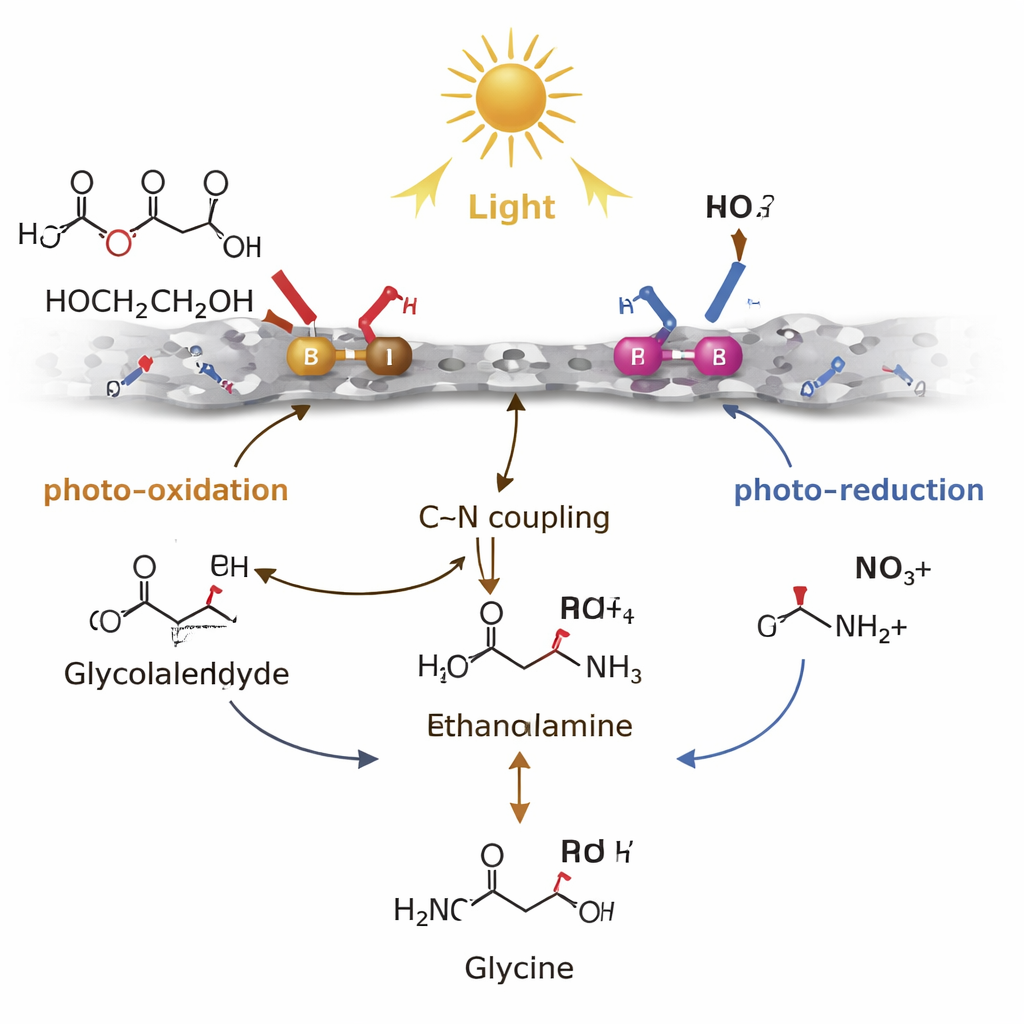
Dal meccanismo in laboratorio ai rifiuti reali
I ricercatori hanno confermato ogni parte di questo percorso con un insieme di tecniche, tracciando radicali, intermedi e prodotti azotati in tempo reale. Hanno confrontato diversi materiali e metalli catalizzatori e hanno scoperto che supporti di g‑C3N4 con coppie isolate Pd–B mostravano le migliori prestazioni, raggiungendo tassi di produzione di glicina di 2,9 millimoli per grammo di catalizzatore all’ora. Il catalizzatore è rimasto attivo su più cicli e la sua struttura è rimasta stabile. Cosa importante, il team è andato oltre i reagenti puri da laboratorio. Hanno dimostrato una produzione di glicina su scala di grammi a partire da PET post‑consumo reale — polveri, bottiglie, vestiti, borse e altro — combinato con soluzioni di nitrato e perfino acque reflue complesse. Hanno inoltre mostrato che alcoli correlati derivati dalla biomassa, come la glicerina, possono fungere da fonti carboniose alternative, ampliando la rilevanza dell’approccio.
Una soluzione vantaggiosa per rifiuti e clima
Per avvicinare il concetto alla pratica, gli autori hanno testato il loro processo sotto luce solare naturale concentrata con una semplice lente di Fresnel. Il sistema ha prodotto costantemente glicina con alta selettività, e le modellizzazioni suggeriscono che una scala maggiore potrebbe evitare emissioni significative di anidride carbonica e prevenire il rilascio di nitrati nell’ambiente. In termini semplici, questo lavoro delinea un modo per convertire montagne di plastica usata e acque inquinate in un amminoacido utile, usando solo la luce e un catalizzatore finemente progettato. Pur restando sfide ingegneristiche da affrontare prima di un’applicazione industriale, lo studio evidenzia come il progetto dei catalizzatori a livello atomico possa trasformare due grandi flussi di rifiuti in un unico prodotto chimico di valore.
Citazione: Ya, Z., Li, M., Fu, D. et al. Glycine photosynthesis via C−N coupling of waste plastic and nitrate over diatomic Pd−B catalyst. Nat Commun 17, 1887 (2026). https://doi.org/10.1038/s41467-026-68666-z
Parole chiave: glicina, riciclo della plastica, fotocatalisi, acque reflue nitratiche, catalizzatori ad atomo singolo