Clear Sky Science · it
Regolazione dell’assemblaggio dell’adattatore AP1 dal chaperone bifronte MEA1
Perché questo aiutante nascosto della cellula è importante
All’interno di ogni cellula umana, migliaia di piccoli pacchetti trasportano proteine dove servono oppure al “centro di riciclaggio” cellulare per la degradazione. Questo traffico mantiene le cellule in salute e regola le nostre difese immunitarie. L’articolo riassunto qui rivela una proteina prima misteriosa, chiamata MEA1, che si dimostra essenziale per costruire una delle macchine di smistamento chiave che caricano questi pacchetti. Capire come funziona MEA1 aiuta a spiegare come le cellule controllano carichi importanti, incluse molecole che accendono o spengono risposte antivirali.
Controllo del traffico nell’hub di spedizione della cellula
Gran parte dell’attività di spedizione cellulare passa attraverso una struttura chiamata Golgi, una pila di sacche appiattite che funziona come un ufficio centrale postale. Dal Golgi, il carico può essere inviato alla superficie cellulare per l’uso o reindirizzato a compartimenti interni per la degradazione. Un complesso proteico noto come AP1 sta al centro di questa via. AP1 riconosce etichette sulle proteine cargo, aiuta a curvare la membrana e recluta un rivestimento esterno di clatrina per formare piccole vescicole di trasporto. Senza un AP1 correttamente assemblato, carichi cruciali si accumulano nei posti sbagliati e percorsi di segnalazione normali, compresi quelli legati all’immunità, possono andare fuori controllo. 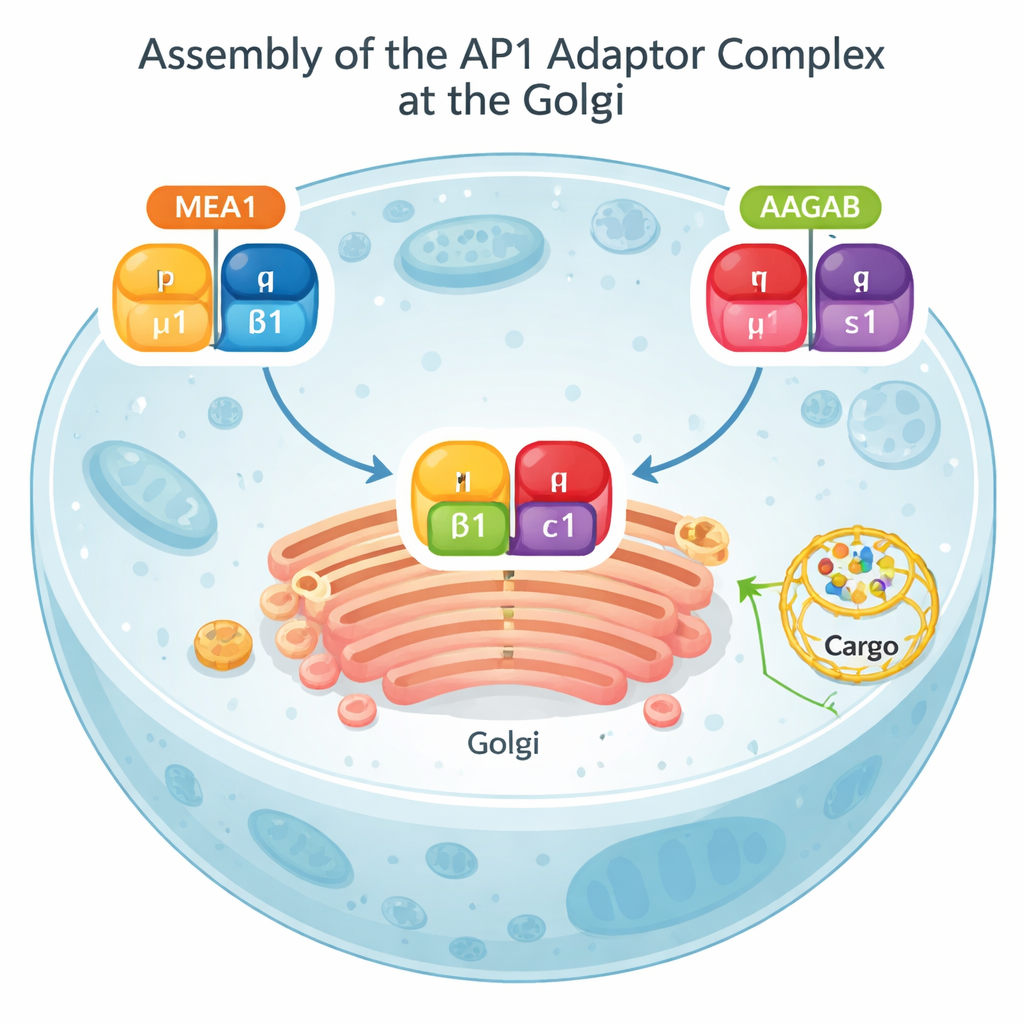
Alla ricerca di un operaio mancante per l’assemblaggio
Gli autori hanno cercato di identificare proteine che si associano fisicamente ad AP1 e che potrebbero aiutarne l’assemblaggio. Hanno analizzato un ampio database di interazioni proteiche, eliminato candidati improbabili e poi usato uno strumento di intelligenza artificiale, AlphaFold, per prevedere come le proteine rimaste potessero entrare in contatto con le singole parti di AP1. Questa ricerca ha messo in evidenza MEA1, una proteina piccola e precedentemente non caratterizzata, presente in molti tessuti. Esperimenti successivi in cellule umane hanno confermato che MEA1 si lega a due specifici subunità di AP1, note come μ1 e β1, sia quando testate singolarmente sia nel loro stato naturale non modificato.
MEA1 mantiene AP1 intatto e il traffico dei carichi in movimento
Per indagare cosa fa effettivamente MEA1, i ricercatori hanno eliminato il gene MEA1 in linee cellulari umane. In assenza di MEA1, tutte e quattro le parti di AP1 risultarono drasticamente ridotte e i punti caratteristici di AP1 vicino al Golgi quasi scomparvero. Questa perdita ebbe chiare conseguenze funzionali. Un cargo di AP1, il recettore del folato FOLR1, si accumulò sulla superficie cellulare invece di essere inviato all’interno, segno distintivo di un difetto nello smistamento da parte di AP1. Un altro cargo, la proteina di segnalazione immunitaria STING, non venne più confezionata in modo efficiente in vescicole dirette ai lisosomi, i centri di riciclaggio della cellula. Di conseguenza, STING attivato e la sua chinasi partner TBK1 rimasero elevati, indicando che l’“interruttore off” per questa via antivirale non funzionava correttamente. La reintroduzione di MEA1 ripristinò i livelli di AP1 e correggeva questi difetti di traffico.
Un chaperone a due ‘mani’ e un processo di assemblaggio basato sulla collisione
Test biochimici e modelli di AlphaFold hanno rivelato che MEA1 si comporta come un chaperone di assemblaggio “bifronte”: la sua porzione anteriore afferra la subunità μ1, mentre la porzione posteriore afferra β1. Da soli, μ1 e β1 sono instabili e tendono ad aggregarsi o ad essere distrutti; legati a MEA1 diventano solubili e pronti per l’assemblaggio. Un altro chaperone noto, AAGAB, svolge un lavoro parallelo per le altre due subunità di AP1, γ e σ1. Quando i complessi MEA1–μ1–β1 e AAGAB–γ–σ1 si incontrano, le loro subunità si combinano in un adattatore AP1 completo a quattro parti. A quel punto, entrambi i chaperoni si staccano e ritornano nel fluido cellulare, mentre l’AP1 neoformato si sposta verso le membrane per svolgere il suo lavoro di smistamento. Questo meccanismo di “collisione a doppio chaperone” mostra che l’assemblaggio di AP1 è attentamente orchestrato e non lasciato al caso.
Lezioni più ampie sul controllo di qualità cellulare
Oltre ad AP1, lo studio suggerisce una strategia più generale che le cellule potrebbero usare per costruire molte grandi macchine proteiche. MEA1 può anche assistere debolmente un altro complesso adattatore chiamato AP2 e, insieme ad AAGAB e a un terzo chaperone chiamato CCDC32, illustra una via più ampia che gli autori definiscono “Assemblaggio di Proteine Adattatrici Assistito da Chaperoni”. In questo schema, chaperoni specializzati stabilizzano subunità fragili, mettono insieme le coppie corrette e bloccano temporaneamente i siti di legame dei cargo fino a che il complesso non è completamente formato e sicuro da impiegare. 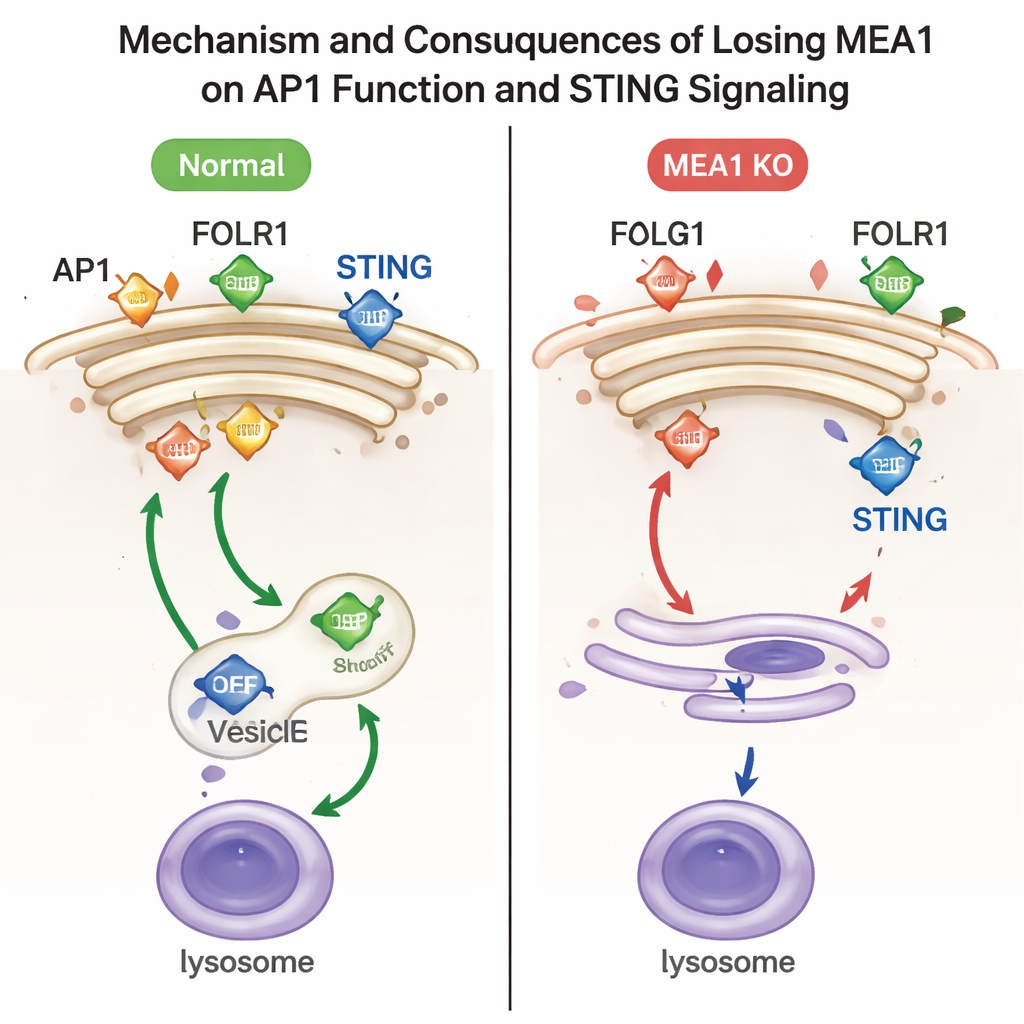
Che cosa significa per salute e malattia
Per i non specialisti, il punto chiave è che MEA1 è un importante operatore dietro le quinte che aiuta ad assemblare AP1, una macchina centrale di smistamento nelle nostre cellule. Quando MEA1 manca, AP1 si disfa, si formano ingorghi di traffico e regolatori importanti come STING non vengono spenti correttamente. Questa nuova comprensione potrebbe infine aiutare a spiegare alcuni disturbi immunitari o altre malattie legate a un traffico proteico difettoso e rivela un principio generale su come le cellule costruiscono in modo sicuro macchine molecolari complesse da parti instabili.
Citazione: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
Parole chiave: traffico proteico, proteina adattatrice AP1, chaperoni molecolari, segnalazione STING, biologia cellulare