Clear Sky Science · it
Riconoscimento molecolare della tireoglobulina da parte della sortilina
Come le cellule tiroidee decidono quando rilasciare l’ormone
Gli ormoni tiroidei regolano il nostro “termostato” metabolico, influenzando tutto, dalla frequenza cardiaca alla temperatura corporea. Questi ormoni sono sintetizzati e immagazzinati all’interno di una proteina gigantesca chiamata tireoglobulina. Questo studio svela come un’altra proteina, la sortilina, aiuti le cellule tiroidee a selezionare quale forma di tireoglobulina richiamare all’interno della cellula affinché l’ormone possa essere rilasciato nel flusso sanguigno — una decisione che alla fine determina la quantità di ormone tiroideo disponibile per il corpo.
Una proteina di deposito in attesa di essere processata
La tireoglobulina è una proteina enorme a forma di Y prodotta e secreta dalle cellule tiroidee in una massa gelatinosa chiamata colloide. Lì svolge il ruolo di materia prima e di magazzino per gli ormoni tiroidei: specifici residui aminoacidici all’interno della tireoglobulina vengono modificati chimicamente con iodio per diventare ormoni tiroidei, rimanendo tuttavia incorporati nella proteina più grande. Per liberare effettivamente questi ormoni, la tireoglobulina deve essere richiamata nella cellula, degradata all’interno di compartimenti di riciclo chiamati lisosomi e i frammenti ormonali trasportati nel sangue.
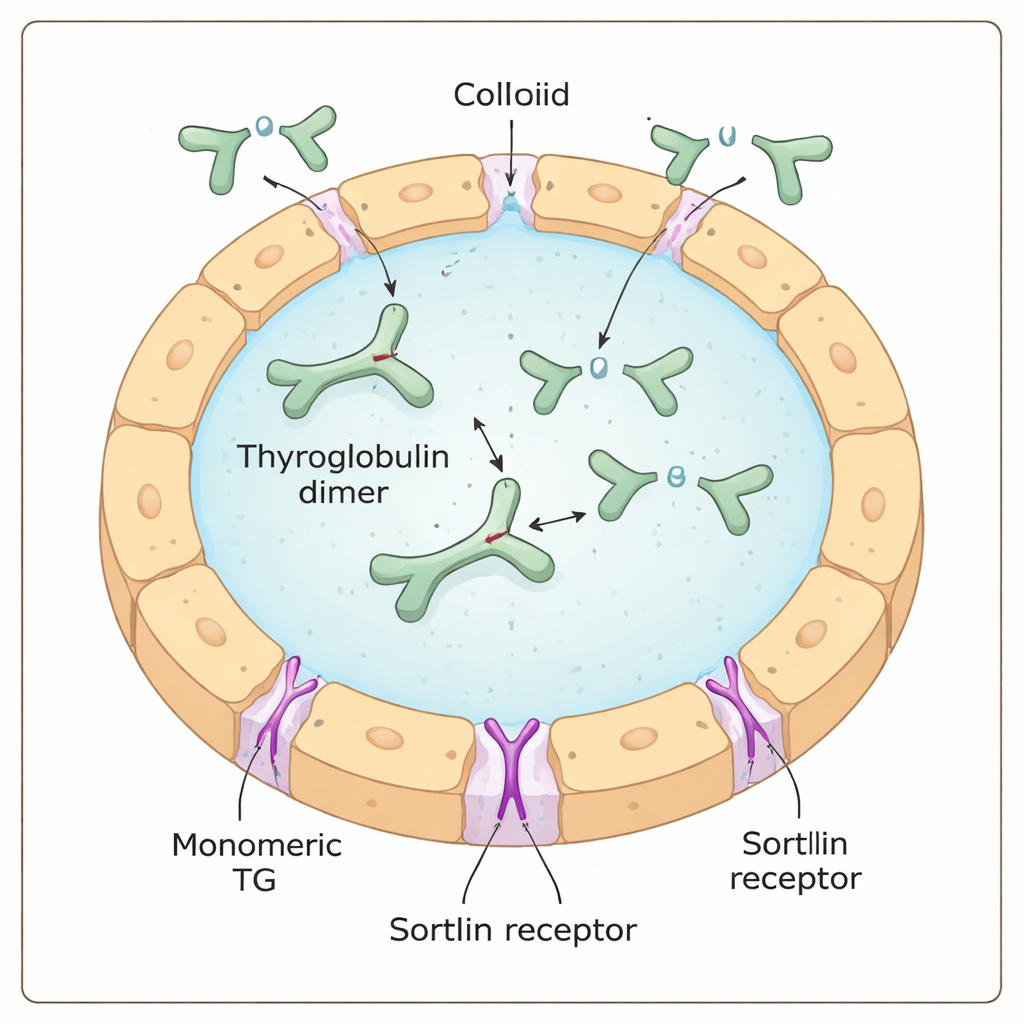
Un guardiano cellulare con una preferenza nascosta
Il recettore sortilina è stato proposto come uno dei “guardiani” che legano la tireoglobulina sulla superficie cellulare e la guidano verso l’interno. Lavori precedenti suggerivano che la sortilina preferisse la tireoglobulina altamente iodata, insinuando che il recettore potesse in qualche modo percepire direttamente il contenuto di iodio. Utilizzando una combinazione di test biochimici, misurazioni di massa a singola molecola e esperimenti di captazione su cellule, gli autori hanno invece scoperto che la sortilina favorisce nettamente la forma monomerica (a unità singola) della tireoglobulina rispetto alla sua più comune forma dimerica (accoppiata). Più monomero è presente in un campione, più efficacemente formava complessi con la sortilina ed era internalizzato dalle cellule tiroidee, indipendentemente dalla quantità di iodio che conteneva.
Avvicinarsi al punto di contatto
Per comprendere questa preferenza a livello atomico, il gruppo ha impiegato microscopia crio–elettronica ad alta risoluzione e spettrometria di massa con cross-linking. Questi metodi hanno mostrato che la sortilina riconosce una breve coda flessibile al C-terminale (una estremità) della tireoglobulina monomerica. Questa coda si infila in una cavità centrale della sortilina, modellata come una elica a dieci pale, ancorandosi in due piccoli “punti caldi” interni. È notevole che, nella forma dimerica della tireoglobulina, parte della regione intorno a questa coda sia sepolta e quindi inaccessibile alla sortilina, spiegando perché il dimerio è un partner povero. I dati suggeriscono che il taglio o l’allentamento extracellulare della tireoglobulina — attraverso la degradazione proteica naturale — contribuisca a convertire i dimeri in monomeri che la sortilina può catturare.
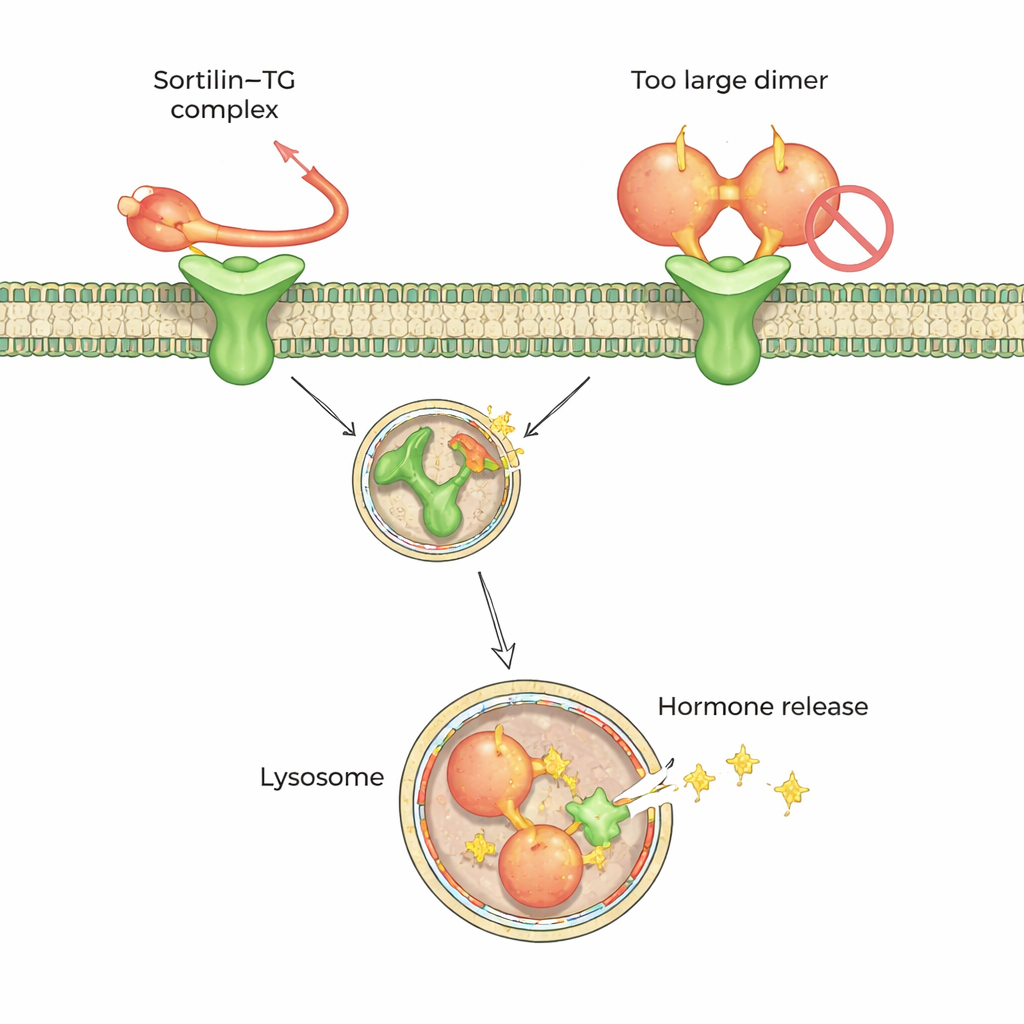
Un codice di aggancio condiviso per molti carichi
La sortilina non è una proteina esclusiva della tiroide; partecipa al traffico di molte molecole diverse nell’organismo, compresi fattori collegati a malattie cardiache e disturbi cerebrali. Combinando il loro lavoro strutturale con avanzati strumenti di predizione strutturale come AlphaFold e AlphaPulldown, i ricercatori hanno confrontato come dozzine di noti partner della sortilina potrebbero legare la sua cavità a elica. Hanno riscontrato un motivo ricorrente: molti cargo presentano un segmento peptidico non strutturato di circa venti aminoacidi che si adatta nella stessa tasca della coda della tireoglobulina, talvolta corrono nella stessa direzione di un peptide cerebrale noto, la neurotensina, e talvolta nella direzione opposta. Nonostante l’orientamento invertito, questi peptidi condividono caratteristiche simili — un gruppo acido o carico negativamente a un’estremità, un residuo aromatico voluminoso all’altra estremità e un tratto flessibile, spesso ricco di prolina, nel mezzo.
Perché lo iodio conta meno della forma
Poiché il contatto chiave tra sortilina e tireoglobulina è questa coda flessibile, gli autori hanno testato se aggiungere iodio a una tirosina della coda coinvolta nella formazione dell’ormone avrebbe modificato il legame. Non è cambiato: un peptide sintetico contenente un ormone tiroideo completamente formato si comportava quasi identicamente alla versione non modificata. La modellazione ha mostrato che l’anello iodato sporge nel solvente senza creare nuovi contatti stretti. Insieme agli esperimenti di captazione, questo supporta una visione rivista: la sortilina non «conteggia» gli atomi di iodio sulla tireoglobulina. Piuttosto, avverte se la proteina si è rilassata o è stata parzialmente degradarta a sufficienza da esporre la sua forma monomerica e la coda nel modo corretto.
Cosa significa per la salute della tiroide
Per un non specialista, il messaggio centrale è che il rilascio degli ormoni tiroidei è regolato meno da un sensore interno dello iodio e più da un controllo meccanico sulla forma e flessibilità della proteina. La sortilina agisce come uno scanner sulla superficie cellulare, cercando molecole di tireoglobulina che siano state allentate o tagliate in monomeri, per poi richiamarle all’interno per il rilascio finale dell’ormone e il riciclo dello iodio. Questo lavoro chiarisce un passaggio chiave nella biologia degli ormoni tiroidei e suggerisce che farmaci progettati per bloccare la sortilina — ora oggetto di studio per altre malattie — potrebbero involontariamente alterare la gestione degli ormoni tiroidei interferendo con questo passo di riconoscimento.
Citazione: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
Parole chiave: ormone tiroideo, tireoglobulina, sortilina, traffico proteico, endocitosi