Clear Sky Science · it
L’elica ponte di Cas12a è un regolatore allosterico della formazione dell’R-loop e dell’attivazione di RuvC
Perché questo conta per l’editing genico
Molti potenti strumenti per l’editing genetico, inclusi quelli alla base di terapie emergenti e test diagnostici rapidi, si basano su proteine CRISPR che tagliano il DNA in siti selezionati. Se queste forbici molecolari tagliano nel punto sbagliato possono però provocare effetti collaterali dannosi. Questo studio analizza una piccola parte mobile all’interno dell’editor Cas12a, chiamata elica ponte, e mostra come i cambiamenti della sua conformazione funzionino come un interruttore di sicurezza interno che collega il riconoscimento corretto del bersaglio al taglio del DNA. Comprendere questo interruttore fornisce una road map per progettare strumenti CRISPR più precisi e più sicuri per applicazioni mediche e biotecnologiche.
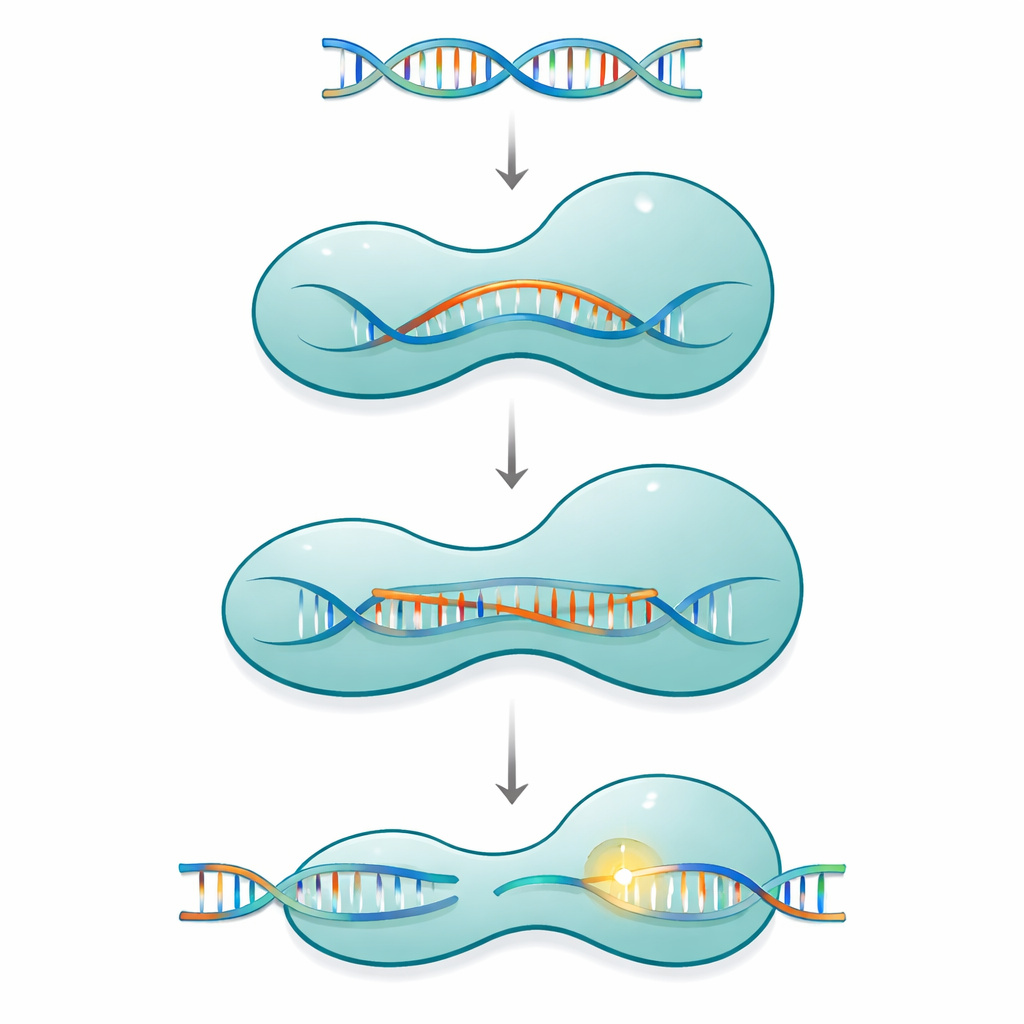
Una morsa molecolare con parti mobili
Cas12a appartiene a una famiglia di sistemi CRISPR a singola proteina che usano un breve RNA guida per trovare e tagliare DNA corrispondente in virus o nel genoma di una cellula. La proteina ha la forma di una morsa a due bracci: un lato di riconoscimento che verifica la sequenza e un lato di taglio che ospita il macchinario chimico. Queste due metà sono connesse da un sottile segmento carico positivamente chiamato elica ponte. Quando Cas12a lega il suo RNA guida e poi il DNA bersaglio, la proteina non si comporta come uno strumento rigido. Si muove invece attraverso una serie di grandi e piccoli cambiamenti conformazionali che si chiudono gradualmente attorno a una crescente struttura ibrida RNA–DNA nota come R-loop, attivando completamente il sito di taglio solo dopo che si è formato un tratto sufficientemente lungo di appaiamento corretto delle basi.
Indagare l’interruttore di sicurezza interno
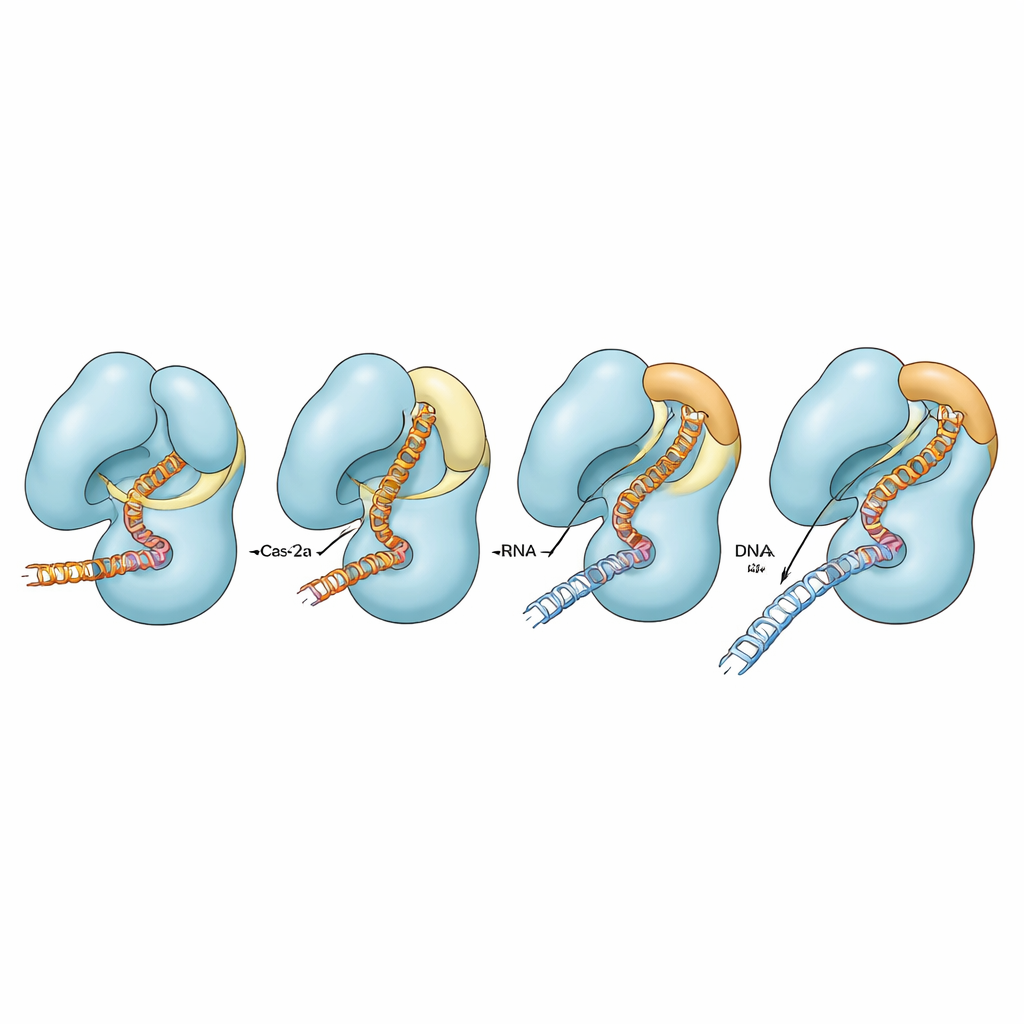
I ricercatori si sono concentrati su una Cas12a del batterio Francisella novicida e su una versione precedentemente ingegnerizzata nella quale due amminoacidi nell’elica ponte sono stati sostituiti con prolina, una modifica nota per irrigidire o interrompere le eliche. Questa variante, chiamata FnoCas12aKD2P, taglia il DNA in modo più selettivo ma più lento rispetto alla proteina naturale. Usando la criomicroscopia elettronica hanno catturato cinque istantanee strutturali distinte di questa variante legata al suo RNA guida e a un frammento di DNA bersaglio. Queste istantanee mostrano la proteina in diverse fasi del suo percorso di attivazione, dal primo riconoscimento del DNA fino a stati successivi in cui parte dell’ibrido RNA–DNA è formata ma la piena prontezza al taglio non è ancora stata raggiunta.
Come i cambiamenti di forma guidano il taglio accurato
Il confronto della variante con strutture già determinate della Cas12a normale ha rivelato un motivo chiaro. Nella proteina naturale, un segmento dell’elica ponte passa da un anello flessibile a un’elica più lunga e dritta e si piega verso l’ibrido RNA–DNA in crescita, entrando in stretto contatto con esso. Allo stesso tempo, un’elica vicina nel dominio di taglio si allenta e una piccola regione chiamata “coperchio”, che normalmente blocca il sito attivo, si ribalta da un anello a un’elica e si apre. Questi movimenti coordinati aprono una tasca che consente a un singolo filamento di DNA di entrare ed essere tagliato. Nella variante contenente prolina, l’elica ponte non riesce a completare questa transizione da anello a elica né a piegarsi correttamente. Di conseguenza, l’ibrido RNA–DNA rimane distorto e più distante, il coperchio resta in uno stato chiuso simile a un anello e il complesso raggiunge raramente una conformazione completamente precatalitica. Questo collo di bottiglia meccanico rallenta il taglio on-target e rende più difficile per DNA con mismatch superare i checkpoint interni.
Affinare la fedeltà modificando i contatti
Per valutare come diversi contatti intorno al coperchio e all’elica ponte contribuiscano all’attività, gli autori hanno modificato residui caricati specifici che collegano queste regioni. Nella Cas12a normale, interrompere questi contatti aveva solo effetti modesti sul taglio del DNA perfettamente corrispondente, sebbene in alcune condizioni ciò abbia influenzato l’efficienza con cui veniva clivato il secondo filamento quando erano presenti mismatch. Nello sfondo con l’elica ponte compromessa, tuttavia, le stesse sostituzioni riducevano gravemente o quasi abolivano il taglio di entrambi i filamenti, specialmente quando guida e DNA non corrispondevano perfettamente. Simulazioni al computer hanno supportato questi risultati, mostrando che solo quando l’elica ponte può assumere pienamente la sua forma elicoidale il ponte, l’elica adiacente, il coperchio e gli acidi nucleici si muovono in modo fortemente coordinato. Quando l’elica è compromessa, questi movimenti diventano parzialmente o completamente scollati e l’enzima fatica a completare il suo ciclo catalitico.
Una guida di progettazione per strumenti CRISPR di nuova generazione
Nel complesso, il lavoro rivela l’elica ponte come una leva di controllo interna che collega la lunghezza e la qualità dell’ibrido RNA–DNA all’apertura della tasca di taglio in Cas12a. Costringendo la proteina a completare una specifica sequenza di cambiamenti conformazionali prima di clivare il DNA, questo meccanismo applica naturalmente la discriminazione dei mismatch. I risultati aiutano a spiegare perché modifiche mirate in questa piccola regione possono produrre varianti di Cas12a con ridotto taglio fuori bersaglio e diminuita attività “collaterale” sul DNA, proprietà desiderabili per editing del genoma e diagnostica più sicuri. Più in generale, lo studio mette in evidenza come spostamenti sottili in piccole eliche possano coordinare la comunicazione a lunga distanza in grandi macchine molecolari, offrendo principi generali per progettare enzimi di lavorazione degli acidi nucleici ad alta fedeltà.
Citazione: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
Parole chiave: CRISPR-Cas12a, fedeltà dell’editing genico, elica ponte, formazione dell’R-loop, regolazione allosterica