Clear Sky Science · it
RoboA rafforza il destino delle cellule staminali planarie attraverso FoxA e Anosmin1a
Come i vermi ricrescono i loro organi
Alcuni platelminti possono ricostruire quasi ogni parte mancante del corpo, dal loro tubo alimentare fino al cervello. Questa notevole abilità dipende da cellule staminali adulte in grado di trasformarsi, su richiesta, in molti diversi tipi cellulari. Ma con tanta libertà, come fanno queste cellule a evitare di costruire il tessuto sbagliato nel posto sbagliato — per esempio, generare cellule dello stomaco nella testa invece dei neuroni? Questo studio utilizza la planaria per scoprire come un piccolo insieme di segnali mantiene le cellule staminali altamente flessibili sulla strada giusta durante la rigenerazione.
Il verme rigenerante e il suo potenziale nascosto
La planaria Schmidtea mediterranea è un modello molto usato per studiare la rigenerazione perché una larga popolazione di cellule staminali è distribuita in tutto il corpo. Un organo chiave è la faringe, un tubo muscolare per l’alimentazione che si trova al centro del verme e si apre all’esterno quando l’animale si nutre. Lavori precedenti hanno mostrato che un gene chiamato foxA è cruciale per ricostruire questa faringe dopo un danno, e che solo certe cellule staminali vicine alla faringe normalmente attivano foxA. Il nuovo studio pone una domanda apparentemente semplice: cosa impedisce alle cellule staminali in altre regioni — specialmente nella testa e nel cervello — di scegliere anch’esse un’identità faringea?
Quando viene meno la guida
I ricercatori si sono concentrati su una proteina recettore chiamata RoboA, presente a bassi livelli in molti tipi cellulari, comprese le cellule staminali. Quando hanno ridotto l’attività di RoboA mediante interferenza RNA, gli animali spesso sviluppavano faringi addizionali e mal posizionate dopo il taglio. Un’ispezione più ravvicinata ha rivelato qualcosa di più sottile: anche nei vermi non feriti, l’abbassamento di RoboA causava la comparsa di neuroni e muscoli di tipo faringeo all’interno della regione cerebrale. Questi “neuroni faringei ectopici” si comportavano come normali cellule faringee dal punto di vista dell’espressione genica, ma si trovavano nel posto sbagliato. Importante, il piano corporeo generale e l’architettura cerebrale rimanevano per lo più intatti, suggerendo che RoboA non stesse rimodellando l’intero animale, ma piuttosto regolava con precisione ciò che le cellule staminali vicine diventavano.
Un interruttore a tre attori per il destino cellulare
Per capire come funziona RoboA, il team ha cercato partner al di fuori della cellula. Sebbene le proteine Robo siano note soprattutto per legare un ligando chiamato Slit, l’abbassamento di Slit non ha riprodotto le cellule faringee mal posizionate. Una vasta schermata RNAi di proteine secrete e di membrana ha invece individuato Anosmin1a (Anos1a), una proteina secreta correlata a un fattore umano coinvolto nella sindrome di Kallmann. La riduzione di Anos1a ha provocato neuroni faringei extra simili, e gli abbassamenti combinati di RoboA–Anos1a si comportavano come se agissero nella stessa via. Allo stesso tempo, il profilamento molecolare ha mostrato che il fattore di trascrizione FoxA è al centro della decisione: quando RoboA è presente, mantiene FoxA spento nelle cellule staminali della testa; quando la segnalazione RoboA viene rimossa, FoxA si attiva e quelle stesse cellule staminali possono scegliere un destino da neurone faringeo pur trovandosi nel cervello.
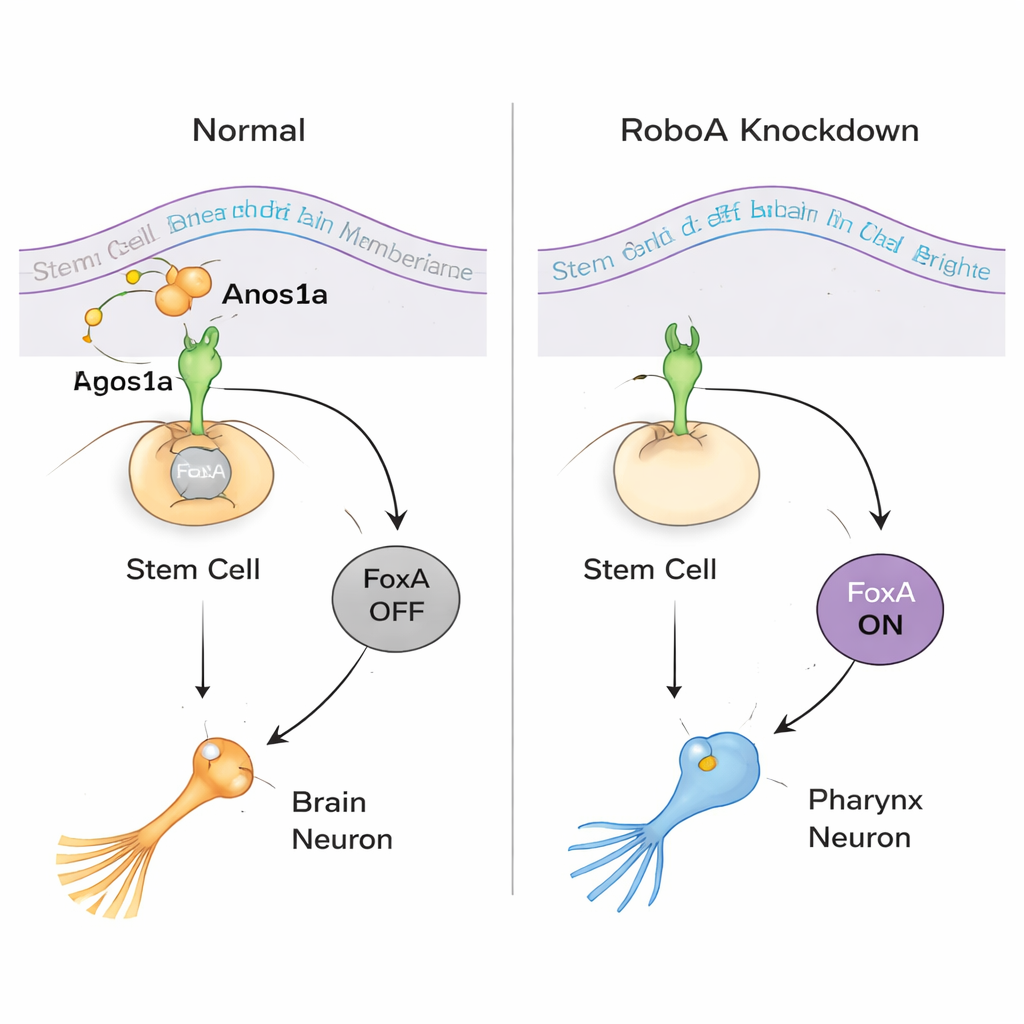
Rivelare una scelta bidirezionale nelle cellule staminali
Il gruppo ha poi chiesto se questa flessibilità operasse in entrambe le direzioni. Negli animali normali, le cellule staminali intorno alla faringe si affidano a FoxA per diventare neuroni faringei e cellule epiteliali, mentre i muscoli faringei seguono un percorso diverso. Quando FoxA è stato silenziato per periodi prolungati, i vermi hanno perso completamente le faringi e hanno sviluppato escrescenze anomale al centro del corpo. L’analisi tramite RNA-seq a singola cellula e l’uso di marcatori hanno rivelato che queste escrescenze contenevano molti tipi cellulari normalmente limitati alla testa, incluse cellule degli occhi e neuroni specifici del cervello. In altre parole, quando FoxA manca nel luogo in cui la faringe dovrebbe formarsi, le cellule staminali locali tendono per default verso un destino simile al cervello. Questa scoperta mostra che le stesse cellule staminali possono essere spinte verso identità “faringe” o “cervello” a seconda dei segnali che ricevono.
Affinare la rigenerazione, non ridisegnare la mappa
Mettendo insieme tutte le evidenze, gli autori propongono che la rigenerazione planaria sia guidata su due livelli. Ampi segnali di “controllo della posizione”, come Wnt e altre molecole di patterning, stabiliscono la mappa grossolana di testa, tronco e coda. Su questo strato, geni locali “che rinforzano il destino” come RoboA e Anos1a agiscono come controlli di sicurezza, bloccando opzioni inadeguate. Nella testa, la segnalazione RoboA–Anos1a mantiene FoxA spento affinché le cellule staminali producano neuroni cerebrali invece di cellule faringee; vicino alla faringe, FoxA può invece accendersi e guidare destini specifici della faringe. Questo controllo stratificato permette alle cellule staminali planarie di rimanere straordinariamente plastiche pur ricostruendo gli organi nel posto giusto, offrendo un progetto di come una rigenerazione robusta possa coesistere con un ordine anatomico rigoroso.
Citazione: Wang, KT., Tsai, FY., Chen, YC. et al. RoboA reinforces planarian stem cell fate through FoxA and Anosmin1a. Nat Commun 17, 1971 (2026). https://doi.org/10.1038/s41467-026-68656-1
Parole chiave: rigenerazione delle planarie, plasticità delle cellule staminali, modellamento degli organi, segnalazione RoboA, fattore di trascrizione FoxA