Clear Sky Science · it
NeoPrecis: migliorare la predizione della risposta all’immunoterapia attraverso l’integrazione di paesaggi neoantigenici qualificati e consapevoli della clonalità
Perché alcuni tumori rispondono all’immunoterapia e altri no
L’immunoterapia ha trasformato la cura del cancro, eppure molti pazienti non ne traggono beneficio e alcuni affrontano effetti collaterali gravi. Una domanda cruciale è perché alcuni tumori vengono individuati e distrutti dal sistema immunitario mentre altri sfuggono. Questo studio presenta NeoPrecis, un metodo computazionale che esamina più in profondità le “segnalazioni” che i tumori mostrano al sistema immunitario — chiamate neoantigeni — e usa queste informazioni per prevedere con maggiore accuratezza quali pazienti sono probabili responder alle immunoterapie moderne.
Nuove «segnalazioni» sulle cellule tumorali
Le cellule tumorali accumulano mutazioni del DNA che possono alterare le proteine che producono. Piccoli frammenti di queste proteine alterate, noti come neoantigeni, possono essere esposti sulla superficie cellulare e riconosciuti come estranei dai linfociti T, gli «assassini» del sistema immunitario. Per anni medici e ricercatori si sono affidati a misure grossolane come il carico mutazionale tumorale — il numero totale di mutazioni — per stimare la probabilità che un tumore risponda agli inibitori del checkpoint immunitario. Ma è uno strumento rozzo: non ogni mutazione crea un bersaglio visibile o attraente per i linfociti T, e i tumori possono essere mosaici di molti sottotipi cellulari. NeoPrecis è stato progettato per andare oltre il semplice conteggio delle mutazioni e valutare invece quante di esse rappresentino davvero bersagli promettenti in tutto il tumore.
Considerare tre ingredienti chiave insieme
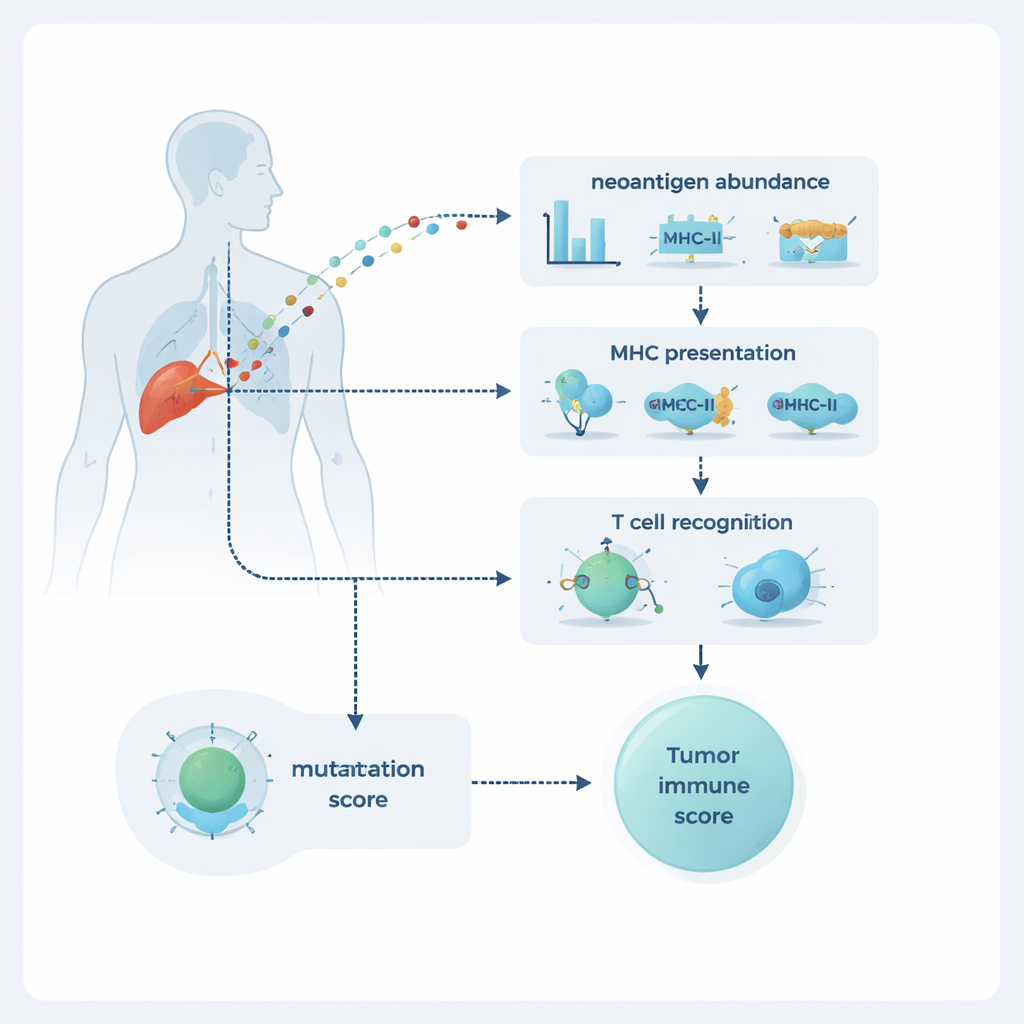
NeoPrecis valuta ogni mutazione secondo tre dimensioni: quanto è abbondante nel tumore, se è probabile che venga esposta sulla superficie cellulare e quanto è probabile che venga notata dai linfociti T. L’abbondanza è stimata tramite sequenziamento del DNA e dell’RNA, che rivelano quanto comune sia la mutazione e quanto sia fortemente espressa. L’esposizione è modellata attraverso il legame alle molecole chiamate MHC di classe I e II, che agiscono come pannelli che mostrano frammenti proteici ai linfociti T. La parte più innovativa è il componente di riconoscimento dei linfociti T, NeoPrecis-Immuno. Questo modello apprende da grandi database di interazioni note tra linfociti T e peptidi per valutare quanto un frammento mutato si discosti dal suo corrispondente normale in modo rilevante per il riconoscimento da parte dei T, tenendo conto anche delle varianti MHC specifiche che ciascuna persona possiede.
Insegnare a un computer ciò che i linfociti T «vedono»
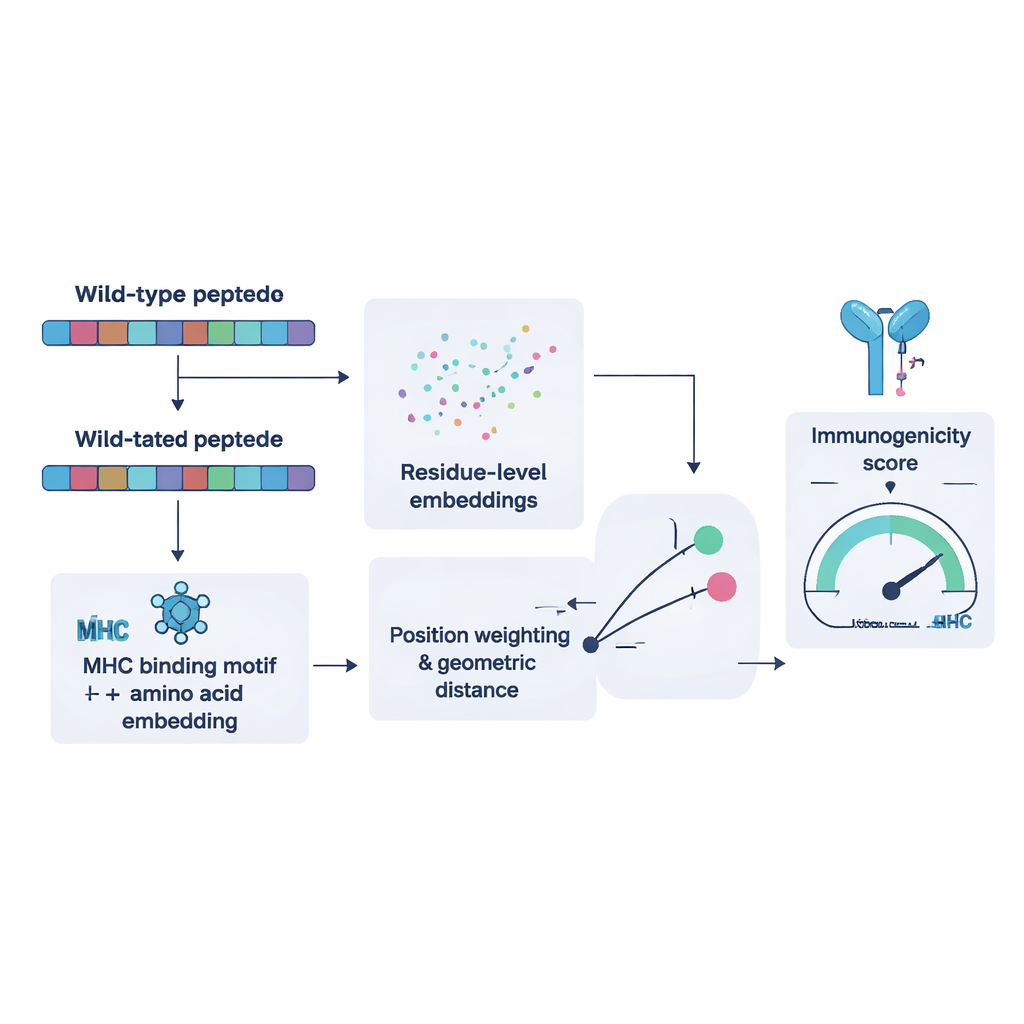
Per addestrare NeoPrecis-Immuno, i ricercatori hanno prima raccolto migliaia di esempi in cui lo stesso linfocita T riconosce più peptidi simili e altri che non riconosce. Hanno usato questi esempi per insegnare al modello che i frammenti mutati che assomigliano molto a quelli normali sono meno propensi a scatenare un attacco immunitario, perché tali bersagli simili al self vengono di solito eliminati durante lo sviluppo dei linfociti T. Il modello rappresenta ogni peptide come un punto in uno spazio matematico modellato sia dalla sua sequenza di aminoacidi sia dalle preferenze di legame delle molecole MHC della persona. Misura quindi quanto il peptide mutato si discosti dall’originale. Distanze maggiori, informate da motivi specifici, corrispondono a una maggiore probabilità di essere immunogeni. Testato rispetto agli strumenti esistenti su dataset oncologici indipendenti, NeoPrecis-Immuno ha eguagliato o superato le prestazioni, specialmente con l’MHC di classe II, che presenta ai linfociti T helper che supportano e sostengono le risposte anti-tumorali.
Dalle singole mutazioni all’intero tumore
Le mutazioni individuali sono solo una parte della storia; conta anche come sono distribuite all’interno del tumore. Alcune mutazioni sono «clonali», presenti in quasi tutte le cellule tumorali, mentre altre sono «sottoclonali», presenti solo in nicchie specifiche. NeoPrecis costruisce un «paesaggio neoantigenico» sommando i suoi punteggi di immunogenicità attraverso le mutazioni e sovrapponendo informazioni su quali sottoclonalità appartengono e quanto siano diffuse. Questo produce punteggi a livello tumorale che evidenziano i tumori ricchi di neoantigeni forti e ampiamente condivisi — specialmente quelli che possono essere presentati sia su MHC di classe I sia di classe II e potenzialmente innescare risposte coordinate di T helper e T killer. In gruppi di pazienti con melanoma e carcinoma polmonare non a piccole cellule trattati con inibitori del checkpoint, questi punteggi basati su NeoPrecis hanno separato con maggiore accuratezza responder e non-responder rispetto ai conteggi mutazionali standard, risultando particolarmente utili nei tumori polmonari complessi e eterogenei.
Cosa significa per i pazienti
Per i pazienti, la promessa di NeoPrecis è un abbinamento più preciso delle immunoterapie a chi ha più probabilità di beneficiarne e una comprensione più chiara del perché alcuni tumori resistono al trattamento. Concentrandosi sulla qualità e sulla distribuzione dei neoantigeni — non solo sulla loro quantità — il quadro aiuta a spiegare perché tumori con carichi mutazionali simili possono comportarsi in modo molto diverso. In futuro, mappe così dettagliate del paesaggio immuno-visibile di un tumore potrebbero guidare non solo l’uso degli inibitori del checkpoint, ma anche la progettazione di vaccini oncologici personalizzati che diano priorità ai bersagli più potenti e ampiamente condivisi nel cancro di ciascuna persona.
Citazione: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
Parole chiave: immunoterapia del cancro, neoantigeni, eterogeneità tumorale, inibitori del checkpoint, oncologia computazionale