Clear Sky Science · it
Stenotrophomonas favorisce la progressione dei tumori gastrointestinali mediante la degradazione di STING nelle cellule tumorali e la riduzione della risposta immunitaria
Germi nascosti all'interno dei tumori
La maggior parte delle persone sa che i microbi nell'intestino possono influenzare la digestione e persino l'umore, ma pochi si rendono conto che batteri vivi possono effettivamente insediarsi all'interno delle cellule tumorali stesse. Questo studio rivela come un comune batterio presente nell'ambiente, Stenotrophomonas, si nasconda all'interno dei tumori gastrointestinali e li aiuti silenziosamente a crescere, attenuando al contempo le difese immunitarie dell'organismo e riducendo l'efficacia delle moderne immunoterapie antitumorali.
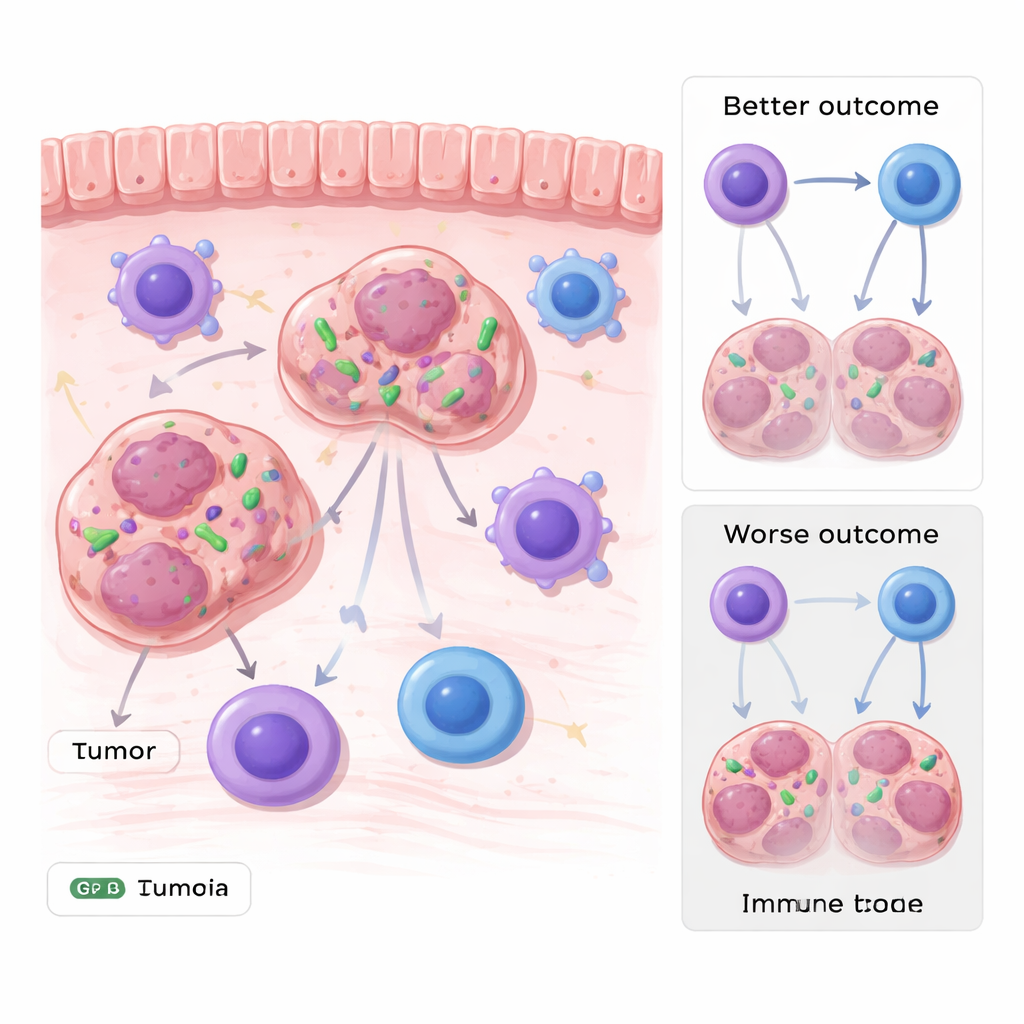
Batteri che vivono nelle cellule tumorali
I tumori gastrointestinali, come i tumori di stomaco e del colon-retto, crescono a stretto contatto con le ricche comunità batteriche del tratto digerente. Analizzando più set di dati genetici di pazienti e poi validando i risultati nei campioni tumorali, i ricercatori hanno riscontrato che il DNA di Stenotrophomonas era insolitamente abbondante in diversi tipi di tumori gastrointestinali. È importante sottolineare che la sua presenza non era semplicemente una contaminazione superficiale: metodi di imaging, comprese sonde fluorescenti e microscopia elettronica, hanno rivelato batteri interi nel citoplasma delle cellule tumorali. I pazienti i cui tumori contenevano livelli più elevati di questo batterio tendevano ad avere un decorso peggiore nel tempo, collegando il microbo a una prognosi sfavorevole.
Come un microbo altera l'equilibrio immunitario
Il gruppo si è poi chiesto se questi batteri nascosti fossero solo concomitanti a tumori aggressivi o se contribuissero attivamente alla progressione della malattia. In modelli murini, hanno infettato cellule tumorali con Stenotrophomonas etichettato con fluorofori prima di impiantarle negli animali. I tumori che ospitavano il batterio crescevano più velocemente e raggiungevano dimensioni maggiori rispetto a quelli privi del microbo, in diversi tipi cellulari tumorali. Analizzando il paesaggio immunitario circostante, hanno osservato che il numero totale di cellule immunitarie, compresi linfociti T e macrofagi, era simile. La differenza critica riguardava un sottogruppo specializzato di macrofagi che esprimono una molecola chiamata MHC-II, che li aiuta a presentare frammenti tumorali ai linfociti T citotossici. Nei tumori che ospitavano Stenotrophomonas, questi macrofagi MHC-II–positivi erano notevolmente ridotti e i T cell mostravano una minore attività citotossica contro il cancro.
Interrompere un sistema d'allarme cellulare
Per comprendere il meccanismo, i ricercatori si sono concentrati su una via d'allarme chiave all'interno delle cellule nota come STING, che normalmente rileva DNA estraneo e innesca il rilascio di segnali antivirali “di pericolo” chiamati interferoni di tipo I. In esperimenti in vitro, le cellule tumorali infettate da Stenotrophomonas producevano molta meno interferone beta e i geni normalmente attivati da questa via risultavano silenziati. Lo studio ha mostrato che il batterio induce stress nel reticolo endoplasmatico, la “fabbrica” di ripiegamento delle proteine della cellula, e poi sfrutta una via di controllo di qualità chiamata degradazione associata al reticolo endoplasmatico (ER-associated degradation). Attraverso una proteina ausiliaria chiamata SEL1L, questa via segnala la proteina STING per la distruzione nel proteasoma, il “tritatutto” cellulare. Con livelli di STING depleti, la cellula tumorale invia un allarme più debole, con minore produzione di interferone e, a valle, una ridotta attivazione dei macrofagi MHC-II–positivi.
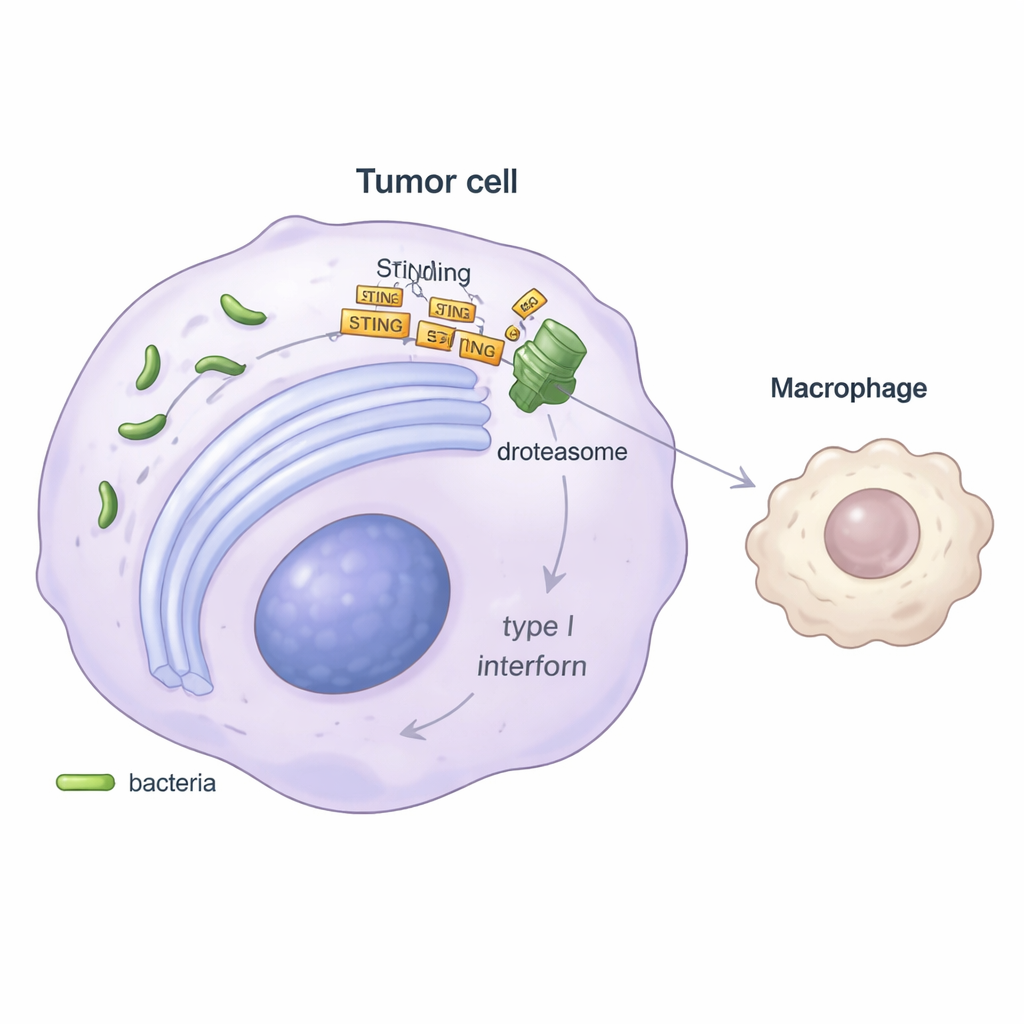
Compromettere l'immunoterapia — e una possibile soluzione
Poiché le immunoterapie moderne come gli anti–PD-1 si basano su risposte vigorose dei linfociti T, il team ha testato l'effetto di Stenotrophomonas intracellulare sul trattamento. Nei topi, i tumori che ospitavano il batterio rispondevano male all'anti–PD-1 rispetto a tumori privi di batteri, anche se combinati con chemioterapia. I linfociti T in questi tumori mostravano marcatori ridotti di attività e proliferazione, coerenti con una scarsa stimolazione immunitaria. In modo significativo, quando i ricercatori trattarono gli animali con l'antibiotico levofloxacina, efficace nel uccidere Stenotrophomonas, la crescita tumorale rallentò e la risposta alla terapia anti–PD-1 migliorò. Ripristinare la segnalazione degli interferoni con un farmaco a base di interferone clinicamente utilizzato riusciva inoltre a recuperare la popolazione di macrofagi MHC-II–positivi e a riattivare in alcuni casi l'attività citotossica dei T cell, sottolineando il ruolo centrale di questa via.
Cosa significa per i pazienti
Per un lettore non specialista, il messaggio chiave è che alcuni tumori gastrointestinali possono essere “armati” con un proprio microbioma interno che li aiuta a sfuggire all'attacco immunitario. Stenotrophomonas, degradando il sistema d'allarme STING all'interno delle cellule tumorali, attenua i segnali immunitari che normalmente mobiliterebbero macrofagi e linfociti T citotossici. Questo non solo accelera la crescita tumorale, ma può anche contribuire a spiegare perché alcuni pazienti non traggono beneficio dalle potenti immunoterapie. Sebbene siano necessari ulteriori studi prima che ciò modifichi la pratica clinica, i risultati suggeriscono la possibilità che testare i tumori per la presenza di tali batteri — e trattarli selettivamente con antibiotici mirati o con farmaci che stabilizzino STING — possa un giorno migliorare gli esiti per le persone con tumori di stomaco e del colon-retto.
Citazione: Feng, H., Chen, K., Xi, Z. et al. Stenotrophomonas promotes gastrointestinal tumor progression via STING degradation in tumour cells and mitigated immune response. Nat Commun 17, 2042 (2026). https://doi.org/10.1038/s41467-026-68649-0
Parole chiave: microbioma tumorale, cancro gastrointestinale, Stenotrophomonas, via STING, immunoterapia oncologica