Clear Sky Science · it
NR6A1 è essenziale per la specificazione, la formazione e la sopravvivenza delle cellule della cresta neurale
Come le prime decisioni cellulari modellano il volto e il corpo
Prima della nascita, un gruppo speciale di cellule chiamate cellule della cresta neurale migra attraverso l'embrione per contribuire a costruire il volto, il cuore, i nervi e altro ancora. Quando queste cellule non si comportano correttamente, i neonati possono nascere con gravi malformazioni congenite. Questo studio mette in luce un interruttore molecolare finora sottovalutato, una proteina chiamata NR6A1, che aiuta a decidere quando e dove si formano le cellule della cresta neurale negli embrioni dei mammiferi e cosa succede quando questo interruttore fallisce.
I costruttori vaganti dell'embrione
Le cellule della cresta neurale compaiono molto presto nello sviluppo, lungo il confine tra il tessuto in formazione che diventerà cervello e midollo spinale. Dopo essersi distaccate da questo tessuto, migrano per lunghe distanze per dare origine a molte strutture diverse, dalle ossa e cartilagini del volto a parti del sistema nervoso periferico e alle cellule pigmentate della pelle. Poiché contribuiscono a così tanti organi, anche piccole alterazioni nella loro formazione possono causare condizioni diffuse note come neurocristopatie, tra cui sindromi craniofacciali come la sindrome di Treacher Collins. Capire come queste cellule appaiono per la prima volta è quindi centrale per spiegare sia lo sviluppo normale sia i difetti alla nascita.
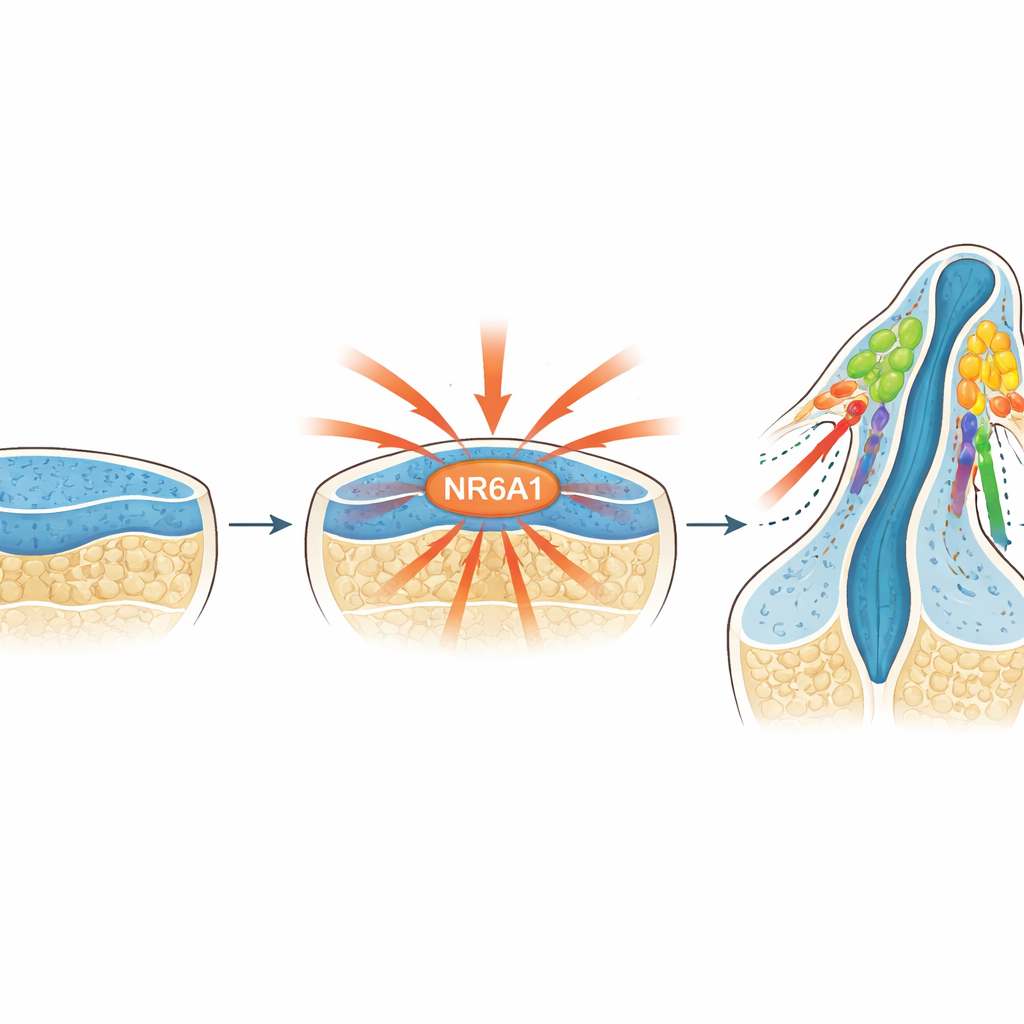
Un interruttore maestro riconosciuto di recente
I ricercatori si sono concentrati su NR6A1, un membro della famiglia dei recettori nucleari di proteine che controllano l'attività genica. Lavori precedenti suggerivano che NR6A1 potesse essere coinvolto in difetti della testa e del volto, ma il suo ruolo nelle cellule della cresta neurale era sconosciuto. Monitorando NR6A1 in embrioni di topo a partire subito dopo l'impianto, il gruppo ha osservato che la sua presenza combaciava strettamente con dove e quando le cellule della cresta neurale si formano normalmente: appare nel tessuto neurale precoce, si concentra lungo il lato dorsale del cervello e del midollo spinale in sviluppo ed è visibile anche nelle cellule proprio mentre si staccano da questo tessuto per iniziare la migrazione.
Cosa succede quando l'interruttore manca
I topi privi completamente di NR6A1 muoiono nelle fasi precoci dello sviluppo, quindi il gruppo ha esaminato embrioni poco prima di questo stadio. Hanno osservato una grave carenza di cellule della cresta neurale, particolarmente dietro il primo arco che formerà parti della mascella e del collo, dove le cellule migratorie della cresta neurale erano quasi del tutto assenti. I programmi genici chiave che normalmente contrassegnano l'identità della cresta neurale e permettono alle cellule di distaccarsi e muoversi risultavano fortemente ridotti. Allo stesso tempo, i geni che mantengono le cellule in uno stato staminale altamente proliferativo restavano attivi e molte delle cellule simil-cresta neurale che si formavano morivano presto. Questi risultati indicano che senza NR6A1 le cellule neurali staminali non riescono a effettuare correttamente la transizione verso cellule migratorie della cresta neurale e non possono sopravvivere.
Spegnere la staminalità e accendere il movimento
Per capire come NR6A1 eserciti questo controllo, gli autori hanno combinato diverse tecniche molecolari potenti, tra cui sequenziamento dell'RNA a singola cellula, mappatura dell'accessibilità della cromatina e saggi mirati di legame DNA–proteina sia in cellule della cresta neurale derivate da topo sia da cellule staminali umane. Hanno scoperto che NR6A1 si lega fisicamente a motivi di DNA specifici vicino a geni che governano due programmi opposti: uno che mantiene la pluripotenza (la capacità di diventare molti tipi cellulari) e un altro che guida l'identità della cresta neurale e il movimento cellulare. Quando NR6A1 è presente, la cromatina che circonda geni della staminalità come Oct4 e Nanog diventa meno accessibile e questi geni vengono repressi, mentre regioni vicine a geni della cresta neurale e della transizione epiteliale-mesenchimale si aprono e si attivano. L'overespressione di Oct4 durante la finestra critica della formazione della cresta neurale ha riprodotto la perdita di NR6A1, mostrando ulteriormente che la staminalità deve essere silenziata affinché emergano le cellule della cresta neurale.
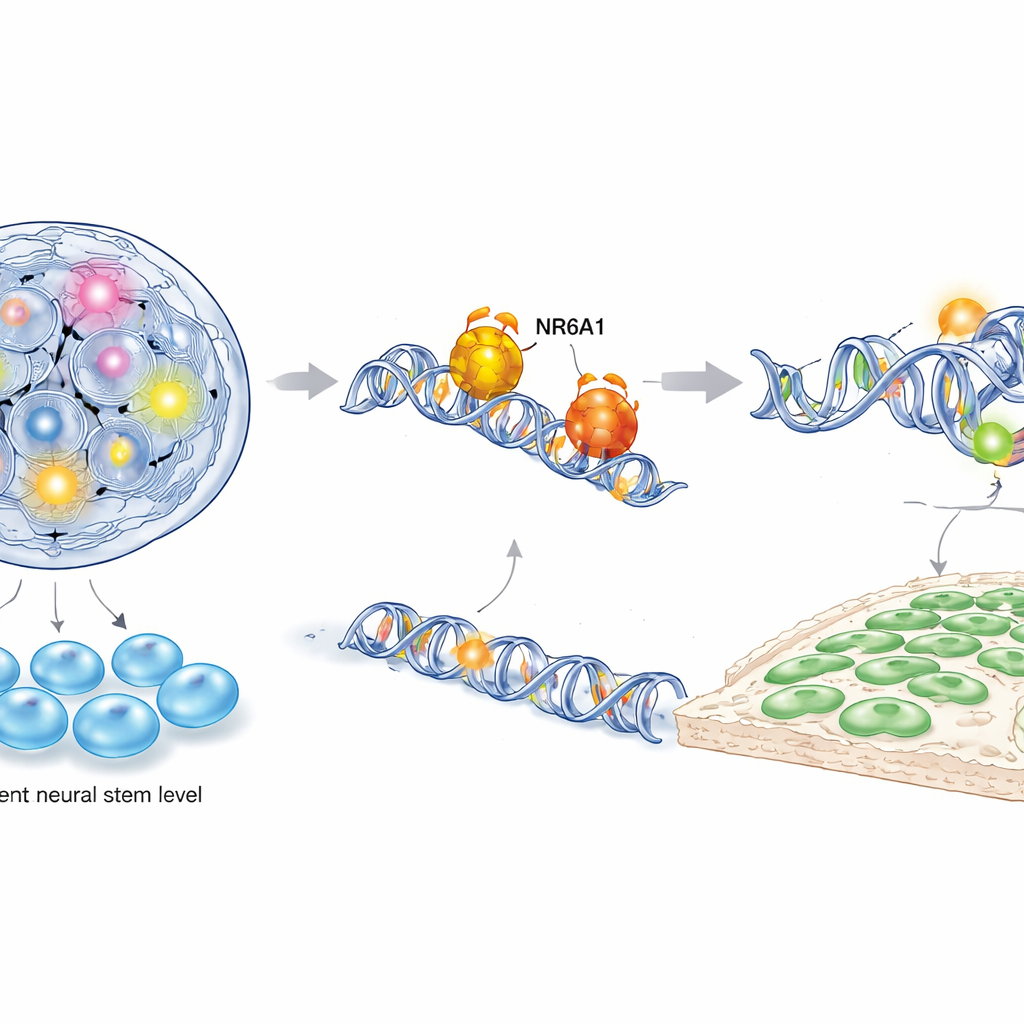
Rivedere la timeline dello sviluppo precoce
Lo studio rivede anche il calendario di quando inizia la specificazione delle cellule della cresta neurale nei mammiferi. Utilizzando un sistema genetico inducibile per rimuovere NR6A1 a diversi momenti, il team ha mostrato che cancellarlo entro la metà della gastrulazione—uno stadio precedente rispetto a quanto tradizionalmente ritenuto—era sufficiente a bloccare l'attivazione dei geni della cresta neurale. Al contrario, la delezione di NR6A1 in fasi successive, compresa l'uso di una linea driver specifica per la cresta neurale molto usata, non produceva difetti evidenti. Ciò significa che decisioni cruciali sul destino della cresta neurale vengono prese prima che quegli strumenti standard comincino a funzionare, spiegando perché alcuni studi precedenti sul topo potrebbero aver mancato requisiti precoci.
Perché questo è importante per i difetti alla nascita e le malattie
Complessivamente, il lavoro rivela NR6A1 come un coordinatore centrale che aiuta le cellule neurali staminali a "diventare adulte" trasformandosi in cellule della cresta neurale, spegnendo contemporaneamente i programmi di pluripotenza e attivando i programmi di migrazione e sopravvivenza. Questa azione duale sembra iniziare durante la metà della gastrulazione, prima di quanto fosse riconosciuto nei mammiferi, e avvicina lo sviluppo del topo a quello di altri vertebrati. Chiarendo quando e come opera questo interruttore, lo studio fornisce un quadro per reinterpretare esperimenti genetici precedenti, identificare strumenti migliori per studiare la biologia della cresta neurale e, in ultima analisi, comprendere e potenzialmente prevenire le neurocristopatie che insorgono quando questa precoce decisione dello sviluppo va storta.
Citazione: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
Parole chiave: cellule della cresta neurale, NR6A1, sviluppo embrionale, interruttore della pluripotenza, neurocristopatia