Clear Sky Science · it
Progettare il sistema MmeFz2-ωRNA per l’editing genomico efficiente tramite un quadro integrato computazionale-sperimentale
Forbici geniche più piccole per grandi problemi medici
L’editing genico ha già cambiato il modo in cui gli scienziati studiano le malattie, ma trasformarlo in una medicina sicura e praticabile resta una sfida importante. Un grande ostacolo è che le «forbici» del DNA più potenti oggi, come CRISPR-Cas9, sono fisicamente ingombranti e difficili da imballare nei minuscoli vettori di somministrazione usati nei pazienti. Questo studio presenta un nuovo strumento di editing genico compatto, costruito da una famiglia di enzimi poco nota chiamata Fanzor2, e mostra come l’intelligenza artificiale possa ridisegnarlo rapidamente in un forte candidato per future terapie genetiche.
Una nuova classe di editor genici compatti
La maggior parte degli editor genomici attuali, come Cas9 e Cas12a, sono proteine voluminose composte da oltre mille unità. Questa dimensione le rende difficili da inserire nei virus adeno-associati (AAV), il principale sistema di consegna per le terapie geniche. In confronto, le proteine Fanzor2 sono molto più piccole e si trovano naturalmente negli eucarioti, il ramo della vita che include animali e esseri umani. Gli autori si sono concentrati su un membro di questa famiglia, MmeFz2, che utilizza una breve molecola di RNA chiamata ωRNA per trovare e tagliare sequenze di DNA specifiche. Sulla carta, MmeFz2 sembrava ideale per la terapia: compatta e programmabile. In pratica, però, la sua attività nelle cellule umane era scarsa, modificando meno dell’un per cento dei siti bersaglio. Il team si è quindi posto l’obiettivo di trasformare questo enzima poco performante in uno strumento pratico.
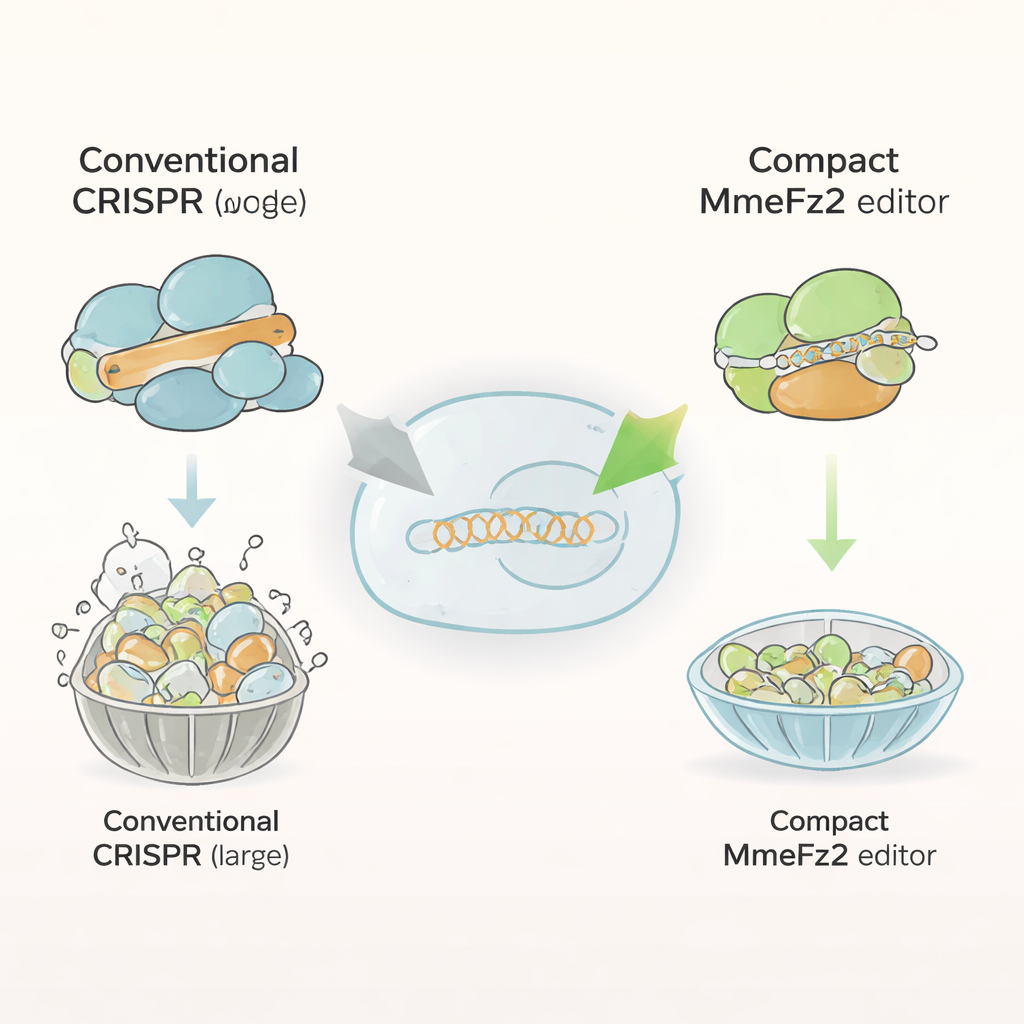
Usare l’IA per ridisegnare la molecola guida
Il primo bersaglio è stato l’ωRNA, la guida che indica a MmeFz2 dove tagliare. Usando AlphaFold3, un programma all’avanguardia che predice le strutture 3D di complessi proteina–RNA–DNA, i ricercatori hanno costruito un modello di MmeFz2 legato alla sua ωRNA e a un bersaglio di DNA. Questa struttura virtuale ha rivelato che parti dell’ωRNA erano flosci, mal appaiate e appena a contatto con la proteina. Guidato da queste informazioni, il team ha sostituito sistematicamente legami instabili nell’RNA e ha rimosso catene di uridine che possono interferire con la trascrizione. Hanno poi testato dozzine di varianti nelle cellule umane. Accumulando le migliori modifiche e accorciando una regione di stelo non necessaria, hanno creato un ωRNA accorciato del 30% ma in grado di fornire quasi un miglioramento di 20 volte nell’efficienza di editing su molti siti di DNA.
Affinare la proteina con il machine learning
Successivamente, il team ha raffinato la proteina stessa. Hanno nuovamente usato AlphaFold3 per mappare i punti di contatto di MmeFz2 con RNA e DNA e hanno progettato oltre cento singole sostituzioni di amminoacidi mirate a rafforzare quei contatti o a migliorare la flessibilità. Dopo averle scremate nelle cellule, hanno inserito i dati di performance in EVOLVEpro, un sistema di apprendimento automatico basato su modelli linguistici per proteine addestrati su milioni di sequenze naturali. Questo strumento ha imparato quali caratteristiche tendevano ad aumentare l’attività e ha suggerito nuove combinazioni di mutazioni previste più efficaci. Attraverso alcuni cicli di questo loop computazionale–sperimentale, gli scienziati sono arrivati a due varianti ottimizzate dell’enzima che, abbinate all’ωRNA migliorato, hanno aumentato l’attività di editing più di 60 volte rispetto al sistema di partenza.
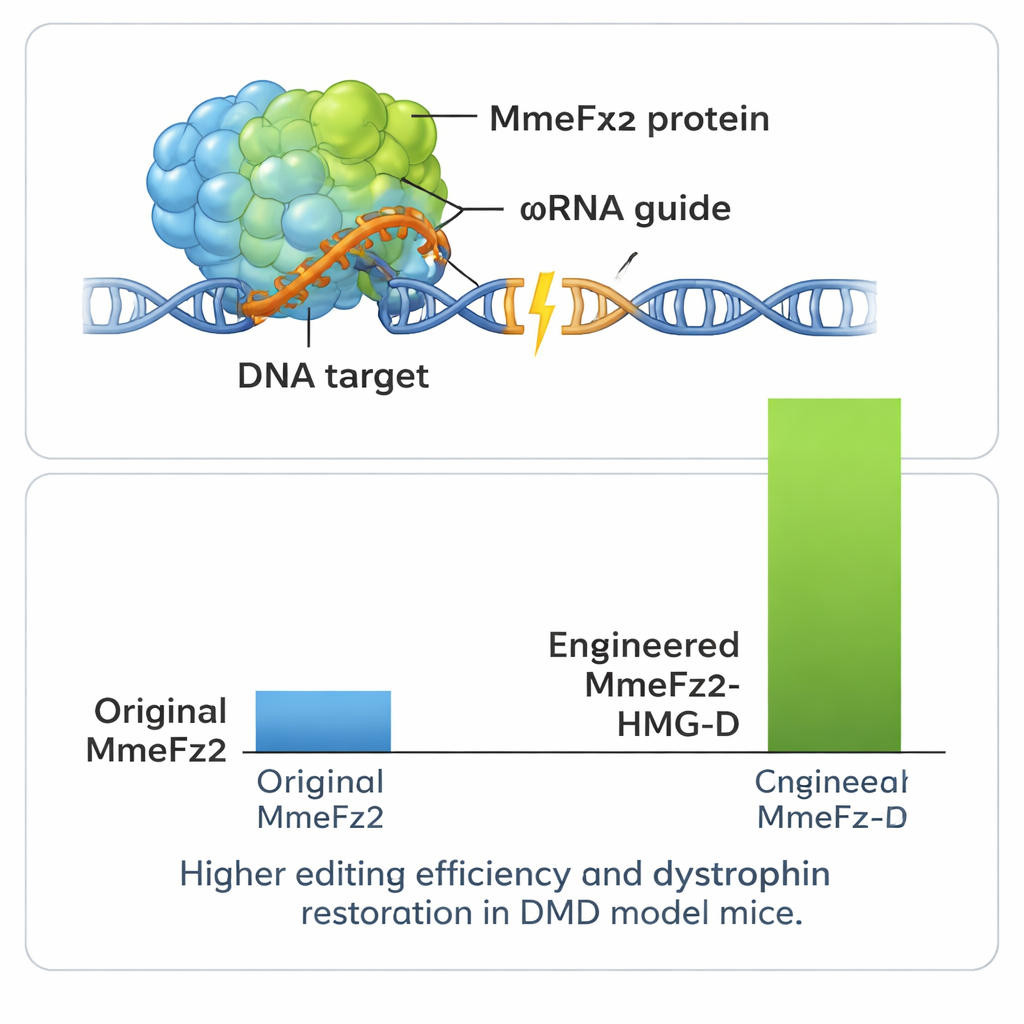
Potenziare l’efficacia e testare in un modello di malattia
Per ottenere ancora più prestazioni dal sistema, gli autori hanno fuso MmeFz2 con piccoli domini leganti il DNA che aiutano le proteine ad ancorarsi al materiale genetico. Uno di questi, chiamato HMG-D, si è dimostrato particolarmente efficace quando attaccato all’estremità dell’enzima ingegnerizzato, producendo livelli di editing superiori all’80% in alcuni siti. È importante che i test sui siti genomici predetti come off-target abbiano mostrato che questa potenza aggiunta non comportava una perdita significativa di precisione. Poiché l’intero editor genico — proteina e RNA guida — è così compatto, entra comodamente in un singolo vettore AAV, cosa non possibile per la maggior parte dei sistemi CRISPR. Il team ha sfruttato questo vantaggio in un modello murino di distrofia muscolare di Duchenne, una malattia letale che provoca degenerazione muscolare dovuta a errori nel gene della distrofina. Una singola iniezione dell’editor veicolato da AAV nel muscolo della zampa ha portato a correzioni rilevabili dell’RNA del gene e ha ripristinato la proteina distrofina in una frazione sostanziale delle fibre muscolari.
Cosa significa per le future terapie geniche
Per chi non è specialista, il messaggio chiave è che gli autori hanno trasformato un enzima di taglio genico debole e oscuro in un editor compatto e ad alte prestazioni che può essere consegnato in un unico pacchetto virale e può riparare una grave malattia genetica in un modello animale realistico. Altrettanto importante è il modo in cui ci sono riusciti: combinando strettamente predizione strutturale basata sull’IA e machine learning con test di laboratorio mirati, hanno migliorato sia la proteina sia la sua RNA guida molto più efficacemente rispetto ai tradizionali approcci di prova-errore. Questa strategia integrata potrebbe accelerare la creazione di molti editor genomici di nuova generazione, avvicinando terapie geniche più precise e sicure a pazienti con distrofia muscolare e altre malattie ereditarie.
Citazione: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
Parole chiave: editing genico, alternative al CRISPR, distrofia muscolare di Duchenne, terapia genica virale, intelligenza artificiale in biologia