Clear Sky Science · it
La clearance dipendente da C1q della alfa-sinucleina consente ai macrofagi di limitare transitoriamente la sinucleinopatia enterica nei topi maschi
Perché l’intestino conta nelle malattie cerebrali
La malattia di Parkinson è più nota per i tremori e i problemi motori, ma molte persone sperimentano anni di grave stipsi e altri disturbi intestinali prima che compaiano sintomi motori. Questo studio esplora cosa accade nel “secondo cervello” del corpo — la rete nervosa nell’intestino — quando una proteina legata al Parkinson si ripiega in modo anomalo lì, e come le cellule immunitarie locali inizialmente aiutino, poi cedano. Comprendere questa battaglia precoce nell’intestino potrebbe aprire nuove strade per alleviare i sintomi e forse rallentare la progressione della malattia molto prima che il cervello sia gravemente danneggiato.
Una proteina problematica nel secondo cervello del corpo
Nella malattia di Parkinson e in disturbi correlati, una proteina chiamata alfa-sinucleina può ripiegarsi male e aggregarsi in ammassi tossici. Questi aggregati si trovano non solo nel cervello ma anche in tutto il sistema nervoso enterico, la rete di neuroni che controlla il movimento intestinale. Molti ricercatori sospettano che, in almeno alcuni pazienti, l’alfa-sinucleina mal ripiegata possa iniziare nell’intestino e poi propagarsi verso il cervello lungo vie nervose. Gli autori hanno usato un modello murino in cui fibrille preformate di alfa-sinucleina vengono iniettate nello stomaco e nella prima parte dell’intestino tenue. Nelle successive due mesi hanno osservato un aumento costante di alfa-sinucleina anomala, marcata chimicamente, all’interno dei neuroni intestinali. Questo accumulo coincideva con un rallentamento del transito intestinale e una ridotta produzione di feci, rispecchiando la stitichezza osservata in molte persone con Parkinson.
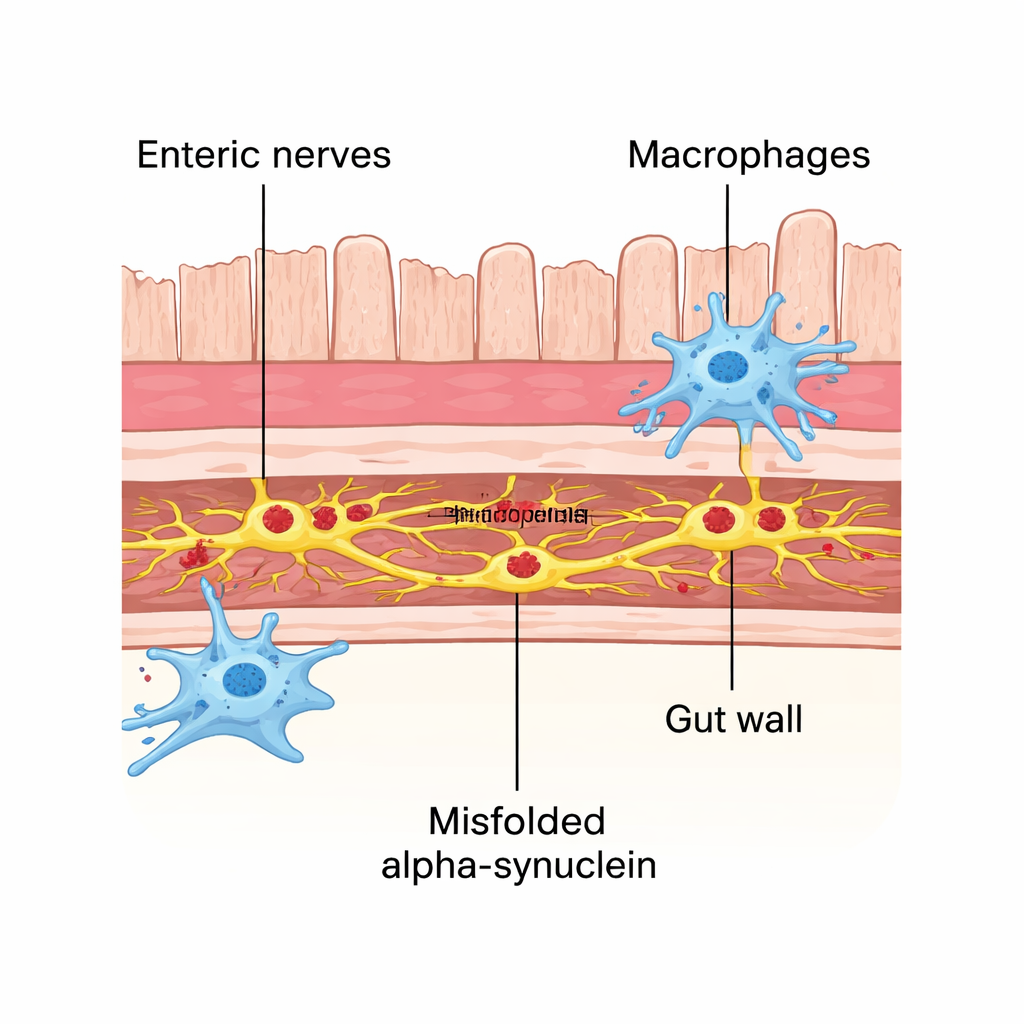
Le cellule immunitarie intestinali entrano in gioco come prime risposte
La parete intestinale contiene cellule immunitarie residenti chiamate macrofagi che comunicano costantemente con i neuroni vicini e contribuiscono a mantenere il tessuto in buona salute. In questo modello, questi macrofagi hanno fatto più che reagire al danno: hanno contattato fisicamente i gruppi neuronali colpiti più spesso e ospitavano piccole punteggiature della proteina mal ripiegata al loro interno. Quando i ricercatori hanno depletato questi macrofagi con un trattamento a base di anticorpi, la patologia da alfa-sinucleina nei neuroni enterici è aumentata in modo significativo. Ciò suggerisce che i macrofagi intestinali svolgono un ruolo protettivo precoce, agendo come spazzini cellulari che inglobano e rimuovono la proteina tossica dalle cellule nervose vicine prima che possa diffondersi.
Un marcatore molecolare che aiuta — e danneggia
Per capire come queste cellule immunitarie riconoscano ciò che devono rimuovere, il gruppo si è rivolto al sequenziamento RNA a singola cellula, profilando migliaia di singole cellule immunitarie intestinali. Hanno identificato sottotipi specifici di macrofagi negli strati muscolari dell’intestino che attivavano geni legati all’inglobamento e alla degradazione proteica, in particolare componenti del sistema del complemento — una via di marcatura molecolare più nota a livello ematico. Un attore chiave, C1q, risultava altamente attivo in questi macrofagi intestinali. Al microscopio, C1q rivestiva i neuroni enterici colpiti, e i macrofagi contenevano punteggiature positive sia per C1q sia per l’alfa-sinucleina mal ripiegata, indicando che C1q aiuta a etichettare la proteina tossica per la rimozione. Quando gli scienziati hanno usato topi geneticamente privi di C1q, la patologia neuronale da alfa-sinucleina è peggiorata e i macrofagi hanno internalizzato meno ammassi proteici. Eppure, sorprendentemente, questi topi privi di C1q mostravano una motilità intestinale leggermente migliore rispetto ai topi normali esposti alle stesse fibrille, il che implica che lo stesso processo che rimuove la proteina tossica può anche disturbare la funzione intestinale — probabilmente tagliando o indebolendo connessioni nervose che controllano il movimento.
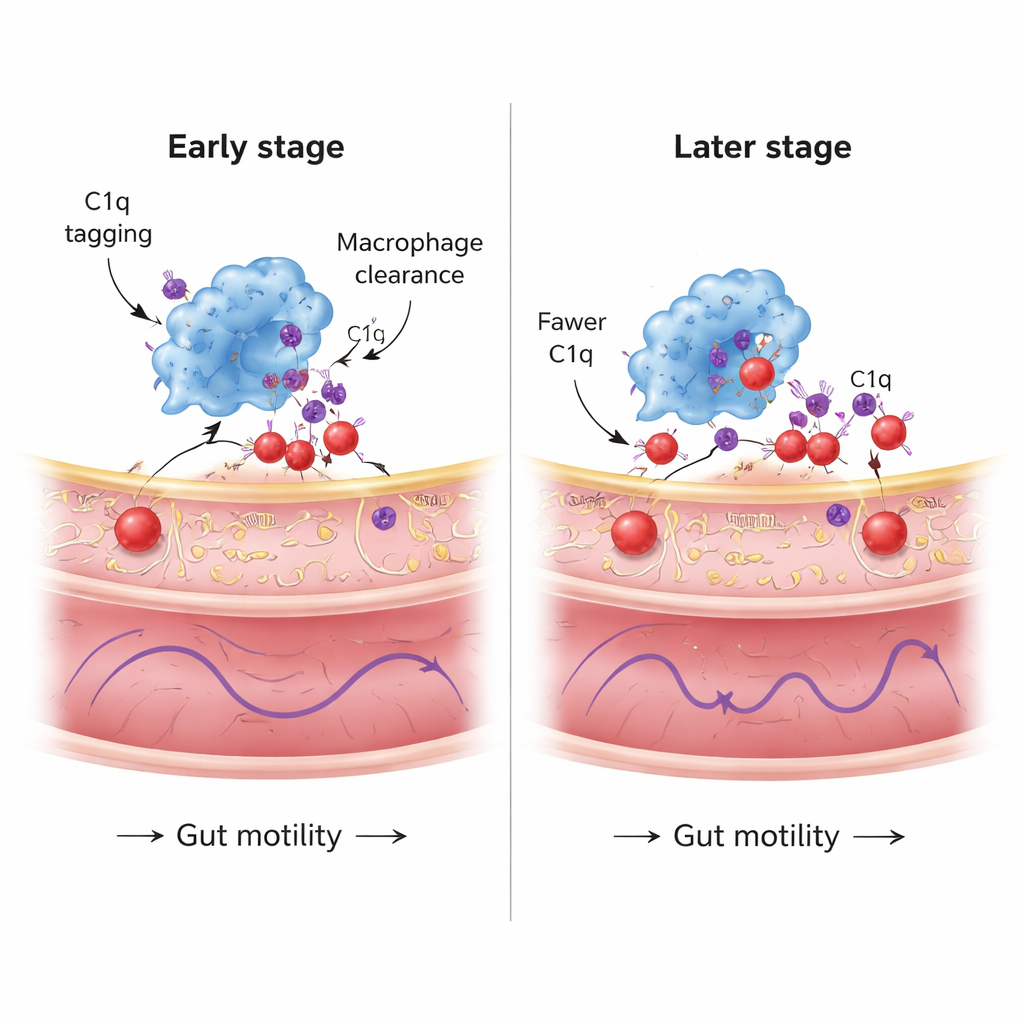
Un sistema protettivo che svanisce col tempo
Lo studio ha anche seguito questa risposta di pulizia su un periodo più lungo. Circa un mese dopo l’introduzione dell’alfa-sinucleina, i macrofagi mostravano una robusta espressione di C1q e molte punteggiature di proteina marcata da C1q all’interno dei loro corpi cellulari, e C1q decorava abbondantemente i neuroni enterici. Dopo due mesi, tuttavia, sebbene i livelli complessivi di C1q nei macrofagi rimanessero, il numero di punteggiature internalizzate C1q/alfa-sinucleina e la quantità di C1q depositata sui neuroni erano diminuite. Allo stesso tempo, la patologia neuronale nell’intestino continuava ad aumentare. Le analisi geniche suggerivano che l’assunzione continua di proteina mal ripiegata sovraccarica la macchina cellulare dei macrofagi per la gestione delle proteine, attivando vie di stress correlate a proteine mal ripiegate, lisosomi e persino morte cellulare. In altre parole, la capacità protettiva dei macrofagi sembra essere finita: inizialmente contengono la patologia, ma man mano che lo stress si accumula, la loro abilità di eliminare l’alfa-sinucleina diminuisce.
Cosa significa per il Parkinson e l’intestino
Il lavoro offre un quadro sfumato di come le cellule immunitarie intestinali modellino i cambiamenti intestinali simili al Parkinson nelle fasi iniziali. All’inizio, i macrofagi residenti aiutano usando C1q per etichettare e ingerire l’alfa-sinucleina mal ripiegata dai neuroni enterici, limitandone la diffusione. Ma la stessa potatura indotta dal complemento può compromettere la trasmissione nervosa e rallentare l’intestino, contribuendo alla stipsi. Col tempo, il sistema di clearance dei macrofagi, appesantito dallo stress, si indebolisce, permettendo l’accumulo di maggiore patologia anche quando funzione intestinale e coinvolgimento cerebrale divergono. Per i pazienti, questo suggerisce che modulare l’attività dei macrofagi o la segnalazione del complemento nell’intestino — con l’obiettivo di potenziare una clearance sicura evitando una perdita eccessiva di sinapsi — potrebbe un giorno essere una strategia per trattare o prevenire i sintomi intestinali legati al Parkinson e forse influenzare il corso più ampio della malattia.
Citazione: Mackie, P.M., Koshy, J.M., Bhogade, M.H. et al. C1q-dependent clearance of alpha-synuclein allows macrophages to transiently limit enteric synucleinopathy in male mice. Nat Commun 17, 1877 (2026). https://doi.org/10.1038/s41467-026-68641-8
Parole chiave: Malattia di Parkinson, sistema nervoso enterico, alfa-sinucleina, cellule immunitarie intestinali, complemento C1q