Clear Sky Science · it
Nanorobot camuffati mirano e regolano i modelli di comunicazione tra organelli subcellulari dei macrofagi per promuovere la rigenerazione neurale
Perché i piccoli aiutanti "camuffati" sono importanti per le lesioni del midollo spinale
La lesione del midollo spinale spesso comporta una paralisi permanente perché il tessuto nervoso danneggiato è estremamente difficile da riparare. Una ragione principale è che il sito della lesione diventa una zona ostile piena di infiammazione e stress cellulare che ostacolano la guarigione. Questo studio descrive un nuovo tipo di nanorobot camuffato che viaggia nel flusso sanguigno, elude le difese dell’organismo e riprogramma le cellule immunitarie nel sito della lesione per passare da una modalità aggressiva a una modalità riparativa, aiutando i nervi a ricrescere in animali con danno spinale.
Il problema: un’infiammazione che non si spegne
Dopo una lesione del midollo spinale, la prima ondata di danno deriva dal trauma fisico stesso. Ma una seconda, più lenta, ondata è guidata dall’infiammazione, da molecole tossiche chiamate specie reattive dell’ossigeno e da una diffusa morte cellulare. Le cellule immunitarie note come macrofagi accorrono per ripulire i detriti. All’inizio assumono uno stato aggressivo «M1» che uccide patogeni e cellule danneggiate ma rilascia anche segnali infiammatori intensi. Perché la vera guarigione abbia inizio, queste stesse cellule devono poi spostarsi in uno stato calmante «M2» che supporta la riparazione tessutale, la crescita dei vasi sanguigni e la rigenerazione nervosa. Sfortunatamente lo stress intenso nei tessuti lesionati può intrappolare i macrofagi nello stato M1 dannoso, instaurando un ciclo di infiammazione cronica che impedisce il recupero funzionale.
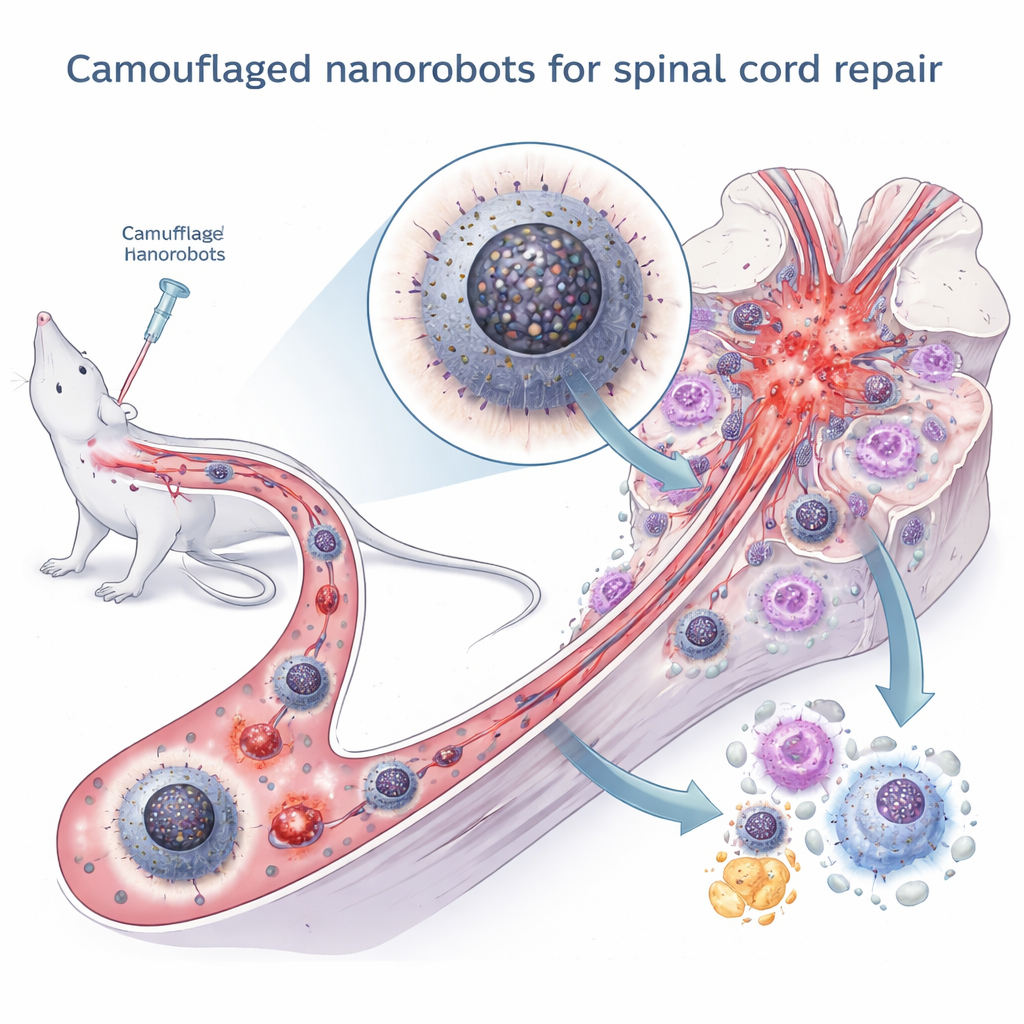
Conversazione nascosta tra parti della cellula
Gli autori si sono concentrati su una «conversazione» interna sottile ma cruciale dentro i macrofagi: il dialogo tra due compartimenti chiave, il reticolo endoplasmatico (che aiuta a ripiegare le proteine e immagazzina il calcio) e i mitocondri (le centrali energetiche della cellula). In condizioni normali queste strutture condividono piccole quantità di ioni calcio attraverso zone di contatto specializzate, contribuendo a far corrispondere la produzione energetica alle necessità cellulari. Dopo la lesione, però, l’eccesso di specie reattive dell’ossigeno provoca il malripiegamento delle proteine e stress nel reticolo endoplasmatico. Questo stress, a sua volta, guida un trasferimento eccessivo di calcio nei mitocondri, portando al collasso energetico, alla formazione di ulteriori molecole tossiche e alla fuga del DNA mitocondriale nel fluido intracellulare. Quel DNA fuoriuscito attiva una potente via d’allarme chiamata cGAS–STING–NFκB, che rinchiude ulteriormente i macrofagi nello stato infiammatorio M1.
Progettare un nanorobot camuffato
Per spezzare questo circolo vizioso, il gruppo ha costruito un nanorobot multilivello chiamato BP@D/N. Al suo nucleo ci sono punti quantici di fosforo nero, particelle minuscole con forte attività antiossidante e antinfiammatoria ma scarsa stabilità nell’organismo. Questi punti sono racchiusi in un guscio cavo di polidopamina, un materiale biocompatibile che li protegge dalla degradazione precoce e aggiunge proprie proprietà antiossidanti. Infine l’intero nanoparticella è avvolta in una membrana prelevata da neutrofili attivati, un tipo di globulo bianco naturalmente attratto dai siti di infiammazione. Questo «mantello» permette al nanorobot di eludere la clearance immunitaria, seguire i segnali infiammatori fino al midollo spinale lesionato e aderire ai macrofagi per un’efficiente captazione.
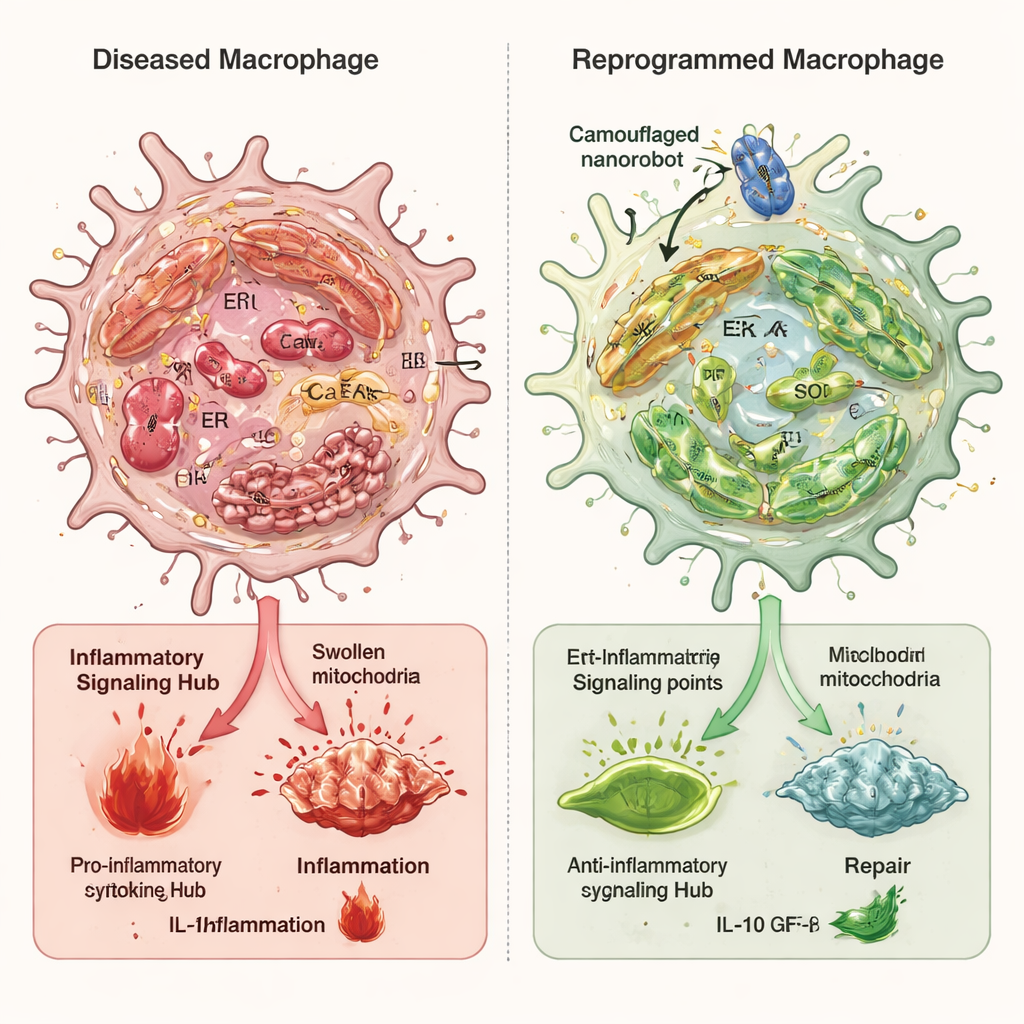
Riprogrammare le cellule immunitarie stressate
Negli studi cellulari, i macrofagi esposti a stimoli infiammatori mostravano alti livelli di stress del reticolo endoplasmatico, mitocondri gonfi e danneggiati, sovraccarico di calcio e forte attivazione della via d’allarme cGAS–STING–NFκB. Trattati con i nanorobot camuffati, lo stress ossidativo complessivo è diminuito nettamente, le membrane interne tra reticolo endoplasmatico e mitocondri sono risultate meno iperconnesse e il calcio mitocondriale è tornato verso valori più normali. Questo ha impedito la fuoriuscita del DNA mitocondriale nel fluido intracellulare e ha attenuato la cascata di segnalazione infiammatoria. Un attore chiave in questo processo è stato un enzima chiamato Ero1α, che contribuisce a controllare l’ambiente ossidativo e il rilascio di calcio dal reticolo endoplasmatico. I nanorobot hanno ridotto l’attività di Ero1α e quando i ricercatori hanno aumentato artificialmente Ero1α, ciò ha in gran parte annullato i benefici del nanorobot, confermando il suo ruolo centrale.
Dal calmare l’infiammazione alla rigenerazione dei nervi
Questi cambiamenti interni hanno fatto sì che i macrofagi passassero dallo stato distruttivo M1 allo stato riparativo M2. In coltura, le cellule polarizzate verso M2 secernevano meno molecole infiammatorie come TNF-α e IL-6 e più fattori di crescita che incoraggiano i neuroni e le cellule di supporto a crescere e allungare gli assoni. In modelli di ratto con lesione del midollo spinale, iniezioni ripetute dei nanorobot hanno ridotto i segnali immunitari dannosi nella lesione, diminuito la formazione di cicatrici, ridotto la formazione di cavità e aumentato le fibre nervose in rigenerazione. Gli animali trattati con i nanorobot camuffati hanno recuperato movimenti posteriori migliori, risposte muscolari più forti e una struttura vescicale migliorata rispetto agli animali non trattati o a quelli ricevuti nanoparticelle meno mirate.
Che cosa potrebbe significare per i pazienti futuri
Questo lavoro mostra che sintonizzare con precisione lo stress interno e la comunicazione tra compartimenti cellulari può trasformare le cellule immunitarie da dannose a favorevoli per i nervi danneggiati. Impacchettando particelle antiossidanti potenti ma fragili in un nanorobot camuffato e mirato, i ricercatori hanno restaurato un equilibrio più sano tra infiammazione e riparazione nel midollo spinale lesionato dei ratti. Pur restando molto da fare prima che questo approccio possa essere testato nell’uomo, offre un progetto promettente: invece di sopprimere l’infiammazione in modo ampio, le terapie future potrebbero orientare specifiche macchine cellulari all’interno dei macrofagi per creare un ambiente più accogliente alla rigenerazione neurale dopo una lesione del midollo spinale.
Citazione: Guo, Q., Wang, W., Jiang, X. et al. Camouflaged nanorobots target and regulate macrophage subcellular organelle crosstalk patterns to promote neural regeneration. Nat Commun 17, 1952 (2026). https://doi.org/10.1038/s41467-026-68636-5
Parole chiave: lesione del midollo spinale, nanorobot, macrofagi, rigenerazione neurale, nanomedicina