Clear Sky Science · it
Caratterizzazione metabolica delle interazioni tumore-immunità tramite immunofluorescenza multiplex che rivela meccanismi spaziali di risposta all’immunoterapia nel carcinoma polmonare non a piccole cellule (NSCLC)
Perché questa ricerca è importante
L’immunoterapia ha trasformato il trattamento per alcuni pazienti con cancro polmonare avanzato, tuttavia la maggior parte dei pazienti vede ancora la progressione della malattia nonostante questi farmaci potenti. Questo studio pone una domanda semplice ma cruciale: possiamo esaminare più da vicino il tessuto tumorale stesso — dove si trovano le diverse cellule e quanta energia consumano — per prevedere chi trarrà realmente beneficio dall’immunoterapia? Trasformando minuscoli campioni bioptici in mappe cellulari dettagliate, i ricercatori puntano ad avvicinare la cura del cancro polmonare a un approccio veramente personalizzato.
Esplorare i tumori polmonari come una mappa cittadina
Il gruppo ha analizzato tessuto proveniente da 55 persone con carcinoma polmonare non a piccole cellule (NSCLC) avanzato trattate con inibitori dei checkpoint immunitari, una classe principale di farmaci immunoterapici. Prima del trattamento, i loro campioni tumorali sono stati colorati con un pannello di 44 marker usando immunofluorescenza multiplex, permettendo di visualizzare molti antigeni contemporaneamente. Un sistema di deep learning ha poi identificato i tipi cellulari chiave — come cellule tumorali, cellule T, cellule B, macrofagi e fibroblasti — e ha classificato il loro stato funzionale (per esempio attivate, in divisione o esauste) così come il loro profilo metabolico, ossia come producevano e utilizzavano energia. Invece di limitarsi a contare le cellule, i ricercatori hanno anche mappato la posizione relativa delle cellule, creando regioni simili a quartieri all’interno di ogni biopsia.
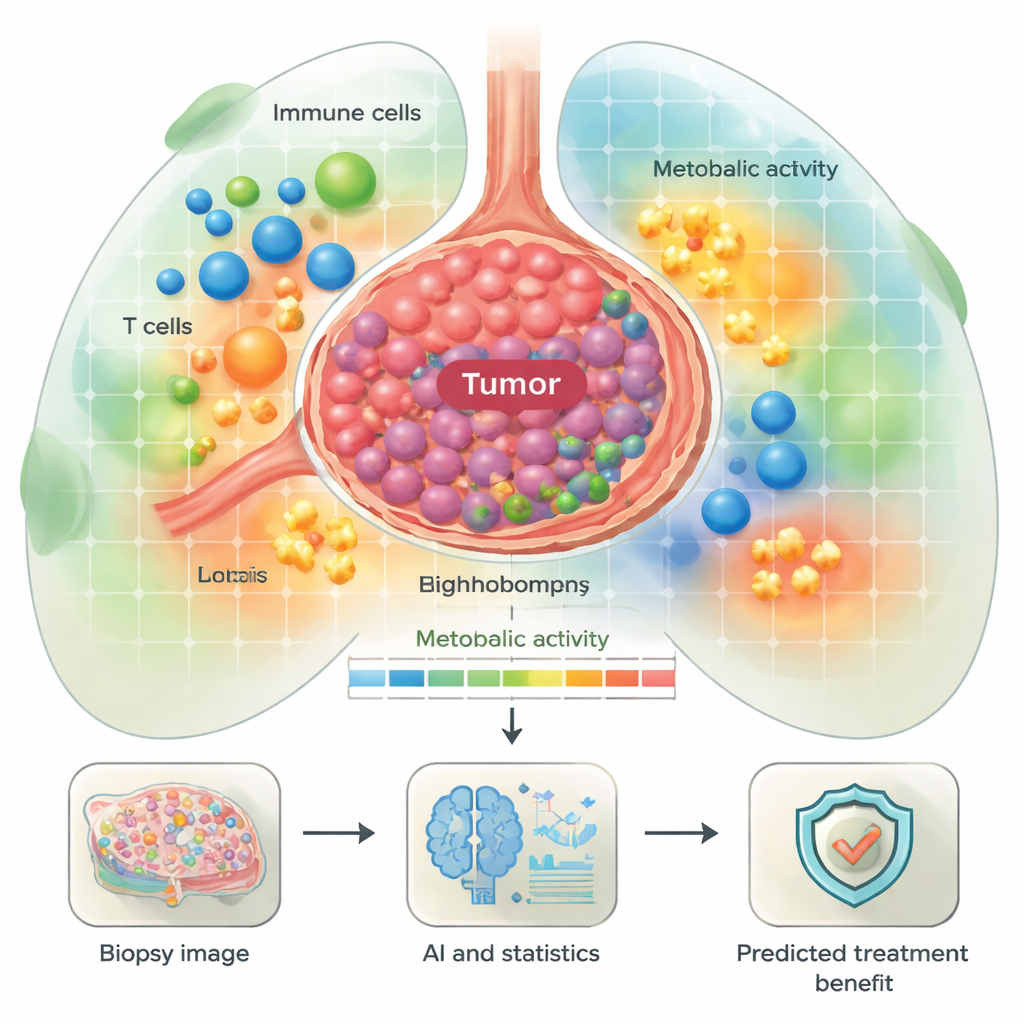
Tumori ad alto consumo energetico e il loro contesto immunitario
Un tema centrale è stato il metabolismo — i modi in cui le cellule generano carburante per crescere o combattere le malattie. I ricercatori hanno definito “quartieri metabolici” con diversi livelli e tipi di attività energetica, da zone a bassa attività a aree altamente attive ricche di fosforilazione ossidativa e glicolisi. Hanno osservato che sia le cellule tumorali sia alcune cellule immunitarie, come i macrofagi, spesso esprimevano vie energetiche forti. Alcuni di questi pattern si sono collegati agli esiti dei pazienti. Per esempio, i tumori con alta attività in vie che consentono l’utilizzo di amminoacidi e l’attivazione del ciclo di Krebs tendevano ad appartenere a pazienti che recidivavano precocemente dopo l’immunoterapia. Al contrario, alcune plasmacellule (cellule B produttrici di anticorpi) con vie energetiche attive all’interno del tumore erano più comuni nei pazienti con esiti migliori, suggerendo che non tutte le cellule energeticamente attive sono dannose — alcune possono sostenere un’immunità anti-tumorale efficace.
Attori immunitari favorevoli e sfavorevoli nel paesaggio tumorale
Oltre alla semplice abbondanza, contava anche il tipo e il comportamento delle cellule immunitarie. I macrofagi che esprimevano la molecola citotossica granzyme B erano fortemente associati a una peggiore sopravvivenza libera da progressione, specialmente quando si trovavano in quartieri metabolicamente a bassa attività o inattivi. Queste regioni possono rappresentare aree povere di nutrienti o dormienti dove l’attacco immunitario è attenuato. Al contrario, certe disposizioni di cellule T regolatorie (Treg) e fibroblasti al confine tra tumore e tessuto circostante sembravano collegate a esiti migliori, forse riflettendo un modello in cui le cellule soppressive sono mantenute ai margini piuttosto che infiltrare profondamente il tumore. I rapporti tra diversi tipi di cellule immunitarie, come granulociti e cellule T CD8, risultavano anch’essi correlati alla risposta, sottolineando che l’equilibrio immunitario e la posizione sono importanti, non solo il numero totale di cellule.
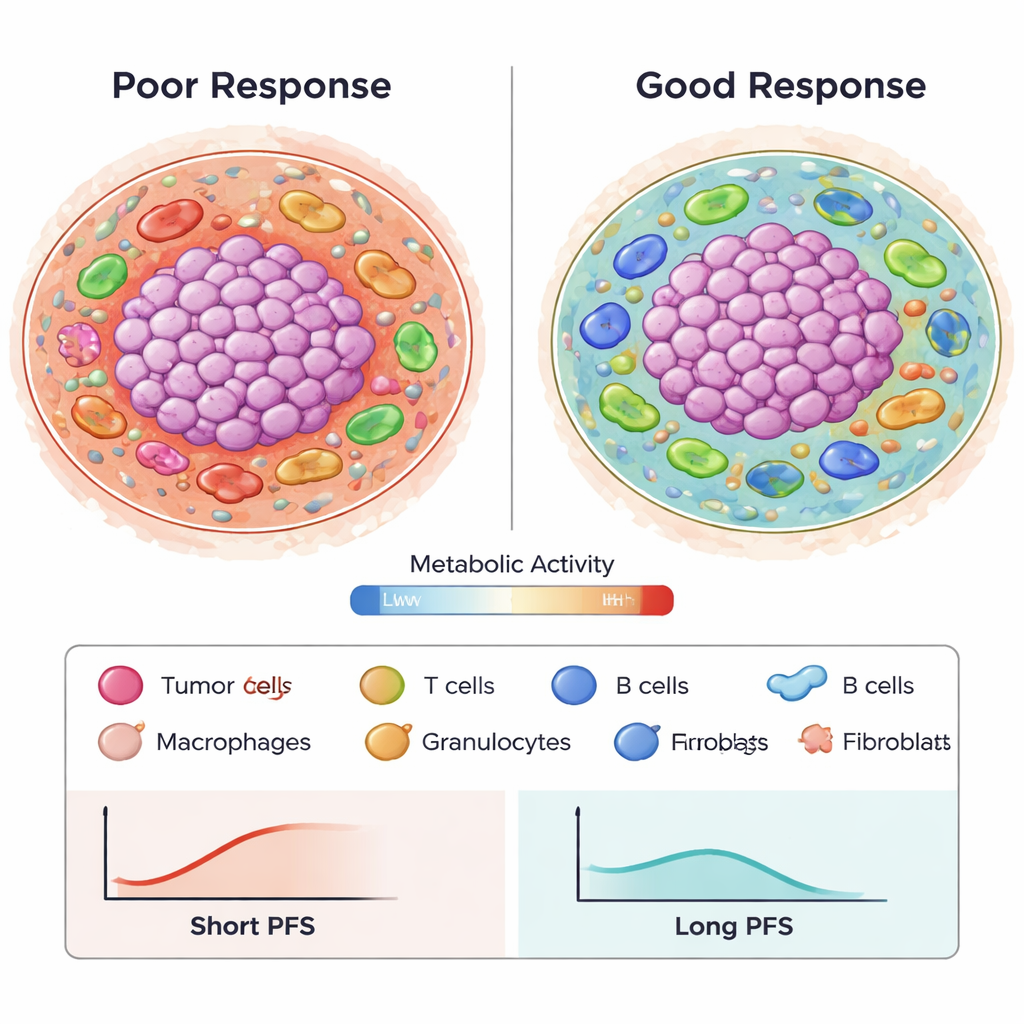
Dalle immagini complesse a pattern predittivi
Per interpretare oltre un milione di caratteristiche spaziali ingegnerizzate descriventi tipi cellulari, distanze e stati metabolici, gli autori hanno utilizzato un avanzato metodo di selezione delle feature (Stabl) e strumenti di modellizzazione della sopravvivenza. Hanno identificato 87 caratteristiche chiave, molte delle quali riflettevano come le cellule tumorali metabolicamente attive interagiscono con macrofagi e cellule T, o come specifici tipi cellulari immunitari si raggruppano vicino a vasi sanguigni e fibroblasti. Utilizzando queste caratteristiche in modelli di regressione di Cox, hanno costruito un predittore che stimava la sopravvivenza libera da progressione con un’accuratezza (AUC) intorno a 0,8 su 24 mesi, superando marcatori tradizionali singoli come la colorazione per PD-L1 o il carico mutazionale tumorale riportati in studi precedenti. È importante che diverse caratteristiche siano risultate riproducibili in due coorti indipendenti di pazienti, suggerendo che i pattern non sono semplicemente rumore casuale.
Cosa significa per i pazienti
Per un lettore non specialista, il messaggio principale è che la posizione delle cellule in un tumore polmonare e il modo in cui si alimentano possono aiutare a spiegare perché alcuni pazienti rispondono bene all’immunoterapia mentre altri no. Questo studio mostra che informazioni spaziali e metaboliche ricche, ricavate da una biopsia di routine e combinate con intelligenza artificiale e modellistica statistica, possono rivelare firme di probabile beneficio o resistenza. Pur richiedendo convalide in gruppi più ampi e in sezioni di tessuto intero, indica una strada verso test futuri che potrebbero dire ai medici, prima dell’inizio del trattamento, quali pazienti sono più propensi a ottenere un controllo durevole dall’immunoterapia e quali potrebbero necessitare di strategie alternative o in combinazione.
Citazione: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
Parole chiave: resistenza all’immunoterapia, carcinoma polmonare non a piccole cellule, microambiente tumorale, biologia spaziale, metabolismo del cancro