Clear Sky Science · it
H3K9me2 mediato da G9a orchestra la rigenerazione epiteliale intestinale attraverso il silenziamento epigenetico di geni correlati al ciclo cellulare
Perché la riparazione intestinale è importante
Ogni giorno il rivestimento dell’intestino è esposto a condizioni difficili: acidi gastrici, particelle di cibo e trilioni di microrganismi. Eppure questo tessuto non solo sopravvive, ma si ripara costantemente. Quando quel sistema di riparazione fallisce — dopo radioterapia, nella malattia infiammatoria intestinale o durante infezioni gravi — le persone possono soffrire dolore, emorragie e complicazioni potenzialmente letali. Questo studio scopre un “interruttore” nascosto all’interno delle cellule intestinali che le aiuta a decidere quando smettere di restare inattive e iniziare a ricostruire, offrendo indizi per nuovi trattamenti che potrebbero potenziare la naturale capacità di riparazione dell’intestino.
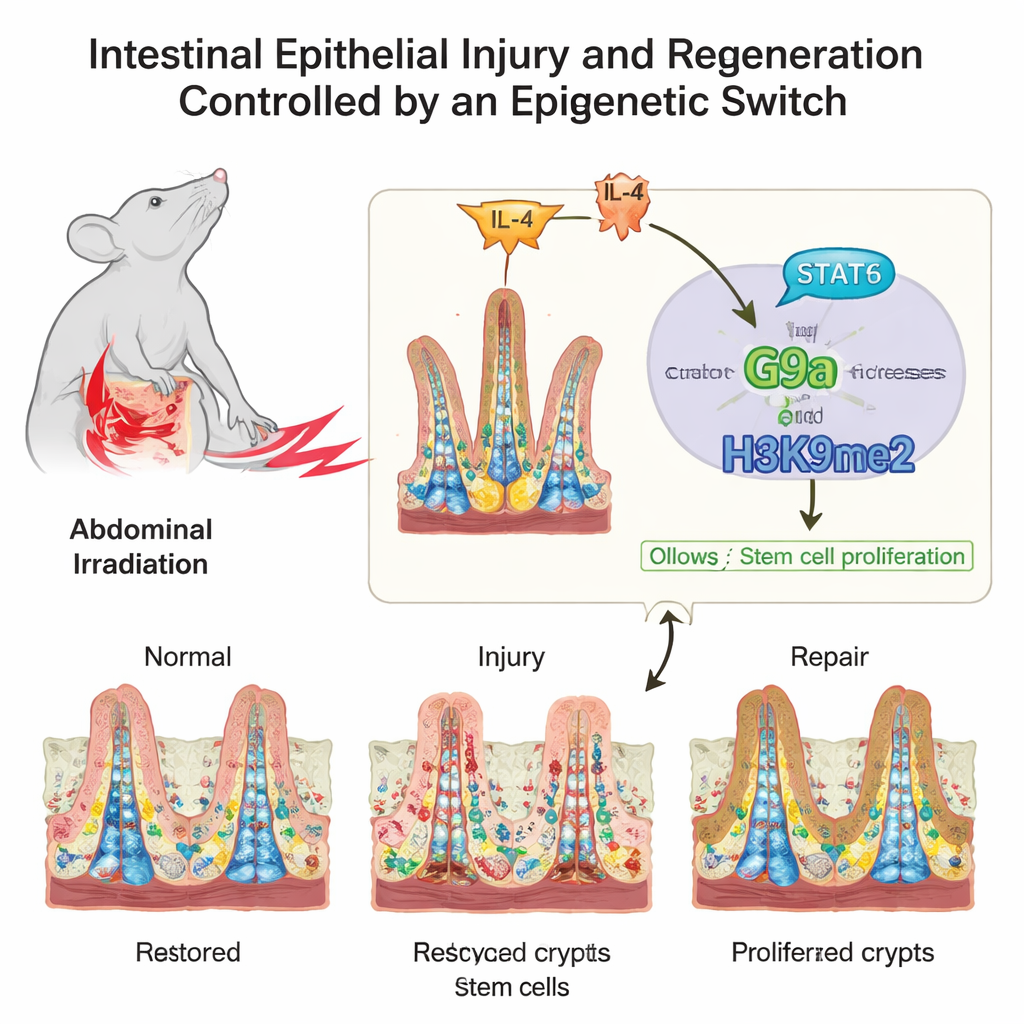
Un’architettura delicata sotto stress costante
La superficie interna dell’intestino al microscopio assomiglia a un tappeto morbido, con villi a forma di dito che assorbono i nutrienti e tasche chiamate cripte dove risiedono le cellule staminali. Queste cellule staminali e le loro figlie a rapida divisione devono trovare un equilibrio tra rinnovamento ordinario e riparazione d’emergenza. Gli autori si sono concentrati su come i tag chimici sulle proteine che impacchettano il DNA, chiamate istoni, influenzino questo equilibrio. Questi tag non modificano i geni in sé, ma funzionano più come dimmer, aumentando o diminuendo l’attività di gruppi di geni mentre l’intestino passa dalla vita normale al danno e poi ritorna alla salute.
Un marchio epigenetico che segue danno e guarigione
Usando topi esposti a radiazioni — una causa comune di danno intestinale durante il trattamento del cancro — i ricercatori hanno analizzato diversi marchi istonici nelle cripte ricche di cellule staminali. Un marchio, noto come H3K9me2, aumentava bruscamente quando l’intestino passava dal danno alla fase di riparazione. Anche l’enzima che lo scrive, una proteina chiamata G9a, mostrava lo stesso andamento. Il gruppo ha quindi esaminato campioni umani di pazienti sottoposti a radioterapia pelvica, così come persone con malattia di Crohn. In entrambi i casi, livelli più elevati di H3K9me2 e di G9a nelle cellule intestinali correllavano con migliori segni di riparazione tissutale, suggerendo che questo sistema è conservato tra topo e uomo.
Quando l’interruttore della riparazione si guasta
Per verificare se questo marchio fosse un semplice spettatore o guidasse davvero la guarigione, gli scienziati hanno rimosso G9a specificamente dal rivestimento intestinale dei topi o ne hanno bloccato l’attività con un farmaco. In entrambi i casi i livelli di H3K9me2 diminuivano. Dopo radiazioni o danno chimico, questi topi perdevano più peso, avevano intestini più corti e più danneggiati e mostravano meno cripte rigeneranti e cellule staminali rispetto agli animali normali. Anche in assenza di lesioni deliberate, il rivestimento intestinale dei topi privi di G9a appariva povero: le cripte erano meno profonde, i villi più corti e diminuivano il numero di cellule staminali e dei loro discendenti specializzati. Piccoli “mini-intestini” coltivati da queste cellule in vitro crescevano male, sottolineando che questo sistema molecolare è centrale per il rinnovo quotidiano dell’intestino.
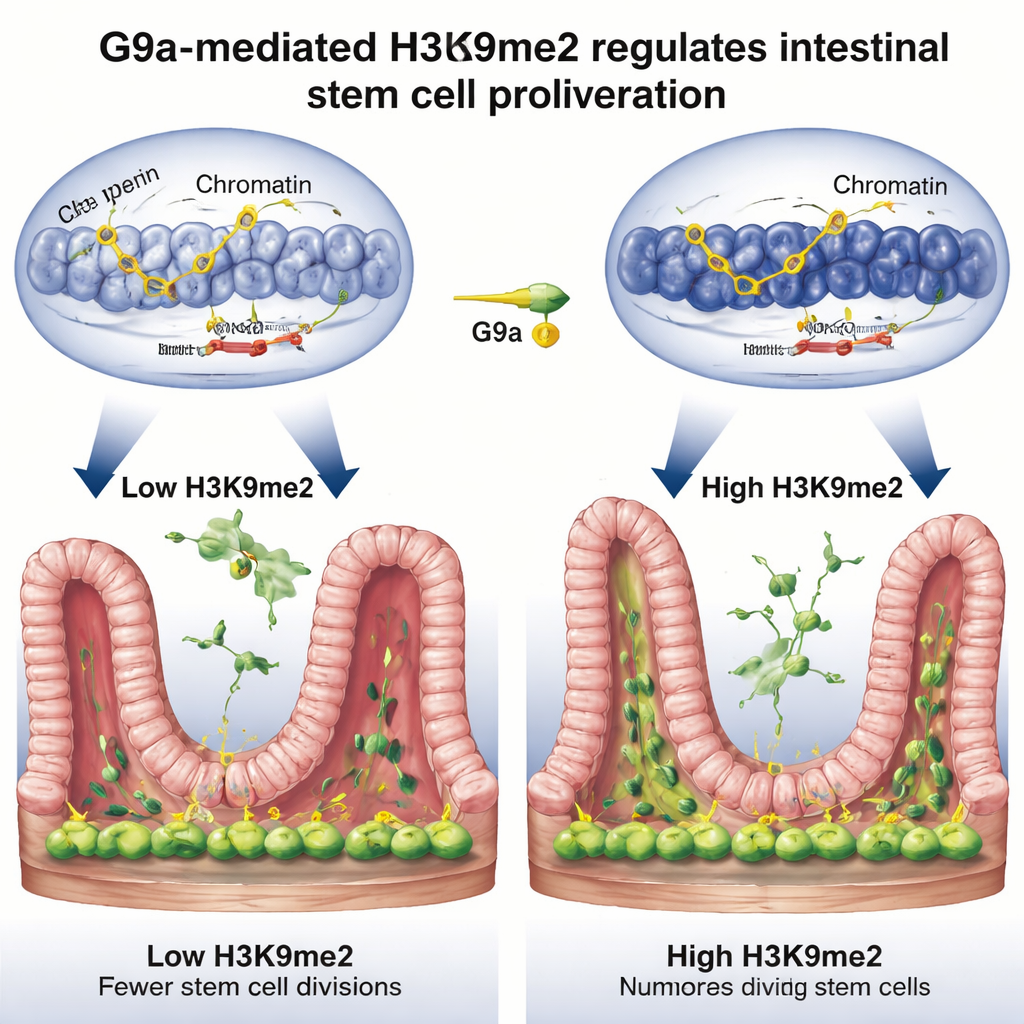
Rilasciare il freno sulla divisione cellulare
Approfondendo, il team ha chiesto quali geni fossero controllati da questo interruttore di riparazione. Combinando tre potenti metodi genomici a livello di tutto il genoma, hanno scoperto che H3K9me2, posto da G9a, tende a localizzarsi su tratti di DNA che normalmente funzionano come freni del ciclo cellulare — geni come Rb1cc1, Rb1, Cdkn1a e Pten, che rallentano o fermano la divisione cellulare. Quando G9a mancava, il marchio chimico scompariva da queste regioni, il DNA circostante si apriva e questi geni freno si attivavano più intensamente, portando a una proliferazione più lenta delle cellule staminali. Durante la riparazione normale dopo il danno, i livelli di H3K9me2 su questi geni aumentavano, la loro attività calava e le cellule staminali erano più libere di dividersi e ricostruire il rivestimento. In sostanza, G9a e H3K9me2 silenziano temporaneamente i segnali di “stop” affinché il tessuto possa rigenerarsi.
Una catena di segnalazione dagli stimoli immunitari alla riparazione
L’intestino non agisce da solo; ascolta continuamente segnali provenienti dal sistema immunitario. I ricercatori hanno ricostruito uno di questi segnali a monte di G9a. Dopo il danno, i livelli del messaggero immunitario IL-4 aumentavano, attivando una proteina chiamata STAT6 nelle cellule intestinali. STAT6 attivato si legava direttamente alla regione di controllo del gene G9a, incrementandone la produzione. Questo generava una catena di comando: IL-4 attiva STAT6, STAT6 aumenta G9a e G9a aggiunge H3K9me2 per silenziare i geni freno del ciclo cellulare, permettendo alle cellule staminali di espandersi e ripristinare il rivestimento danneggiato.
Cosa significa per i trattamenti futuri
Per un non specialista, questi risultati mostrano che la riparazione intestinale è guidata non solo dai geni, ma anche da segni chimici reversibili che regolano finemente quando quei geni vengono utilizzati. La via IL-4–STAT6–G9a–H3K9me2 funziona come un pannello di controllo interno che allenta i freni sulla divisione delle cellule staminali il tempo necessario per guarire, per poi poter essere resettato. In futuro, terapie che potenzino delicatamente questa via — come farmaci o strumenti basati sui geni che aumentino i livelli di G9a nel momento e nel luogo opportuni — potrebbero aiutare i pazienti a recuperare più rapidamente da danni da radiazioni, riacutizzazioni di malattia infiammatoria intestinale o altre condizioni che danneggiano il rivestimento intestinale, minimizzando al contempo i rischi di crescita cellulare incontrollata.
Citazione: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
Parole chiave: rigenerazione intestinale, epigenetica, cellule staminali, metilazione degli istoni, malattia infiammatoria intestinale