Clear Sky Science · it
Due sintetasi del segnale di quorum sensing con doppia funzione DspII e DspI coordinano l’interruttore di virulenza in Pseudomonas aeruginosa
Come un supermicrobo ospedaliero cambia strategia d’attacco
Pseudomonas aeruginosa è un noto patogeno nosocomiale che può causare infezioni polmonari e delle ferite particolarmente ostinate, soprattutto in pazienti vulnerabili. Sopravvive alternando due stili di vita: una comunità protetta e a crescita lenta chiamata biofilm e una forma veloce e aggressiva che invade i tessuti. Questo studio svela come il batterio decide quando uscire da un biofilm cronico e scatenare un attacco acuto, rivelando potenziali nuovi punti deboli per future terapie.
Una vita microbica tra nascondersi e attaccare
Molte infezioni batteriche procedono per fasi. Nelle fasi iniziali, le cellule libere nuotano e si diffondono nel corpo mobilitando armi potenti che danneggiano i tessuti dell’ospite. In seguito spesso si insediano in biofilm—strati densi e vischiosi aderenti a superfici come cateteri, tessuto polmonare o ferite. In queste comunità le cellule sono avvolte in una matrice protettiva che le rende difficili da eliminare con antibiotici o difese immunitarie. Tuttavia i biofilm non sono un vicolo cieco: le cellule possono lasciare la comunità, riacquistare mobilità e innescare nuovi episodi acuti altrove. Fino ad oggi non era chiaro come Pseudomonas aeruginosa coordini attivamente questo passaggio dalla persistenza cronica al ritorno della malattia aggressiva.
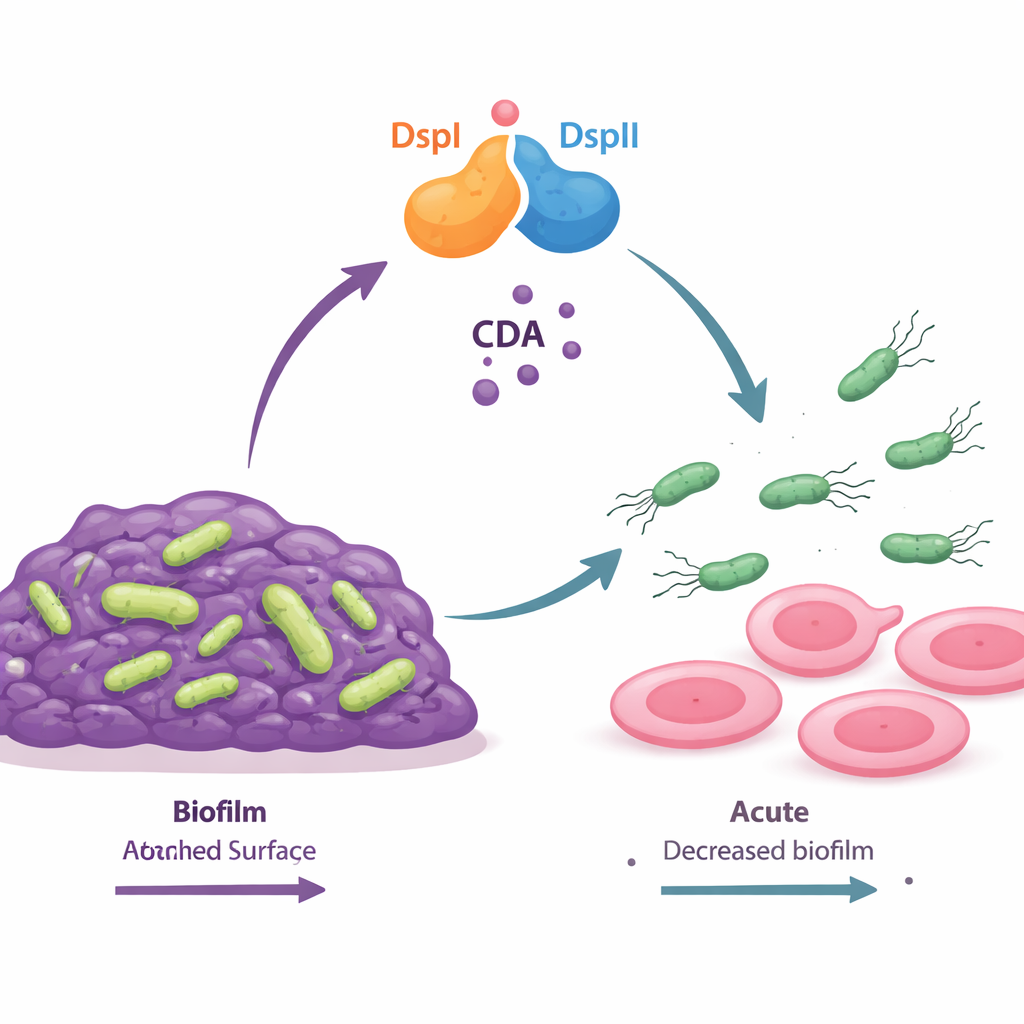
Un interruttore a due proteine che produce un segnale chimico di “vai”
Gli autori hanno scoperto che due proteine batteriche, chiamate DspI e DspII, lavorano insieme come una specie di interruttore molecolare. Entrambe sono enzimi dello stesso tipo generale e sono adiacenti nel genoma batterico, attivandosi insieme quando la popolazione aumenta di densità. Quando formano una coppia, sintetizzano un piccolo acido grasso segnale chiamato cis-2-decenoico (CDA), parte di un gruppo più ampio di molecole di comunicazione note come segnali DSF. I ceppi mutanti privi di DspI o DspII non sono più in grado di produrre CDA, formano biofilm insolitamente spessi e perdono la capacità di spostarsi a sciami sulle superfici. Solo quando entrambe le proteine vengono ripristinate insieme le cellule recuperano la normale produzione di segnale, la dispersione del biofilm e la motilità, dimostrando che i due enzimi funzionano come una squadra interdipendente.
Dal segnale chimico al movimento e alla fuga
CDA non agisce da sola; si integra nel circuito interno del batterio. Il gruppo ha mostrato che CDA riduce i livelli di un altro messaggero, il c-di-GMP, aumentando l’attività di un enzima specifico chiamato RbdA che degrada questo messaggero. Alti livelli di c-di-GMP favoriscono normalmente la costruzione del biofilm stimolando la produzione della matrice zuccherina e sopprimendo le flagelle, le piccole eliche che consentono il nuoto. Quando è presente CDA, i livelli di c-di-GMP diminuiscono, un regolatore chiamato FleQ cambia assetto, la produzione di zuccheri adesivi cala e le flagelle si estendono e si rafforzano. Di conseguenza i biofilm si allentano e le cellule riacquistano la capacità di muoversi e colonizzare nuovi territori.
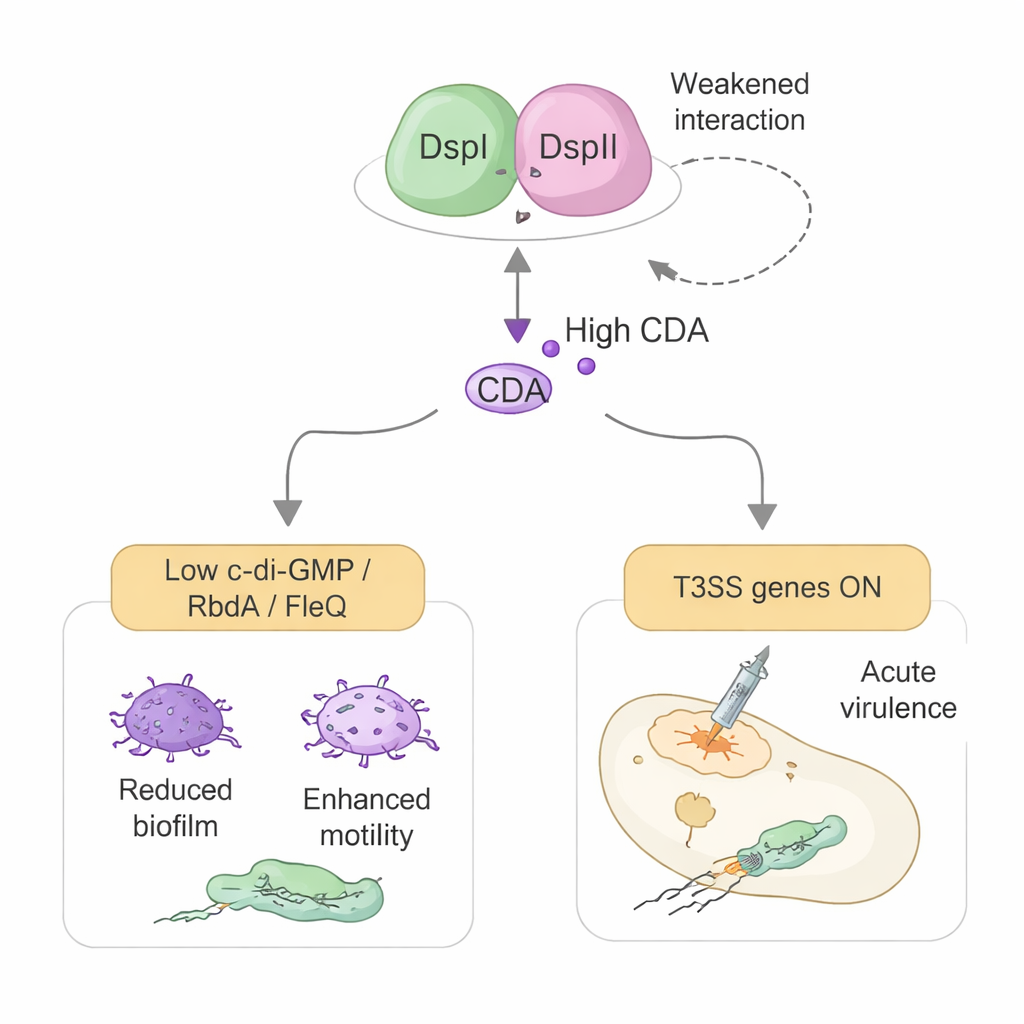
Rimodellare il sistema d’armi batterico
Lo studio rivela anche un secondo ruolo inatteso per DspI e DspII che va oltre la chimica. La stessa coppia proteica contribuisce ad attivare il sistema di secrezione di tipo III (T3SS) del batterio, un apparato a forma di siringa usato per iniettare tossine direttamente nelle cellule dell’ospite. Piuttosto che agire tramite CDA, questo effetto avviene tramite il controllo diretto di interruttori genetici. DspI e DspII attenuano la produzione di due piccoli RNA regolatori, RsmY e RsmZ, che normalmente sopprimono la sintesi delle proteine del T3SS. Lo fanno legandosi alla regione di controllo del DNA di uno degli RNA e interagendo fisicamente con una proteina regolatrice principale chiamata GacA. Quando RsmY e RsmZ sono tenuti sotto controllo, un attivatore a valle chiamato RsmA viene liberato, e i geni del T3SS e il suo controllore principale ExsA vengono attivati, aumentando la citotossicità in colture cellulari e la mortalità in un modello di infezione in insetti.
Un sistema che si autoregola con possibili bersagli farmacologici
In modo sofisticato, la forza della partnership DspI–DspII e il suo controllo sulla virulenza sono a loro volta regolati dai livelli di CDA. A basse concentrazioni—come quelle previste nelle cellule che stanno appena lasciando un biofilm—il CDA rafforza l’interazione tra le due proteine e promuove ulteriore produzione di segnale e attivazione del T3SS. A concentrazioni elevate all’interno di biofilm densi, il CDA indebolisce la loro interazione e riduce la loro capacità di legare il DNA, limitando l’ulteriore sintesi di segnale e la produzione costosa di armi nelle cellule che rimangono. Questo doppio ruolo rende il complesso DspI–DspII un punto nodale che collega la dimensione della popolazione, la fuga dal biofilm e la virulenza acuta. Poiché interrompere il complesso può bloccare sia la produzione del segnale sia l’attivazione del sistema di tossine, esso rappresenta un bersaglio interessante per futuri farmaci che potrebbero mantenere Pseudomonas in uno stato cronico meno dannoso e prevenire pericolose riacutizzazioni.
Citazione: Huang, J., Zhou, T., Zhou, X. et al. Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa. Nat Commun 17, 1926 (2026). https://doi.org/10.1038/s41467-026-68622-x
Parole chiave: Pseudomonas aeruginosa, dispersione del biofilm, quorum sensing, interruttore di virulenza, cis-2-decenoico