Clear Sky Science · it
Impronta dinamica del compromesso attività‑stabilità nell’evoluzione delle lactamasi
Perché è importante per la resistenza agli antibiotici
La resistenza agli antibiotici spesso sembra una scatola nera: i batteri «in qualche modo» cambiano e i farmaci smettono di funzionare. Questo studio apre quella scatola per uno degli enzimi di resistenza più noti al mondo, la β‑lattamasi TEM‑1, che aiuta i batteri a distruggere antibiotici simili alla penicillina. Osservando come la forma e i movimenti di questo enzima cambiano mentre evolve per colpire farmaci più recenti, gli autori rivelano perché le mutazioni che aumentano l’attività spesso indeboliscono la stabilità e come l’evoluzione trovi modi ingegnosi per bilanciare entrambe le proprietà.
Da combattente della penicillina a degradatore di farmaci più ampi
TEM‑1 inizialmente è molto efficace nel degradare le penicilline più vecchie ma è meno capace di affrontare farmaci più recenti e ingombranti come il cefotaxime. In molti ceppi clinici compare una singola mutazione chiave chiamata G238S vicino al sito attivo dell’enzima, la tasca dove vengono tagliati gli antibiotici. Questa mutazione migliora in modo drastico la capacità dell’enzima di distruggere il cefotaxime, pur danneggiando solo modestamente la sua attività originale contro la penicillina. Gli autori mostrano che la G238S non si limita ad allargare la tasca; riorganizza il modo in cui diversi anelli e eliche circostanti si muovono, creando una nuova conformazione funzionale che accoglie meglio i farmaci ingombranti.
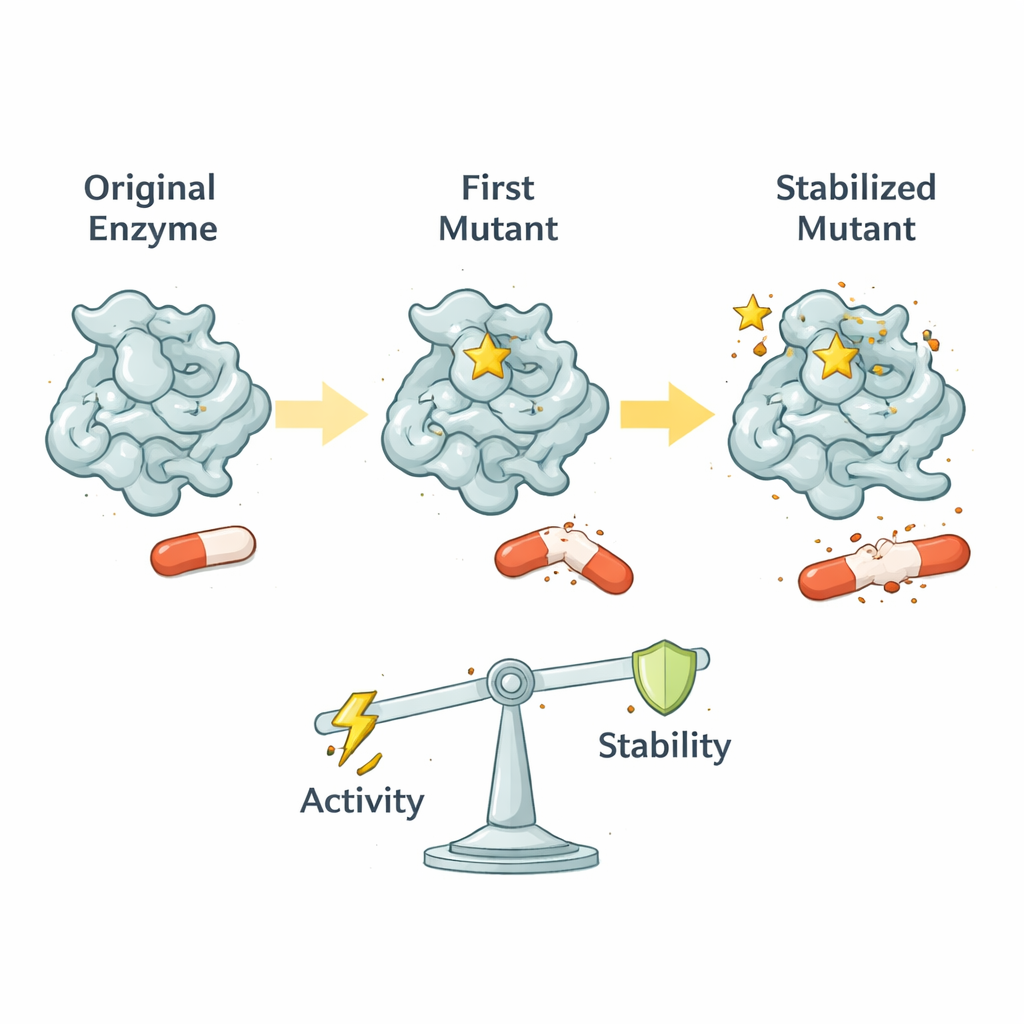
Il movimento delle proteine come manopola evolutiva
Usando tecniche avanzate di risonanza magnetica nucleare (NMR), i ricercatori hanno misurato come diverse parti di TEM‑1 si muovono su scale temporali che vanno dal trilionesimo al millesimo di secondo. Il TEM‑1 selvatico è piuttosto rigido, il che lo aiuta a processare in modo efficiente i suoi substrati originali. G238S lascia intatta la maggior parte di questa rigidità rapida ma introduce movimenti più lenti, accuratamente regolati, in molte pareti del sito attivo. Questi movimenti sono abbastanza veloci da tenere il passo con la chimica dell’enzima ma non così ampi da disturbare residui catalitici critici. Il risultato è una «finestra ottimizzata» di flessibilità: movimento sufficiente ad aprire la tasca per il cefotaxime, mantenendo però l’apparato chimico centrale correttamente allineato.
Bilanciare due forme invece di sceglierne una
L’evoluzione non congela TEM‑1 in una singola nuova forma. L’enzima campiona invece almeno due principali conformazioni: uno stato «penicillinasico» che somiglia alla struttura originale e uno stato più aperto «cefotaximasico» meglio adatto ai farmaci più recenti. Mutazioni aggiuntive che compaiono in seguito, come E104K e A42G, fanno qualcosa di sottile. Piuttosto che rendere semplicemente più stabile la nuova forma favorevole al cefotaxime, riequilibrano la miscela dei due stati. I dati NMR mostrano che parti diverse del sito attivo e dell’impalcatura di supporto possono spostare le loro popolazioni in modo indipendente lungo questo continuum a due stati. Ciò porta a un insieme combinatorio di varianti enzimatiche, ognuna con una diversa miscela di conformazioni simili alla penicillina e al cefotaxime e quindi con profili catalitici differenti.
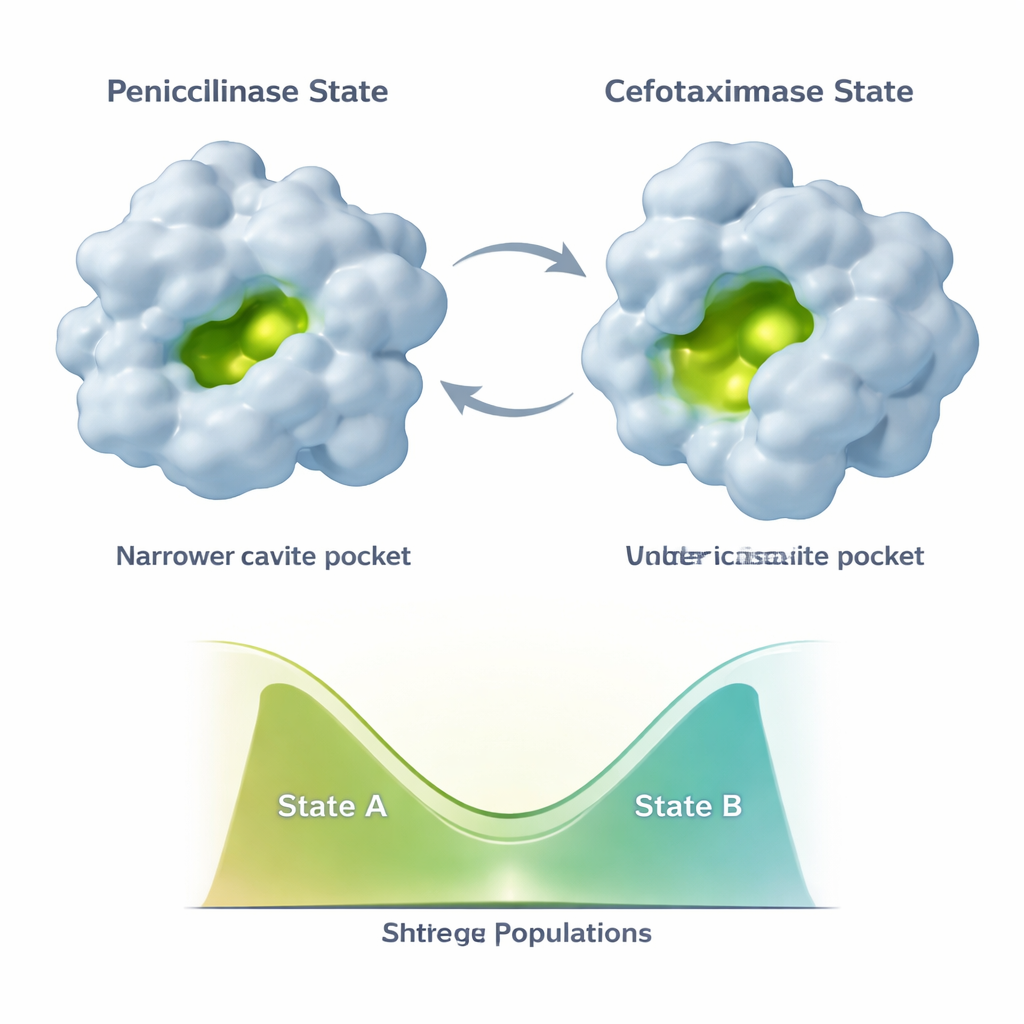
Punti deboli nascosti e riparazioni a distanza
Le mutazioni che migliorano l’attività spesso hanno un costo nascosto: rendono la proteina meno stabile. Invece di guardare solo al disfolding completo, il team ha mappato la stabilità locale a livello di brevi segmenti usando lo scambio idrogeno–deuterio con spettrometria di massa. Si è scoperto che G238S destabilizza non solo anelli vicini ma anche eliche distanti e regioni a foglio che costituiscono una spina dorsale strutturale. Alcune di queste regioni si sovrappongono a una tasca allosterica «criptica»—un’apertura raramente visitata nel nucleo della proteina che può legare piccole molecole e attenuare l’attività. G238S rende questa tasca più facile da aprire, incorporando di fatto una lieve caratteristica auto‑inibitoria nell’enzima. Mutazioni successive, in particolare A42G, rinforzano questa rete di sostegno indebolita, migliorando la stabilità locale intorno a tre eliche interagenti senza rimuovere le dinamiche vantaggiose del sito attivo. In altre parole, l’evoluzione ripara punti deboli strutturali distanti invece di annullare l’innovazione originale.
Cosa rivela lo studio sulla strategia evolutiva
Per un lettore non esperto, il messaggio centrale è che proteine come TEM‑1 non evolvono la resistenza con un semplice interruttore on–off. Ogni mutazione rimodella leggermente il modo in cui l’enzima respira, si flette e divide il proprio tempo tra diverse pose operative. G238S apre la porta a un nuovo compito—distruggere antibiotici più recenti—ma crea anche fragilità locali e uno stato parzialmente auto‑inibitorio. Le mutazioni secondarie agiscono come rinforzi accurati, stabilizzando l’impalcatura e sintonizzando il bilanciamento tra le vecchie e le nuove conformazioni in modo che l’enzima possa rimanere sia attivo sia durevole. Questa visione dinamica dell’evoluzione, in cui i movimenti e le debolezze locali contano quanto la struttura statica, può aiutare a guidare la progettazione di futuri antibiotici e farmaci mirati agli enzimi che siano più difficili da superare per i batteri.
Citazione: Arcia, E., Keramisanou, D., Jacobs, L.M.C. et al. Dynamic signature of activity-stability tradeoff in lactamase evolution. Nat Commun 17, 1884 (2026). https://doi.org/10.1038/s41467-026-68620-z
Parole chiave: resistenza agli antibiotici, beta-lattamasi, evoluzione delle proteine, dinamica degli enzimi, stabilità delle proteine