Clear Sky Science · it
Un atlante spazialmente risolto del cancro gastrico caratterizza una regione aggregata di linfociti
Perché il vicinato attorno a un tumore conta
Il cancro non è solo un ammasso di cellule ribelli; vive in un quartiere affollato di cellule immunitarie e strutturali che possono o aiutare a combattere il tumore o lasciarlo crescere indisturbato. Questo studio mappa quel vicinato nel cancro gastrico con dettaglio senza precedenti, mostrando come piccole aree calde e fredde immunitarie all’interno dello stesso tumore possano influenzare la risposta del paziente alle moderne immunoterapie.
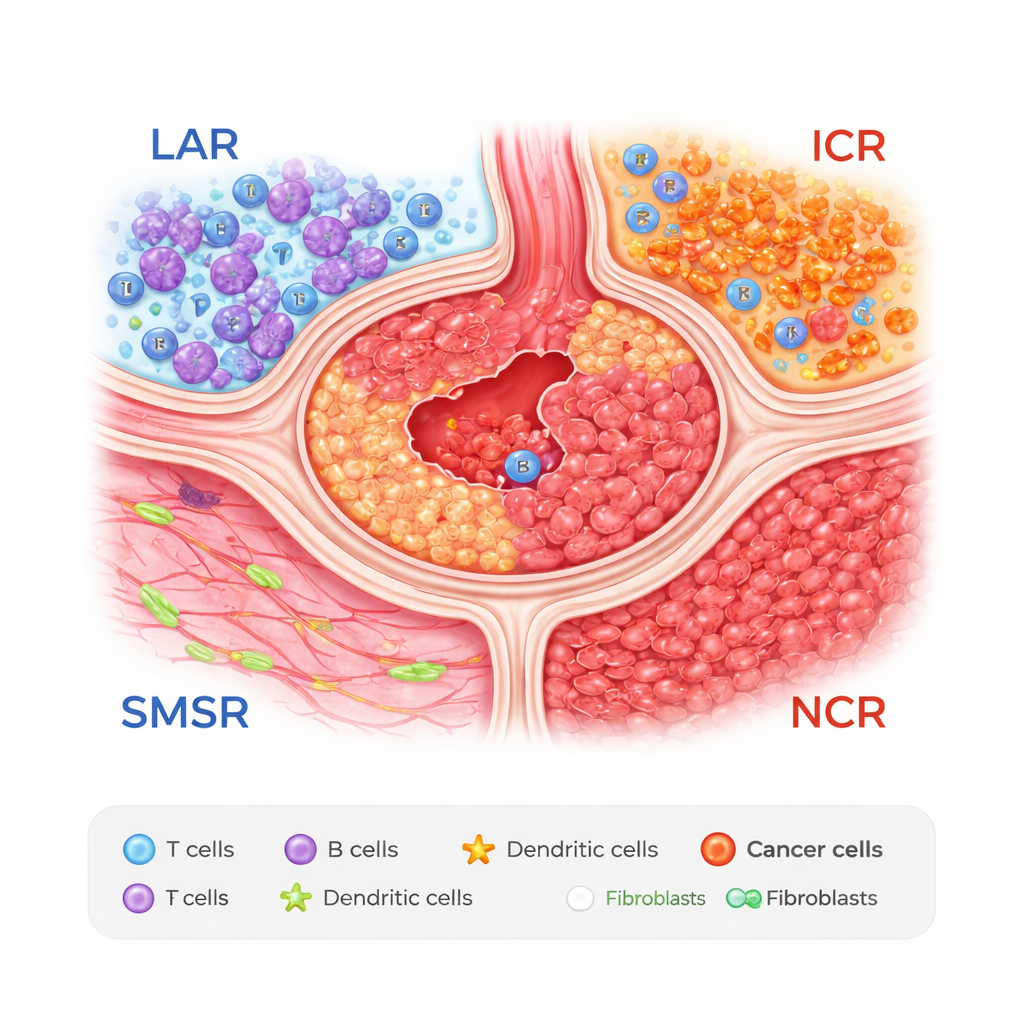
Quattro zone all’interno di un tumore gastrico
I ricercatori hanno combinato due strumenti potenti: il sequenziamento dell’RNA a singola cellula, che legge l’attività genica in singole cellule, e la trascrittomica spaziale, che registra dove quelle cellule si trovano nei campioni tissutali. Analizzando campioni di 27 pazienti, hanno scoperto che i tumori gastrici possono essere suddivisi in quattro zone ricorrenti. Una è una regione aggregata di linfociti (LAR), ricca di ammassi di cellule T e B che assomigliano a piccoli linfonodi. Un’altra è una regione di muscolo liscio e stroma (SMSR), dominata da tessuto muscolare e connettivo. Le restanti due zone sono aree dense di tumore: una regione cancerosa immunogenica (ICR), dove le cellule tumorali si mescolano con alcuni tipi cellulari protettivi dello stomaco, e una regione cancerosa negativamente immunogenica (NCR), piena di cellule maligne e relativamente povera di cellule immunitarie difensive.
Punti caldi immunitari collegati a esiti migliori
Il team ha riscontrato che la zona LAR è arricchita per geni tipicamente espressi nei linfonodi, dove le cellule immunitarie vengono educate e attivate. Questi includono segnali che aiutano a reclutare i linfociti e a organizzarli in strutture chiamate strutture linfatiche terziarie. Analizzando grandi dataset pubblici sul cancro, i tumori con espressione più elevata di geni associati alla LAR tendevano ad avere una sopravvivenza migliore e una probabilità leggermente più alta di rispondere alle terapie di checkpoint immunitario che rimuovono i freni dalle cellule T. Al contrario, le firme geniche delle regioni ricche di muscolo o fortemente cancerose erano generalmente associate a esiti peggiori in vari tipi di tumore.
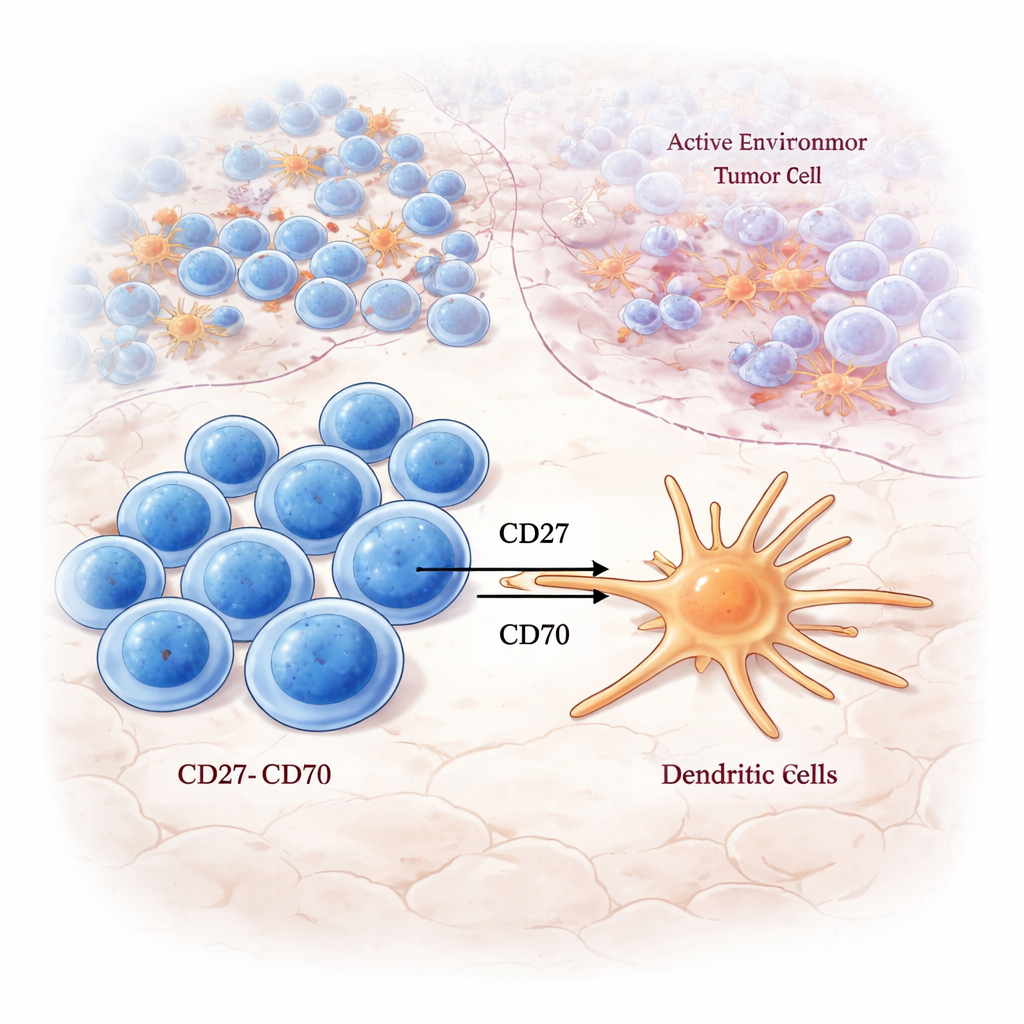
Dove le cellule T naive imparano a combattere
Avvicinandosi alla LAR, gli autori hanno osservato forte attività in vie di segnalazione centrali per il risveglio delle cellule T: la segnalazione del recettore delle cellule T, le vie di costimolazione e l’elaborazione degli antigeni. Le cellule T CD8 naive — cellule che non si sono ancora pienamente impegnate ad attaccare un bersaglio specifico — erano particolarmente correlate a questi segnali di attivazione all’interno della LAR, ma non altrove. Mediante colorazioni multicolori, hanno rilevato cellule CD8 nella LAR che presentavano marker sia di rinnovamento sia di proliferazione, suggerendo che questa regione funzioni come una zona di addestramento e espansione sul posto, dove vengono primate nuove cellule capaci di combattere il tumore.
Due varianti del vicinato immunitario
Non tutte le LAR sono uguali. Quando i ricercatori hanno raggruppato i pazienti in base alla composizione cellulare delle loro LAR, hanno identificato due modelli. Nei tumori del “Gruppo A”, le LAR somigliavano molto ai linfonodi classici, ricche di cellule B specializzate e cellule dendritiche, e le regioni tumorali adiacenti a queste LAR erano piene di linfociti attivati e pronti alla battaglia. Nel “Gruppo B”, le LAR erano meno sviluppate e il tessuto tumorale adiacente conteneva più cellule T in uno stato di riposo, meno impegnate. Analisi computazionali avanzate delle immagini tissutali hanno confermato che le cellule immunitarie attivate si raggruppavano fisicamente vicino a queste LAR più mature, suggerendo che l’architettura locale può indirizzare l’intensità della risposta immunitaria contro il tumore.
Segnali di checkpoint nello spazio
Lo studio ha anche tracciato dove sono espressi i cosiddetti “interruttori” immunitari, noti come molecole di checkpoint. Coppie stimolatorie come CD27–CD70 erano concentrate nella LAR, in particolare nei tumori del Gruppo A, collegando cellule CD8 esauste ma reattive al tumore con cellule dendritiche che potrebbero potenziarne ulteriormente l’attività. Al contrario, molte coppie di checkpoint inibitori, come TIGIT–NECTIN2 e LAG3–LGALS3, risultavano arricchite nella NCR, la zona più dominata dal tumore. Questo suggerisce che anche quando la segnalazione del recettore delle cellule T è presente, il panorama locale dei checkpoint può inclinare l’immunità verso attacco o soppressione, a seconda della regione del tumore.
Cosa significa per i pazienti
Per un non specialista, il messaggio chiave è che il luogo in cui le cellule immunitarie e i segnali si trovano all’interno di un tumore può contare tanto quanto il loro numero. Questo lavoro mostra che i tumori gastrici contengono vicinati immunitari distinti e che regioni robuste, simili a linfonodi, vicino al tumore sono associate a cellule T più attive e meglio posizionate e a esiti più favorevoli. Imparando a riconoscere e possibilmente rafforzare queste regioni aggregate di linfociti, terapie future potrebbero essere meglio adattate — scegliendo farmaci, combinazioni o persino strategie di somministrazione mirata che sfruttino i punti di forza immunitari interni del tumore.
Citazione: Gao, S., Qin, S., Wang, D. et al. A spatially resolved atlas of gastric cancer characterises a lymphocyte-aggregated region. Nat Commun 17, 2059 (2026). https://doi.org/10.1038/s41467-026-68612-z
Parole chiave: cancro gastrico, microambiente tumorale, strutture linfatiche terziarie, trascrittomica spaziale, immunoterapia oncologica