Clear Sky Science · it
Invecchiamento divergente delle mammelle nullipare e paripare rivela cellule epiteliali ibride IL33+
Come la gravidanza può rimodellare il rischio di cancro al seno lungo la vita
Perché avere un figlio in giovane età riduce il rischio di cancro al seno nell’arco della vita di una donna, mentre semplicemente invecchiare lo aumenta? Questo studio usa topi per scrutare l’“ecosistema” cellulare della mammella nel tempo, confrontando animali che non hanno mai avuto una gravidanza con altri che invece l’hanno avuta. Seguendo come singole cellule cambiano con l’età e la riproduzione, i ricercatori scoprono un tipo cellulare raro e mutevole che potrebbe contribuire a spiegare la protezione a lungo termine conferita dalla gravidanza.
La mammella come tessuto vivo e dinamico
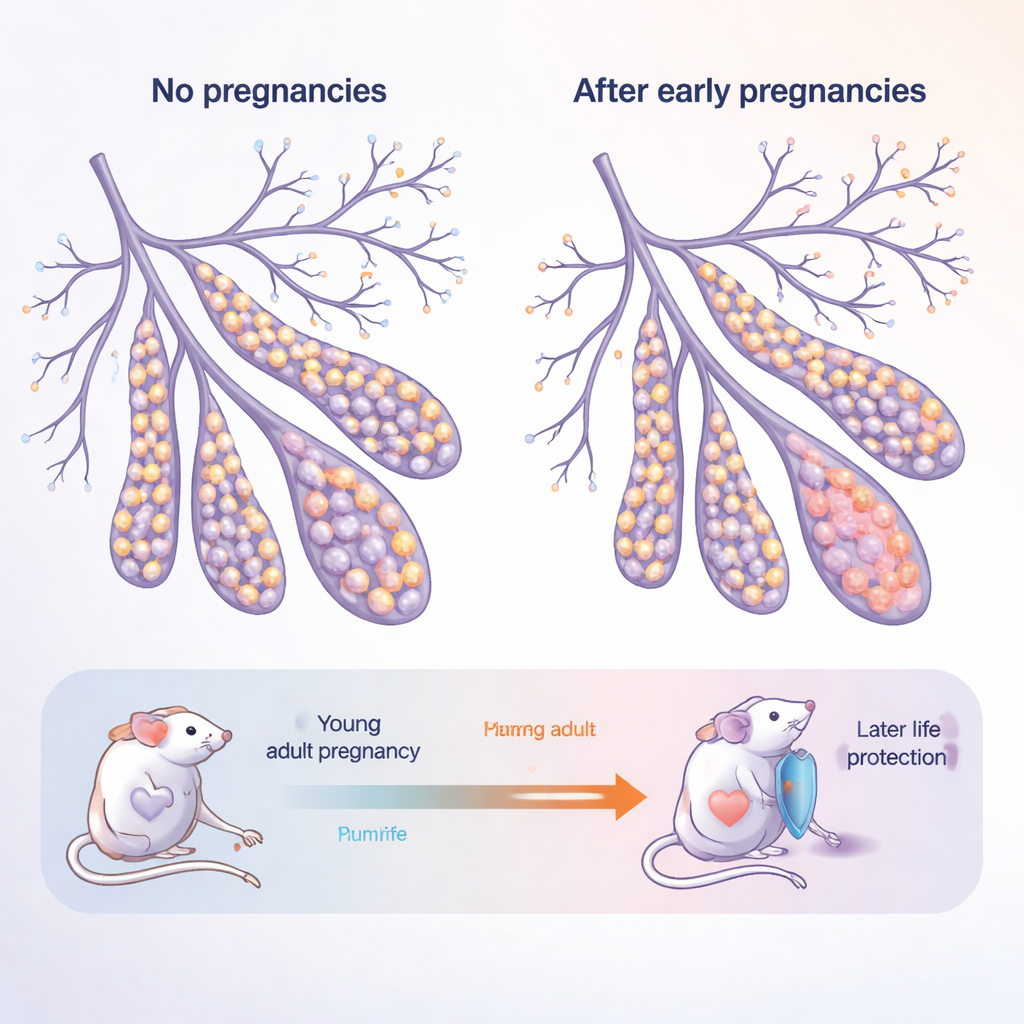
La ghiandola mammaria non è un organo statico: cresce e si rimodella in modo drammatico durante la pubertà, la gravidanza e di nuovo quando la produzione di latte termina. È costituita da due strati principali di cellule epiteliali che rivestono i dotti: le cellule interne “luminali” che mettono in contatto latte e ormoni, e le cellule esterne “basali” che forniscono struttura e ospitano cellule di tipo staminale. Gli autori hanno studiato topi giovani adulti e topi più anziani, “post‑menopausa”, ciascuno sia mai gravido (nulliparo) sia dopo gravidanze multiple (pariparo). Questo disegno imita una donna che dà alla luce nei suoi vent’anni e poi invecchia fino ai cinquant’anni e oltre.
Come invecchiamento e gravidanza tirano il tessuto in direzioni diverse
Con l’avanzare dell’età, nei topi che non avevano mai gravidato le ghiandole mammarie si spostarono verso una quota maggiore di cellule basali e un minor numero di cellule luminali. Queste ghiandole più anziane e mai gravide produssero anche molti più organoidi—strutture 3D in miniatura coltivate da singole cellule—indicando che le loro cellule erano insolutamente propense a proliferare. Al contrario, i topi che avevano sperimentato gravidanze mostrarono un bilanciamento “normalizzato”: l’aumento legato all’età delle cellule basali era attenuato e le loro cellule formarono meno organoidi. Ciò suggerisce che la gravidanza lascia un’impronta duratura che modifica sia come le cellule scelgono il loro destino sia la loro potenziale capacità rigenerativa e, potenzialmente, cancerosa.
La scoperta di cellule ibride e mutevoli
Per indagare più a fondo, il team ha usato il sequenziamento RNA a singola cellula per leggere quali geni erano attivi in migliaia di singole cellule mammarie. Tra le attese cellule luminali, basali, immunitarie e stromali, hanno trovato un gruppo raro che non rientrava nettamente in nessuno dei due strati principali. Queste cellule esprimevano marcatori sia delle linee luminali sia basali, guadagnandosi il nome di cellule epiteliali “ibride”. Sorprendentemente, questi ibridi si accumularono con l’età nei topi mai gravidi ma erano molto meno comuni nei topi altrettanto vecchi che avevano subito gravidanze. Le ibride esprimevano fortemente un gene chiamato Il33, che codifica la molecola di segnalazione IL‑33, insieme a marcatori legati a stadi precoci dello sviluppo e ad alta plasticità—la capacità di cambiare identità o comportamento.
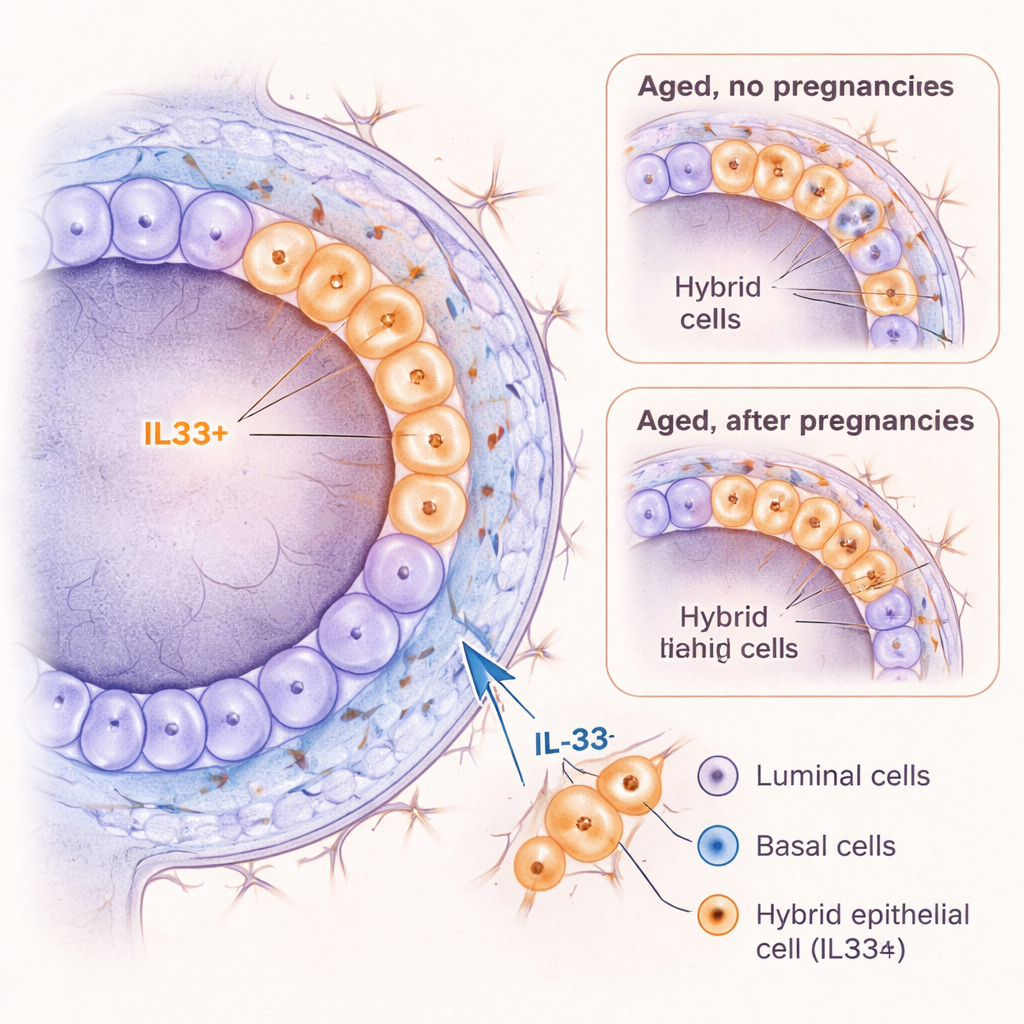
IL‑33 come promotore di stati cellulari rischiosi
Poiché IL‑33 è stato associato a infiammazione e cancro in altri organi, i ricercatori si sono chiesti se potesse attivamente spingere le cellule mammarie verso uno stato simile all’ibrido. Quando trattarono cellule mammarie di topo giovani con IL‑33 in coltura 3D, le cellule dello strato basale formarono più organoidi, mantennero un’identità più primitiva e produssero più cellule con il marcatore ibrido KRT6A. In topi giovani vivi, iniezioni a breve termine di IL‑33 causarono l’allargamento dei dotti e innescarono un’esplosione di divisione cellulare, insieme a un picco temporaneo di cellule ibride positive per KRT6A e uno spostamento verso un profilo più simile al basale. È importante che, quando le cellule portavano una mutazione legata al cancro (perdita del gene oncosoppressore Trp53), IL‑33 ne aumentò ulteriormente la crescita. Nel complesso, questi risultati suggeriscono che IL‑33 contribuisce a creare uno stato cellulare plastico e proliferativo che potrebbe essere particolarmente vulnerabile alla trasformazione cancerosa.
Indizi dal tessuto mammario umano
Per verificare se cellule simili esistono negli esseri umani, gli autori hanno rianalizzato diversi ampi dataset single‑cell da tessuto mammario umano normale. Hanno identificato una piccola popolazione di cellule epiteliali umane che, come gli ibridi murini, mostrava caratteristiche sia luminali sia basali ed esprimeva IL33 e geni correlati. Le cellule IL33‑positive divennero più comuni con l’età in più dataset. In cellule mammarie umane primarie coltivate in laboratorio, il trattamento con IL‑33 aumentò la formazione di organoidi, spostò le cellule verso un profilo più simile al basale e arricchì per cellule positive a CD44—un marcatore spesso associato a cellule immature e di tipo staminale nel cancro al seno. Sebbene i campioni umani disponibili non permettessero di testare in modo netto come una gravidanza precoce altera questa popolazione, le analogie con il modello murino sono notevoli.
Cosa significa per la comprensione della protezione dal cancro al seno
Per un lettore non specialista, il messaggio centrale è che la gravidanza sembra ri‑cablaggiare il modo in cui il tessuto mammario invecchia. Nei topi, una gravidanza precoce previene l’accumulo di cellule ibride ricche di IL‑33 che sfumano il confine tra i principali strati cellulari della mammella e si comportano in modo altamente flessibile e pronto alla crescita. La stessa IL‑33 può spingere le cellule verso questo stato rischioso e mutevole, specialmente quando sono presenti mutazioni legate al cancro. Riducendo il numero o la persistenza di queste cellule ibride, la gravidanza potrebbe diminuire le probabilità che il tessuto mammario invecchiato contenga il “tipo sbagliato” di cellula al “momento sbagliato”—una cellula pronta a precipitare verso il cancro. Questa intuizione meccanicistica potrebbe alla fine guidare strategie per imitare gli effetti protettivi della gravidanza precoce senza richiedere una gravidanza stessa.
Citazione: Olander, A., Medina, P., Haro Acosta, V. et al. Divergent aging of nulliparous and parous mammary glands reveals IL33+ hybrid epithelial cells. Nat Commun 17, 1898 (2026). https://doi.org/10.1038/s41467-026-68611-0
Parole chiave: invecchiamento del seno, gravidanza e cancro al seno, cellule staminali mammarie, segnalazione IL-33, cellule epiteliali ibride