Clear Sky Science · it
Espandere l’ambito dei carichi utili negli anticorpi coniugati per il trasporto di farmaci contenenti gruppi idrossilici tramite fosforamidati auto-immolativi
Missili più intelligenti contro il cancro
I farmaci antitumorali possono essere estremamente potenti, ma spesso agiscono come un bombardamento indiscriminato: colpiscono i tessuti sani quasi quanto i tumori. Gli anticorpi–farmaco coniugati (ADC) sono stati inventati per risolvere questo problema legando una molecola tossica a un anticorpo che indirizza il trattamento alle cellule tumorali, trasformandolo in un missile guidato. Questo articolo descrive un nuovo “connettore” chimico tra anticorpo e farmaco che rende questi missili sia più precisi sia più flessibili, aprendo la strada a molti più tipi di terapie oncologiche rispetto a quelle che gli ADC attuali possono trasportare.
Perché i farmaci mirati odierni sono ancora limitati
Gli ADC sono costruiti da tre parti: un anticorpo che riconosce un marcatore sulle cellule tumorali, un farmaco tossico (il “carico utile”) e un linker chimico che li collega. La maggior parte degli ADC approvati si basa su pochi tipi di carichi utili che danneggiano il DNA o bloccano la divisione cellulare in modi simili. Una ragione principale è il linker: deve trattenere il farmaco in modo saldo mentre l’ADC circola nel sangue, per poi rilasciarlo in modo netto una volta all’interno della cellula tumorale. I linker esistenti funzionano bene solo con certi gruppi chimici sui farmaci, in particolare ammine, e spesso faticano con le numerose molecole che contengono gruppi alcolici (–OH). Questo lascia fuori dal gioco un grande numero di agenti antitumorali promettenti perché non possono essere consegnati in modo sicuro o efficiente dai progetti ADC attuali.
Prendere in prestito un trucco dalle pillole antivirali
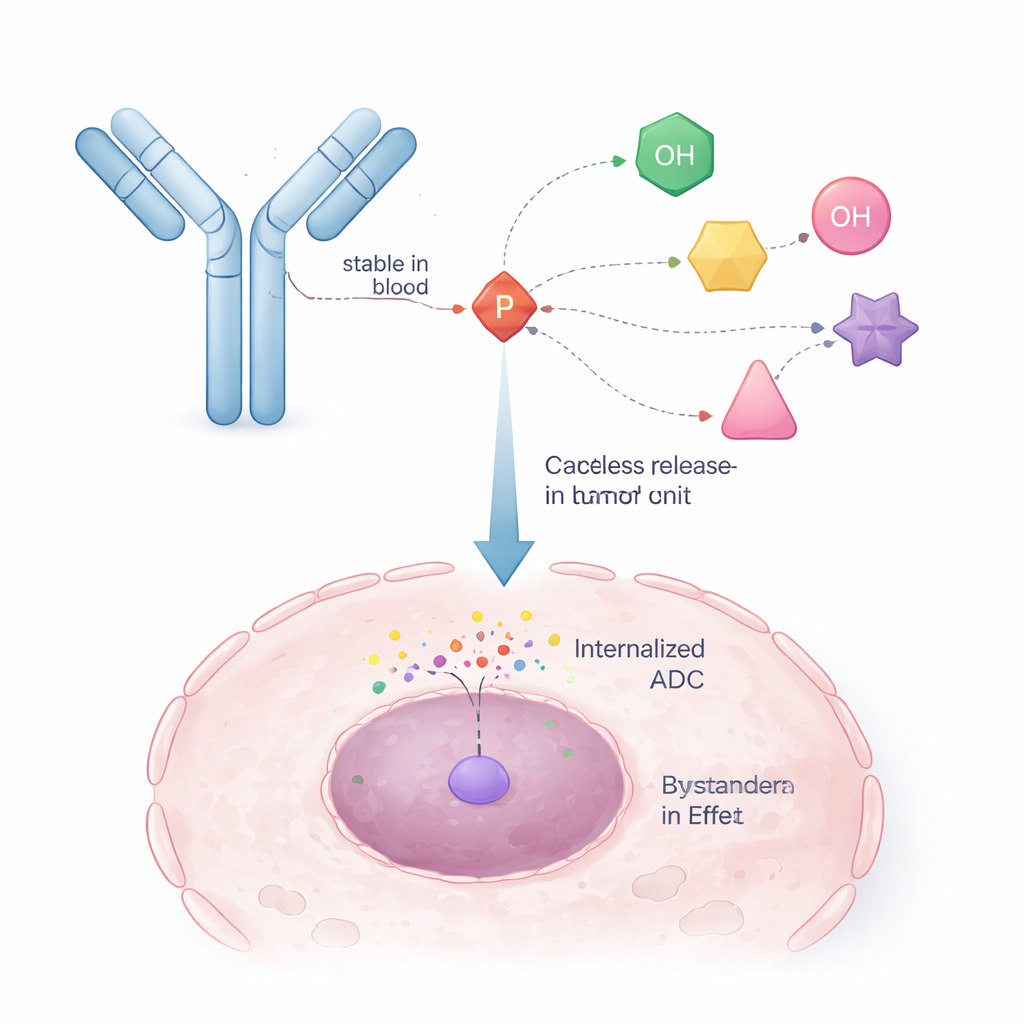
I ricercatori si sono ispirati a una strategia già consolidata nei farmaci antivirali chiamata ProTide. In quei medicinali, un’unità chimica a base di fosforo maschera temporaneamente il gruppo fosfato carico di una molecola in modo che possa entrare nelle cellule, per poi disassemblarsi all’interno e rilasciare la forma attiva. Gli autori hanno reingegnerizzato questo concetto in modo che un braccio del nucleo fosforico venga usato per legarsi all’anticorpo, mentre gli altri bracci trattengono il farmaco antitumorale. Si crea così un linker “auto-immolativo”: una volta che un innesco interno (ad esempio un enzima in una cellula tumorale) taglia una piccola parte della struttura, l’unità fosforica collassa in modo controllato e rilascia la molecola di farmaco originale con il gruppo alcolico ripristinato e non modificato.
Costruire un connettore chimico versatile
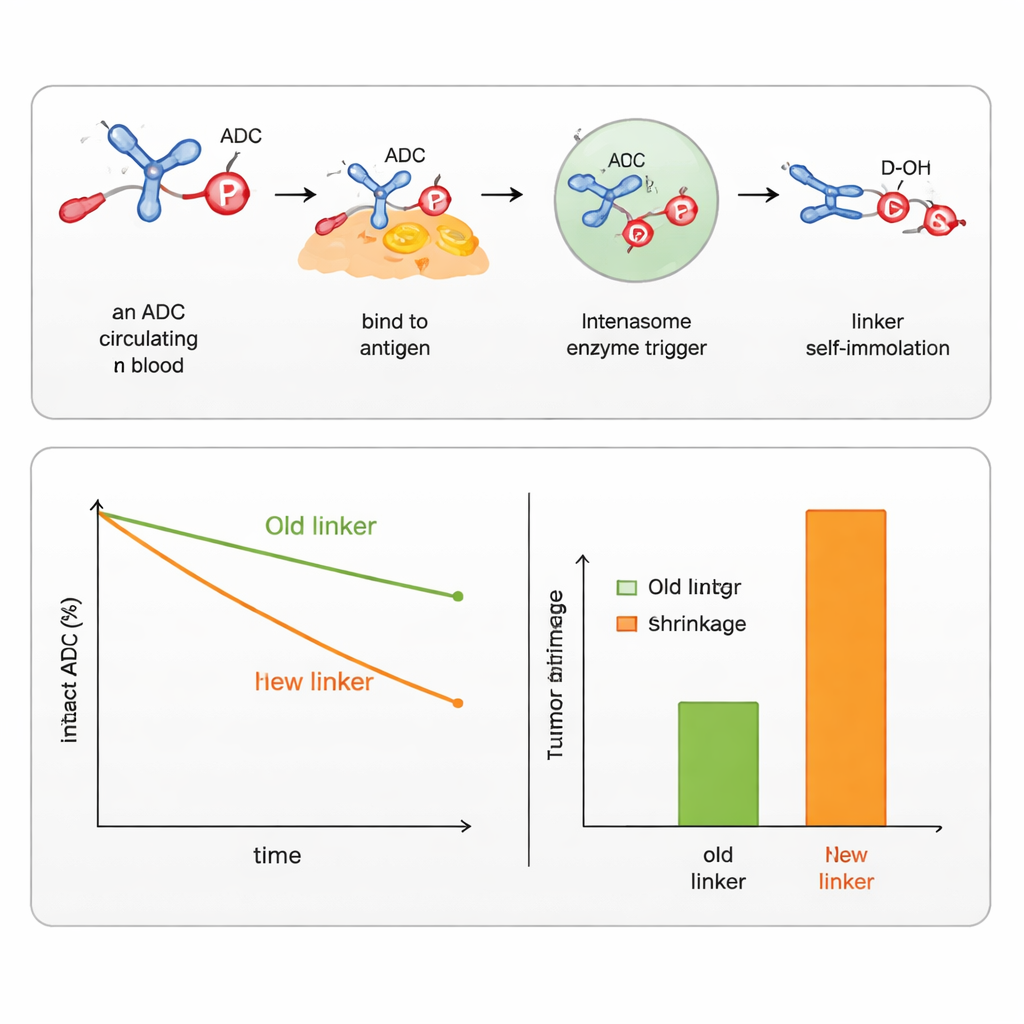
Il gruppo ha dimostrato che, modificando i gruppi attorno all’atomo di fosforo, è possibile calibrare la stabilità del linker nel sangue e la rapidità con cui si disintegra all’interno delle cellule. Hanno progettato versioni che rispondono a diversi tipi di inneschi comuni nelle cellule tumorali, inclusi esterasi e proteasi (enzimi che tagliano legami specifici), enzimi che riconoscono gruppi zuccherini e condizioni riducenti nei compartimenti cellulari. Con questi design sono riusciti ad attaccare e rilasciare sia alcoli aromatici (come la chemioterapia SN38) sia alcoli alifatici (come DXd, il carico utile in un ADC approvato per il cancro al seno). Confrontati direttamente con i linker commerciali esistenti per SN38 e DXd, i nuovi linker fosforamidati hanno mantenuto i farmaci legati più a lungo nel siero, hanno consegnato più farmaco ai tumori e hanno prodotto una maggiore riduzione tumorale nei topi, mostrando al contempo un minor impatto sulle cellule sane.
Sbloccare molti nuovi carichi utili per il cancro
Per verificare l’ampiezza di impiego del linker, i ricercatori hanno assemblato ADC contenenti dieci farmaci diversi che presentano almeno un gruppo –OH ma agiscono in modi molto differenti all’interno delle cellule tumorali. Questi includevano inibitori della sintesi del DNA, del ripiegamento proteico (HSP90), del metabolismo energetico (NAMPT e DHODH) e della traduzione proteica, oltre ad agenti noti come paclitaxel e gemcitabina. Nonostante l’ampia varietà di strutture, sono riusciti a ottenere ADC omogenei con elevato carico di farmaco per tutti. In studi cellulari su diversi tipi di tumore, la maggior parte di questi ADC ha mostrato potenza a livello nanomolare o anche sub-nanomolare e una chiara selettività per le cellule che esprimevano l’antigene riconosciuto dall’anticorpo, confermando che il linker poteva rilasciare in modo affidabile il farmaco attivo all’interno delle cellule giuste.
La gemcitabina come esempio illustrativo
La gemcitabina è una chemioterapia ampiamente utilizzata, ma nella sua forma convenzionale viene eliminata dall’organismo così rapidamente che i pazienti devono ricevere dosi ripetute e elevate, il che limita la quantità somministrabile in sicurezza. Usando il linker fosforamidato, gli autori hanno legato la gemcitabina a un anticorpo che mira HER2 in corrispondenza di due possibili posizioni alcoliche e hanno mostrato che entrambe le versioni recuperano piena attività una volta all’interno delle cellule tumorali. In modelli murini di tumori HER2-positivi, una singola dose dell’ADC con gemcitabina—contenente circa mille volte meno gemcitabina totale rispetto ai regimi con farmaco libero tipici—ha prodotto un controllo tumorale forte e selettivo. Il comportamento dell’ADC nel flusso sanguigno coincideva strettamente con quello dell’anticorpo non coniugato e dosi elevate sono state ben tollerate nei ratti, suggerendo un ampio margine di sicurezza.
Cosa significa per il trattamento futuro del cancro
Per i non specialisti, il messaggio principale è che questo lavoro fornisce un nuovo connettore chimico altamente adattabile che permette agli anticorpi di trasportare una gamma molto più ampia di farmaci antitumorali rispetto al passato, e di farlo in modo più sicuro. Garantendo che i farmaci rimangano legati durante la circolazione e vengano rilasciati solo dopo che l’ADC è stato internalizzato nella cellula tumorale, i linker fosforamidati migliorano la quantità di farmaco che raggiunge il tumore e riducono i danni collaterali ai tessuti sani. Altrettanto importante, consentono di riutilizzare farmaci small-molecule potenti esistenti—con forme e meccanismi molto diversi—come terapie mirate. Questo potrebbe ampliare notevolmente il ventaglio di ADC disponibili per i pazienti e aiutare a trattare tumori che hanno sviluppato resistenza al limitato insieme di carichi utili attuali.
Citazione: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
Parole chiave: anticorpi–farmaco coniugati, consegna di farmaci per il cancro, linker auto-immolativi, chimica dei fosforamidati, chemioterapia mirata