Clear Sky Science · it
Cianazione C–H regio-divergente e enantioselettiva di ammine secondarie controllata dal ligando
Perché cambiare piccoli legami conta per grandi farmaci
Molti farmaci di maggior successo contengono piccoli elementi azotati chiamati ammine. Piccole variazioni nel modo in cui gli atomi sono connessi attorno a queste ammine possono trasformare un farmaco debole in un trattamento potente e selettivo — o in qualcosa di inattivo o persino dannoso. Questo articolo descrive un nuovo modo per modificare questi blocchi amminici a piacere, permettendo ai chimici di scegliere esattamente dove sulla molecola intervenire e quale forma enantiomerica ottenere, entrambi aspetti cruciali per progettare farmaci più sicuri ed efficaci.
Scegliere un punto in una molecola affollata
Le ammine nei farmaci spesso possiedono diversi legami carbonio–idrogeno (C–H) molto simili che normalmente si comportano quasi allo stesso modo. I chimici vorrebbero sostituire solo uno di quegli idrogeni con un gruppo utile, come il gruppo ciano (–CN), senza alterare il resto della molecola. Questo è difficile perché le reazioni standard tendono a reagire nel sito più reattivo imposto dalla struttura molecolare, non in quello scelto dal chimico. Qui, gli autori lavorano con ammine secondarie semplici e flessibili che portano due catene carboniose diverse legate all’azoto. Dimostrano che, a partire dalla stessa ammina, possono indirizzare la reazione verso una di due posizioni vicine — o adiacente al piccolo gruppo N‑metile (il cosiddetto sito α′) oppure un carbonio più lontano sull’altra catena (il sito β) — semplicemente cambiando il ligando intorno a un catalizzatore al rame.
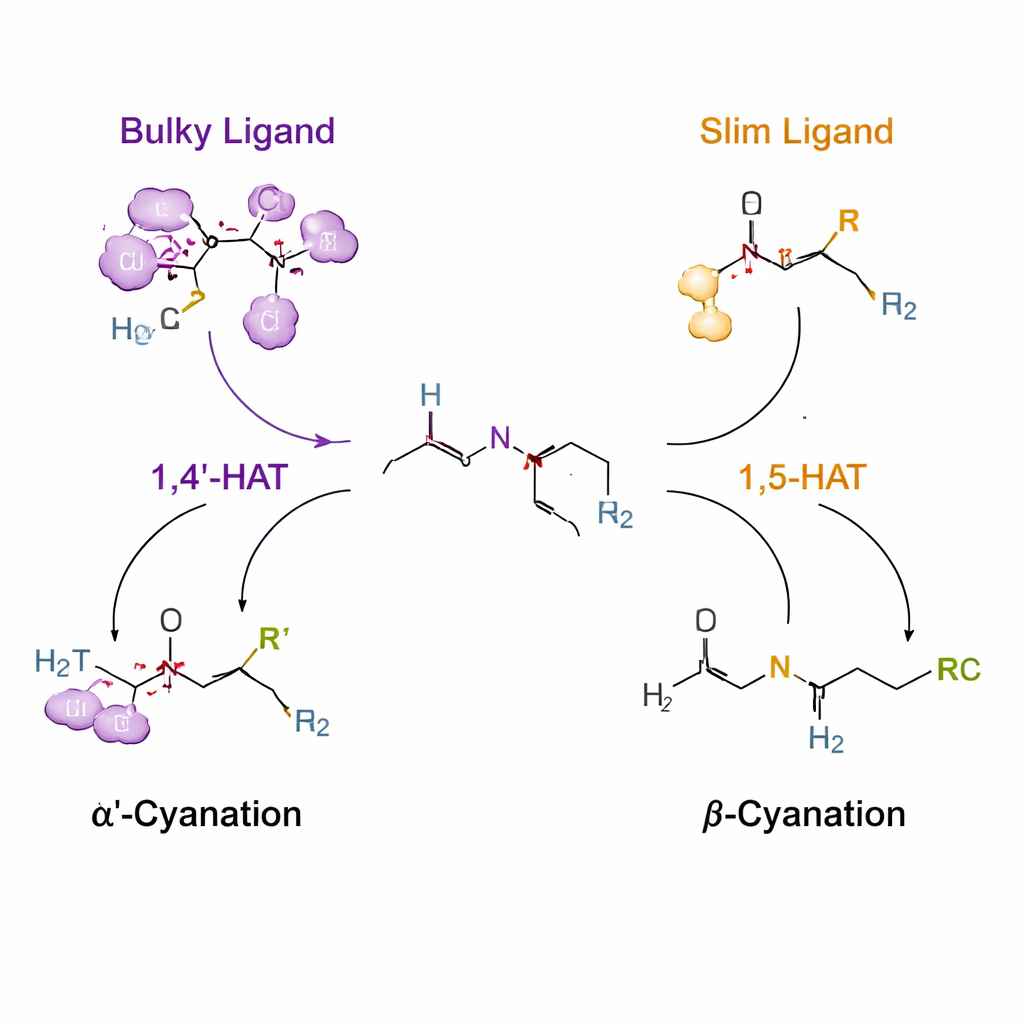
Usare “salti” controllati di idrogeno per guidare la reattività
Il trucco chiave si basa su un processo chiamato trasferimento di atomo di idrogeno, in cui un radicale centrato sull’azoto a vita breve asporta un idrogeno da un carbonio vicino. Normalmente questi radicali preferiscono una distanza particolare, favorendo una «portata» a sei termini nota come 1,5‑HAT. Gli autori installano un manico temporaneo a base di urea e cloro sull’ammina in modo che, sotto catalisi al rame, si formi questo radicale azotato e possa strappare un idrogeno sia dalla posizione α′ sia da quella β. Progettando ligandi — molecole organiche che avvolgono il rame — rimodellano l’ambiente del radicale. Un ligando molto ingombrante (denominato L14) spinge il sistema verso un inusuale step 1,4′‑HAT che prende di mira il gruppo N‑metile, portando a una cianazione α′ selettiva. Ligandi più snelli (come L8) consentono il percorso convenzionale 1,5‑HAT, indirizzando invece la reazione verso il sito β.
Dal controllo della posizione al controllo della mano
Oltre a scegliere dove reagire, il gruppo mira anche a controllare la chiralità, che è vitale perché molti farmaci esistono in forme sinistrorse e destrorse che si comportano diversamente nell’organismo. Per ottenere ciò introducono ligandi chirali — molecole che possiedono una forma con mano propria — nel complesso di rame. Due di questi ligandi, L24 e L41, conferiscono un’alta preferenza per un enantiomero quando la reazione introduce il gruppo ciano in posizioni β, includendo sia siti benzylici (adiacenti ad anelli aromatici) sia siti allylici (adiacenti a doppi legami C–C). Su una vasta gamma di ammine di partenza, il metodo fornisce prodotti β‑cianati con eccellente selettività sia di sito sia di mano, e funziona su scala grammo, mostrando che il processo è pratico e robusto per la sintesi.
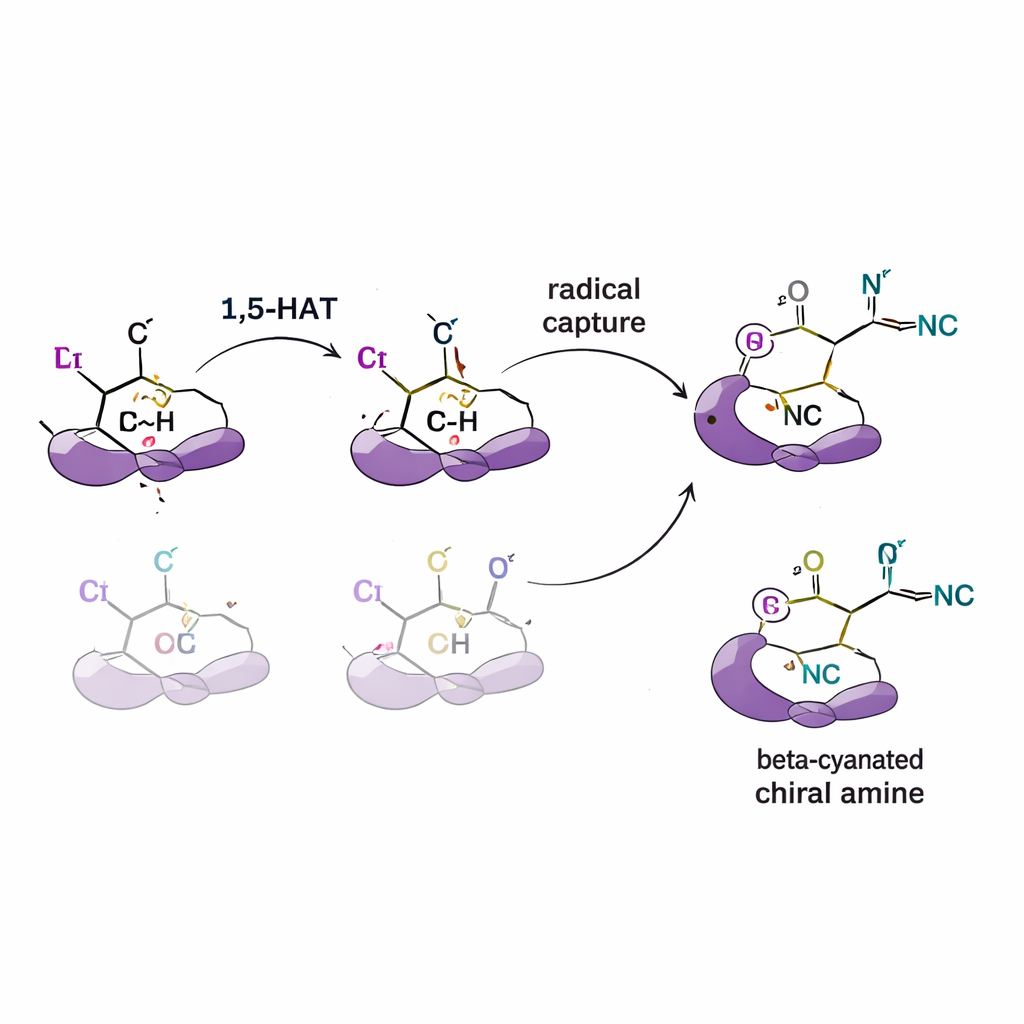
Mettere alla prova il meccanismo dietro la selettività
Per capire come nasce questo controllo, gli autori conducono una serie di esperimenti meccanicistici. Aggiungendo «trappole» per radicali confermano che sono coinvolti intermedi radicalici reattivi. Usando substrati in cui alcuni idrogeni sono sostituiti con deuterio (una forma più pesante dell’idrogeno), rilevano effetti isotopici cinetici che indicano che il trasferimento di idrogeno è lo step lento e quello che determina la selettività della reazione. Esperimenti di marcatura mostrano anche che l’idrogeno si muove in un singolo passo unidirezionale piuttosto che saltellare avanti e indietro tra le posizioni. Simulazioni complementari al calcolatore (teoria del funzionale della densità) supportano questi risultati, indicando che la forma e l’ingombro del ligando alterano l’energia dei percorsi concorrenti di trasferimento di idrogeno e il modo in cui il radicale si combina quindi con il rame e il cianuro per dare un enantiomero preferito.
Cosa significa per la progettazione futura di farmaci
Nel complesso, questo lavoro introduce una strategia flessibile per rimodellare gruppi amminici comuni in due siti strettamente correlati, su richiesta, con un controllo fine sulla chiralità molecolare. Cambiando solo il ligando su un catalizzatore al rame, i chimici possono scegliere se collocare un gruppo ciano su un piccolo gruppo N‑metile oppure sul carbonio vicino di una catena laterale diversa, e farlo su molte molecole complesse di tipo farmaceutico. Poiché i gruppi ciano sono preziosi punti di partenza per molte altre funzionalizzazioni, questo approccio «scegli-il-sito» e «scegli-la-mano» dovrebbe rendere più semplice esplorare e ottimizzare nuovi farmaci costruiti a partire dagli stessi scheletri amminici di base.
Citazione: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
Parole chiave: funzionalizzazione delle ammine, trasferimento di atomi di idrogeno, catalisi al rame, cianazione enantioselettiva, chimica medicinale