Clear Sky Science · it
Doppie localizzazioni genomiche e funzioni regolatorie geniche di MBD-2 con e senza NuRD in Caenorhabditis elegans privo di metilazione del DNA
Come i vermi minuscoli riscrivono le regole del controllo genico
Le nostre cellule usano marchi chimici sul DNA e sulle proteine per ricordare quali geni devono essere attivi o spenti. Uno dei marchi più noti, la metilazione del DNA, manca in alcuni animali—eppure questi crescono e si riproducono normalmente. Questo articolo esplora come un piccolo verme, Caenorhabditis elegans, gestisca il controllo genico senza metilazione del DNA, rivelando un sistema di riserva sorprendentemente flessibile che può mutare il modo in cui pensiamo all’epigenetica.
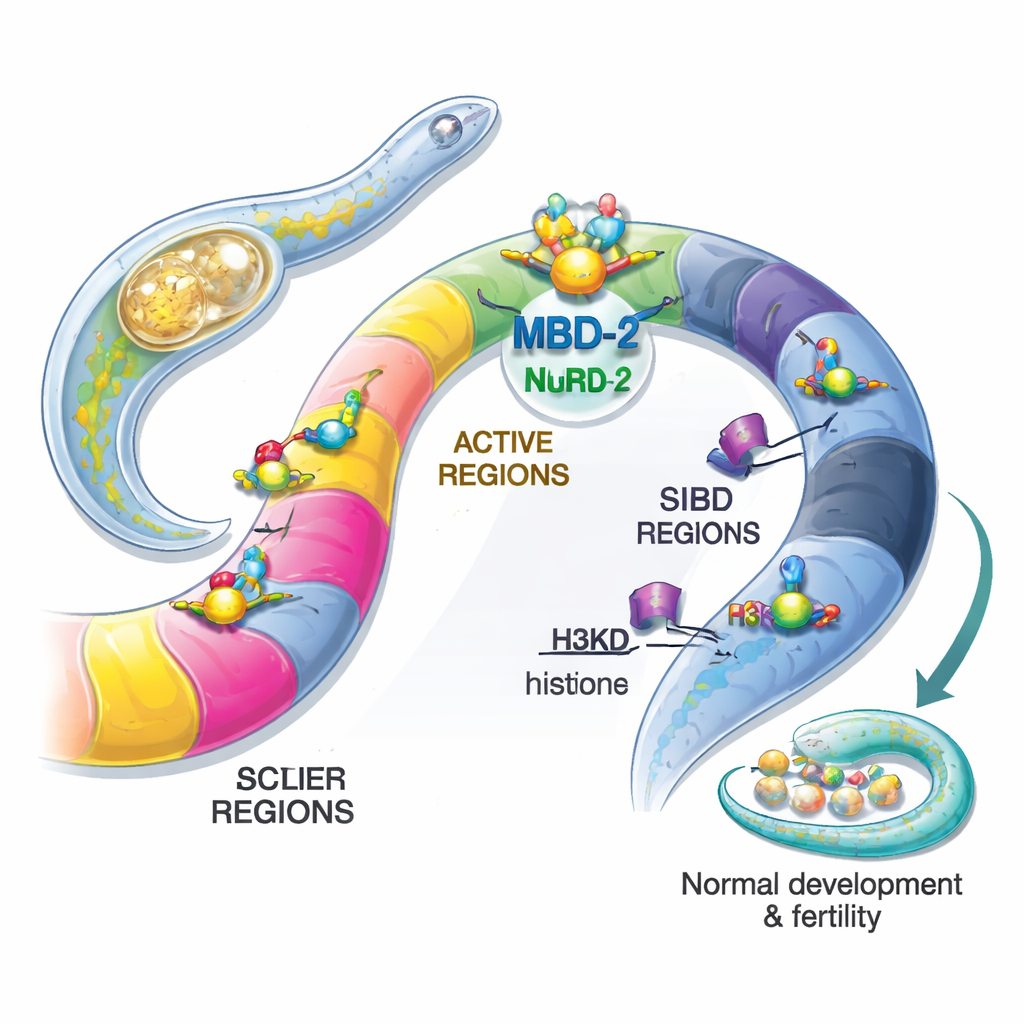
Un marchio del DNA mancante solleva una grande domanda
Nei mammiferi, un marchio chimico chiamato 5‑metilcitosina (5mC) aiuta a silenziare geni durante lo sviluppo, l’inattivazione del cromosoma X e la difesa contro elementi trasponibili. Proteine chiamate MBD2 e MBD3 leggono questi marchi e reclutano una grande macchina proteica, il complesso NuRD, che può rimodellare e disattivare porzioni di cromatina. Stranamente, molti invertebrati, compresi C. elegans e la Drosophila, hanno perso 5mC e gli enzimi che la introducono—ma hanno conservato una proteina simile a MBD2/3. Questo pone un rompicapo: perché mantenere un “lettore” della metilazione del DNA in un genoma che non usa più quella marca, e cosa fa invece?
Una proteina impalcatura di cui i vermi non possono fare a meno
Gli autori si sono concentrati sulla versione del verme di questa proteina, chiamata MBD‑2. A differenza dei suoi parenti nei mammiferi, MBD‑2 del verme ha perso il classico dominio di legame alla metilazione che riconosce 5mC, ma conserva segmenti flessibili e coiled‑coil che possono agganciarsi ad altre proteine. Marcando MBD‑2 con etichette fluorescenti, il gruppo ha mostrato che si trova nel nucleo di quasi tutte le cellule per tutta la vita del verme, coerente con un ruolo ampio nella regolazione genica. Usando ingegneria genetica hanno poi creato vermi privi totalmente di MBD‑2, o privi solo della sua regione coiled‑coil, che media il contatto con NuRD. Entrambe le mutazioni causarono problemi gravi: gli animali erano piccoli, si muovevano male, sviluppavano strutture riproduttive malformate e risultavano in gran parte sterili. Ciò dimostra che MBD‑2 è essenziale per lo sviluppo normale e la fertilità, anche in assenza di metilazione del DNA.
Ricostruire la macchina NuRD in un mondo privo di metilazione
Per verificare se MBD‑2 del verme lavori ancora con NuRD, gli autori hanno purificato MBD‑2 marcato da estratti di verme e identificato i suoi partner tramite spettrometria di massa. La maggior parte dei componenti noti di NuRD erano presenti, confermando che MBD‑2 funge da impalcatura centrale in questo complesso, molto come MBD2/3 nei mammiferi. Quando la regione coiled‑coil venne rimossa, molte di queste interazioni vennero perse, in particolare quelle con proteine che rimodellano i nucleosomi. Allo stesso tempo, il sequenziamento dell’RNA su larga scala rivelò che oltre un quarto di tutti i geni del verme modificò la propria attività nei mutanti per MBD‑2, con molte più sequenze che si attivavano rispetto a quelle che si spegnevano. Questo schema indica che MBD‑2, spesso insieme a NuRD, agisce generalmente come repressore per mantenere silenziosi geni inappropriati, pur contribuendo a mantenere l’attività corretta di un sottoinsieme di geni altamente espressi.
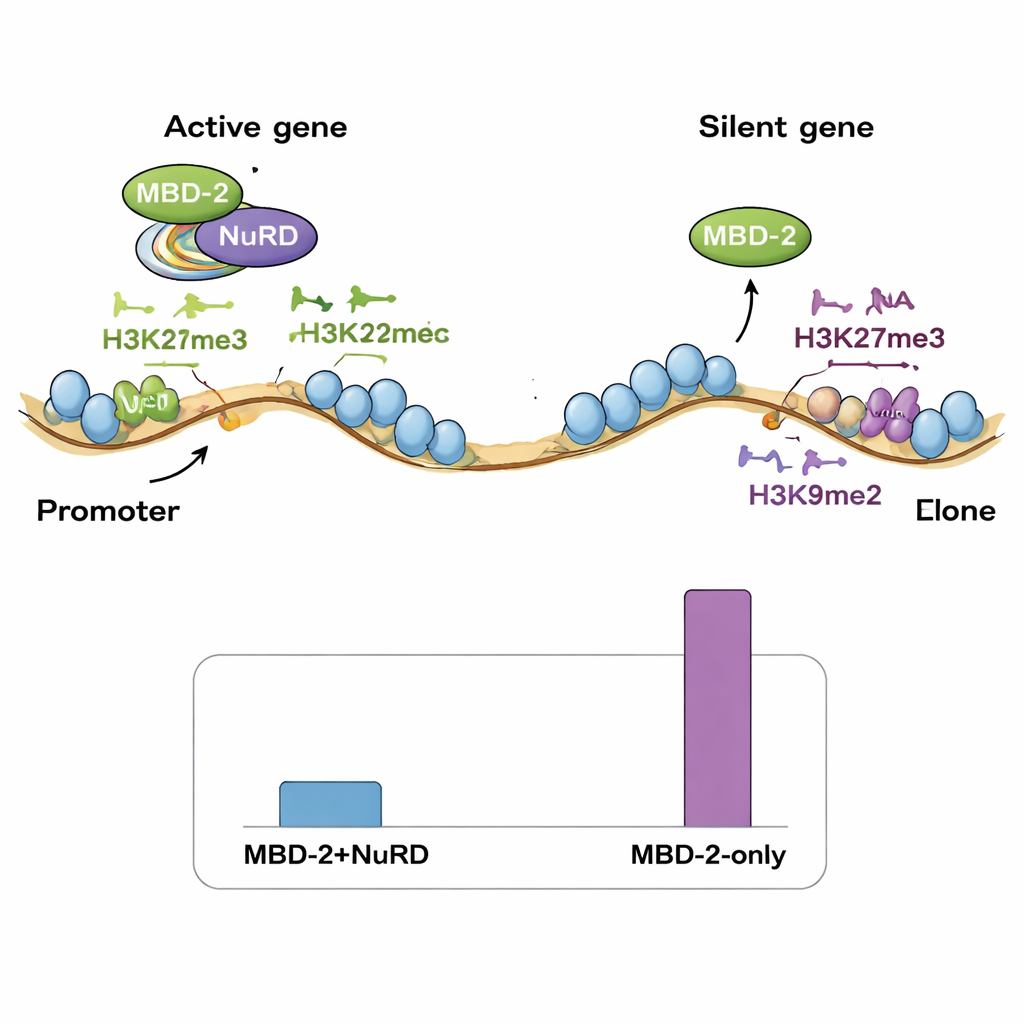
Due modalità di legame sul genoma
Successivamente, il gruppo ha mappato dove MBD‑2 si posiziona lungo il genoma usando ChIP‑seq e ha confrontato queste posizioni con mappe esistenti dei componenti NuRD e di vari marchi istonici. Sorprendentemente, solo una piccola frazione dei siti di MBD‑2 si sovrapponeva strettamente con proteine NuRD e con marchi di cromatina aperta e attiva. La gran parte dei siti di MBD‑2 si trovava altrove, nelle “braccia” cromosomiche ricche di marchi istonici repressivi come H3K27me3 e H3K9me2/3. In altre parole, MBD‑2 mostra un comportamento duplice: in una minoranza di siti viaggia con NuRD per modulare finemente geni attivi, ma in molti più siti si lega indipendentemente in regioni già silenti. Anche il modello di legame all’interno dei geni è importante—quando MBD‑2 si concentra vicino ai siti di inizio del gene, la perdita della proteina tende ad attivare quei geni, mentre il legame più profondo nei corpi genici è spesso associato a una riduzione dell’espressione quando MBD‑2 viene rimosso.
Un backup evolutivo per la metilazione del DNA mancante
Gli autori propongono che, nelle specie che hanno perso la metilazione del DNA, i marchi istonici repressivi—in particolare H3K27me3—possano essersi espansi per occupare un ruolo regolatorio simile. MBD‑2 del verme sembra essere stato riutilizzato: invece di leggere 5mC sul DNA, ora si associa a regioni di cromatina contrassegnate da specifiche modifiche istoniche, pur ancorando ancora il complesso NuRD tramite i suoi domini conservati di interazione proteica. Questo lavoro mostra che un antico strumentario per il silenziamento genico può essere riorientato nel corso dell’evoluzione: il marchio chimico sul DNA può scomparire, ma la macchina proteica associata sopravvive passando a segnali alternativi. Per i non specialisti, il messaggio chiave è che la regolazione genica è straordinariamente adattabile—le cellule possono perdere un importante marchio epigenetico e tuttavia mantenere un controllo complesso di migliaia di geni facendo maggiore affidamento su altri marchi della cromatina e sui ruoli di impalcatura versatili di proteine come MBD‑2.
Citazione: Tsui, H.N., Wong, C.Y.Y., Zheng, C. et al. Dual genomic localizations and gene regulatory functions of MBD-2 with and without NuRD in Caenorhabditis elegans which lacks DNA methylation. Nat Commun 17, 1875 (2026). https://doi.org/10.1038/s41467-026-68592-0
Parole chiave: epigenetica, cromatina, regolazione genica, C. elegans, modificazione degli istoni