Clear Sky Science · it
Un enzima mononucleare non-eme altamente dinamico per la biosintesi in due fasi dell’isonitrile
Come i batteri costruiscono strumenti chimici esotici
Gli isonitrili sono piccoli ma potenti gruppi chimici che si comportano come coltellini svizzeri: possono legare metalli, reagire in modi diversi e spesso fungono da «testata» in potenti antibiotici e tossine naturali. Alcuni batteri patogeni, incluso l’agente della tubercolosi Mycobacterium tuberculosis, aggiungono isonitrili a molecole lipidiche per aiutarli a sottrarre metalli all’ospite. Questo articolo esplora come uno dei loro enzimi, chiamato Rv0097, realizzi questa chimica particolarmente impegnativa in due fasi finemente coreografate.
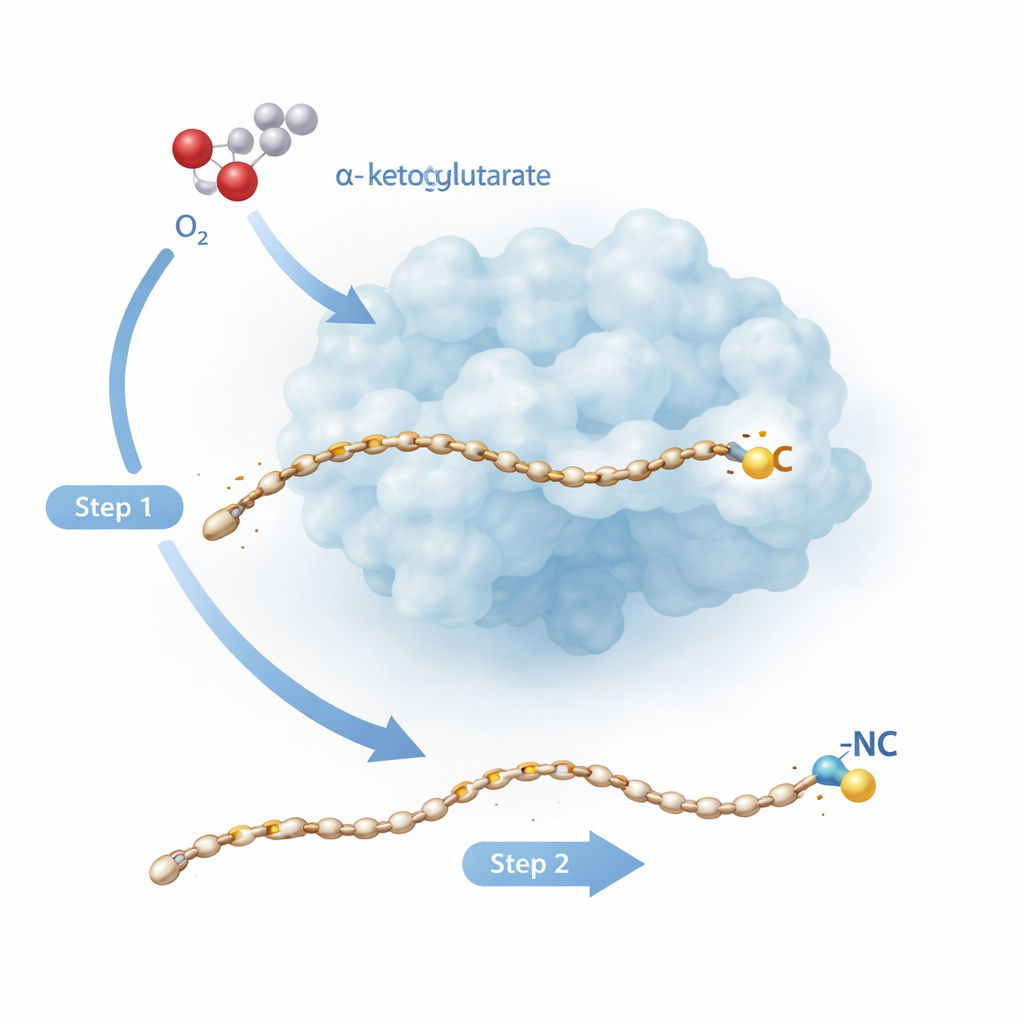
Una trasformazione molecolare in due passaggi
Rv0097 appartiene a una grande famiglia di enzimi dipendenti dal ferro che normalmente svolgono compiti più semplici, come l’introduzione di ossigeno in un singolo punto di una molecola. Qui il compito è più arduo: a partire da un blocco di costruzione «glicil–acido grasso», l’enzima deve generare un nuovo gruppo isonitrile, con entrambi gli atomi chiave — il carbonio e l’azoto — provenienti dallo stesso piccolo frammento di glicina. Lavori precedenti su un enzima correlato, ScoE, suggerivano che ciò non possa avvenire in un unico colpo. Sono necessarie invece due «mezzecicli» di reazione separati, ciascuno alimentato da una specie ferro‑ossigeno formata quando l’enzima scinde una molecola helper chiamata α‑chetoglutarato e la combina con l’ossigeno dell’aria. Il nuovo studio si concentra sull’enzima della tubercolosi Rv0097 per osservare, a risoluzione atomica, come un enzima possa concatenare questi due passaggi radicalari sullo stesso substrato senza perdere il controllo.
Congelare l’enzima in azione
Utilizzando la cristallografia a raggi X, i ricercatori hanno catturato sedici istantanee ad alta risoluzione di Rv0097 in stati diversi: vuoto, legato al suo substrato grasso (una molecola a dieci atomi di carbonio chiamata CADA), legato al co‑fattore α‑chetoglutarato e in combinazioni che imitano intermedi transitori della reazione. Queste strutture mostrano che Rv0097 ha una personalità divisa. A riposo, il suo sito attivo è per lo più chiuso, con un amminoacido chiave (fenilalanina 102) che ruota tra due orientamenti mantenendo la tasca per la lunga coda lipidica asciutta e pronta per il legame idrofobico. Quando si lega CADA, questo residuo scatta in un unico orientamento e la «testa» polare del substrato viene ancorata da catene laterali cariche mentre la sua coda oleosa si adagia in un tunnel avvolgente. Mutare questa coppia di residui di controllo (F102 e una glicina vicina, G204) ostruisce la tasca o lascia entrare troppa acqua, riducendo nettamente l’attività e modificando le lunghezze di catena preferite dall’enzima.
Coperture mobili e anse dinamiche
Oltre alla tasca per il substrato, Rv0097 si comporta come una piccola macchina con porte mobili. Il team ha osservato conformazioni «aperte» e «chiuse» in cui due regioni simili a coperchi oscillano separate o insieme sopra il sito attivo. L’apertura espone il centro di ferro e crea una via per l’ingresso di α‑chetoglutarato e substrato; la chiusura protegge la chimica dall’acqua circostante una volta avviata la reazione. Due anse superficiali flessibili, chiamate ansa His e ansa Arg in riferimento all’istidina e all’arginina che portano, agiscono come una porta aggiuntiva. In alcune strutture queste anse si avvicinano in modo che il residuo di arginina possa afferrare l’α‑chetoglutarato; in altre si allontanano, apparentemente creando un canale laterale attraverso il quale i frammenti helper consumati (succinate e anidride carbonica) possono uscire e un nuovo α‑chetoglutarato può entrare per il secondo passaggio — il tutto mentre l’intermedio derivato dal substrato rimane fissato al suo posto.
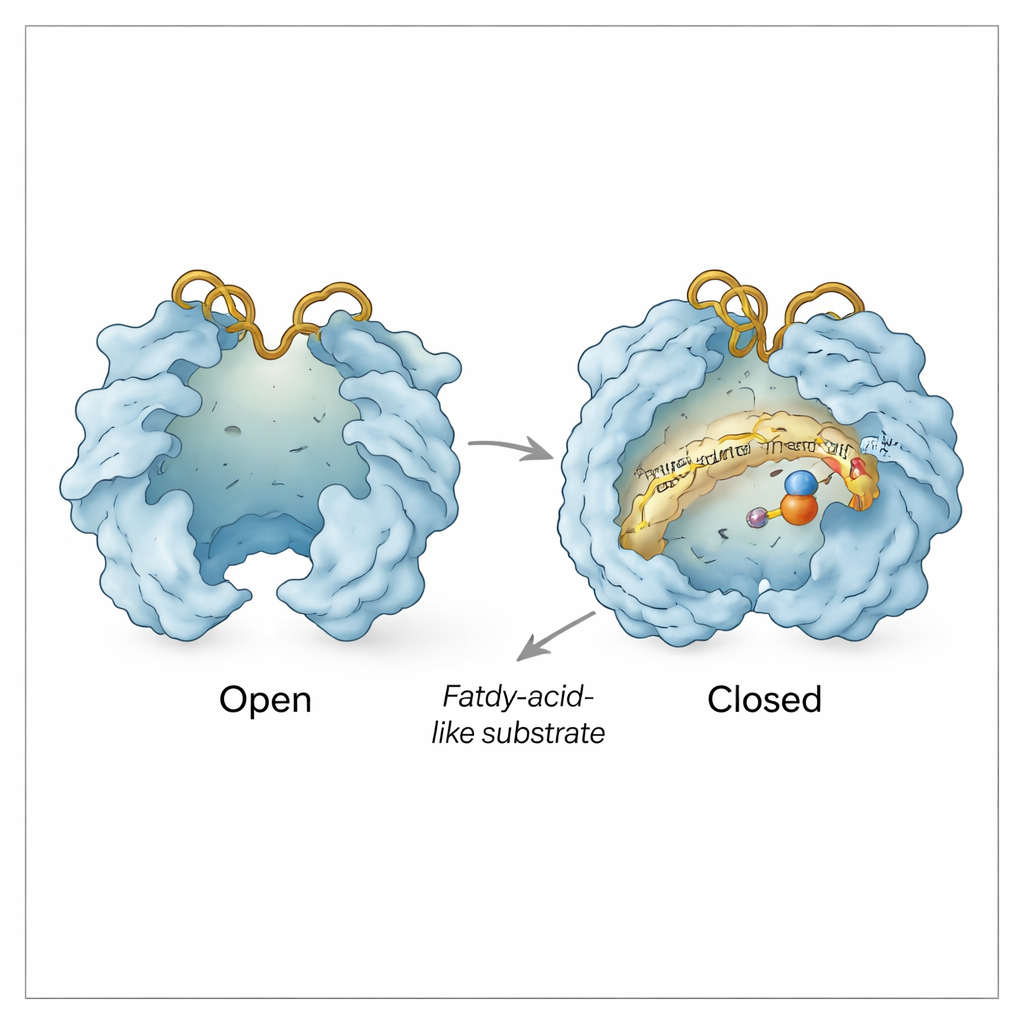
Proteggere un intermedio fragile
Saggezza biochimica sostiene questo quadro strutturale. La prima metà della reazione converte CADA in un intermedio immina altamente reattivo che si degraderebbe rapidamente se finisse in soluzione. Trappolando chimicamente il suo prodotto di degradazione, gli autori mostrano che la maggior parte di questo intermedio viene rilevata solo quando l’enzima è ancora presente, il che implica che rimane legato e protetto all’interno di Rv0097 tra i due mezzecicli. Le strutture spiegano il come: un sottile riposizionamento delle anse His e Arg, insieme a piccoli spostamenti di residui vicini, sembra sigillare l’intermedio in una cavità riparata permettendo al contempo a piccole molecole come α‑chetoglutarato, succinato e anidride carbonica di scambiare attraverso canali controllati.
Perché questo conta per la TB e oltre
Nel complesso, questi risultati rivelano Rv0097 come una linea di assemblaggio altamente dinamica, a proteina singola, che utilizza per due volte di seguito la chimica a base di ferro sullo stesso substrato senza mai rilasciare un pericoloso prodotto intermedio. Per i batteri della tubercolosi, questa precisione sostiene la fabbricazione di molecole decorate con isonitrili che li aiutano a ottenere metalli essenziali all’interno dell’ospite, e studi genetici indicano che la via è importante per la loro sopravvivenza durante l’infezione. Per i chimici e i progettisti di farmaci, il lavoro offre un modello per ingegnerizzare enzimi correlati per costruire nuovi composti contenenti isonitrili e suggerisce che interferire con i coperchi e i cancelli mobili di Rv0097 potrebbe essere un modo per sviluppare nuovi antibiotici.
Citazione: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
Parole chiave: biosintesi dell’isonitrile, enzima non-eme a ferro, Mycobacterium tuberculosis, dinamica enzimatica, prodotti naturali che chelano metalli