Clear Sky Science · it
La perturbazione dell'omeostasi del ferro sensibilizza il tumore pancreatico all’elettroporazione irreversibile
Usare elettricità e ferro contro un cancro letale
Il cancro pancreatico è uno dei tumori più difficili da trattare e anche terapie locali aggressive spesso non riescono a impedirne la recidiva. Questo studio esplora un modo nuovo per rendere più efficace e sicura una procedura già esistente — l’elettroporazione irreversibile, che elimina i tumori con brevi impulsi elettrici ad alta potenza. Disturbando in modo mirato la gestione del ferro da parte delle cellule tumorali, i ricercatori dimostrano di poter spingere le cellule sopravvissute verso una forma distruttiva di morte cellulare, riducendo potenzialmente la probabilità che il tumore ricompaia.
Perché i soli impulsi elettrici non bastano
L’elettroporazione irreversibile (IRE) tratta i tumori inserendo sottili elettrodi dentro o intorno alla massa tumorale e sparando impulsi rapidi ad alta tensione. Questi impulsi perforano permanentemente le membrane cellulari, uccidendo molte cellule tumorali e innescando una risposta immunitaria. Tuttavia il campo elettrico non è perfettamente omogeneo. Aree che ricevono impulsi leggermente più deboli possono lasciare cellule tumorali vive, e questi sopravvissuti possono dare origine a un nuovo tumore. Analizzando più da vicino cellule di cancro pancreatico e tumori murini esposti a un campo elettrico sub-letale, il team ha osservato che invece di morire per un processo guidato dal ferro chiamato ferroptosi, queste cellule attivavano un ampio programma di difesa antiossidante. Gene chiave di protezione, inclusi quelli che neutralizzano i danni legati al ferro, risultavano sovraespressi, permettendo alle cellule di resistere allo stress e riprendersi.
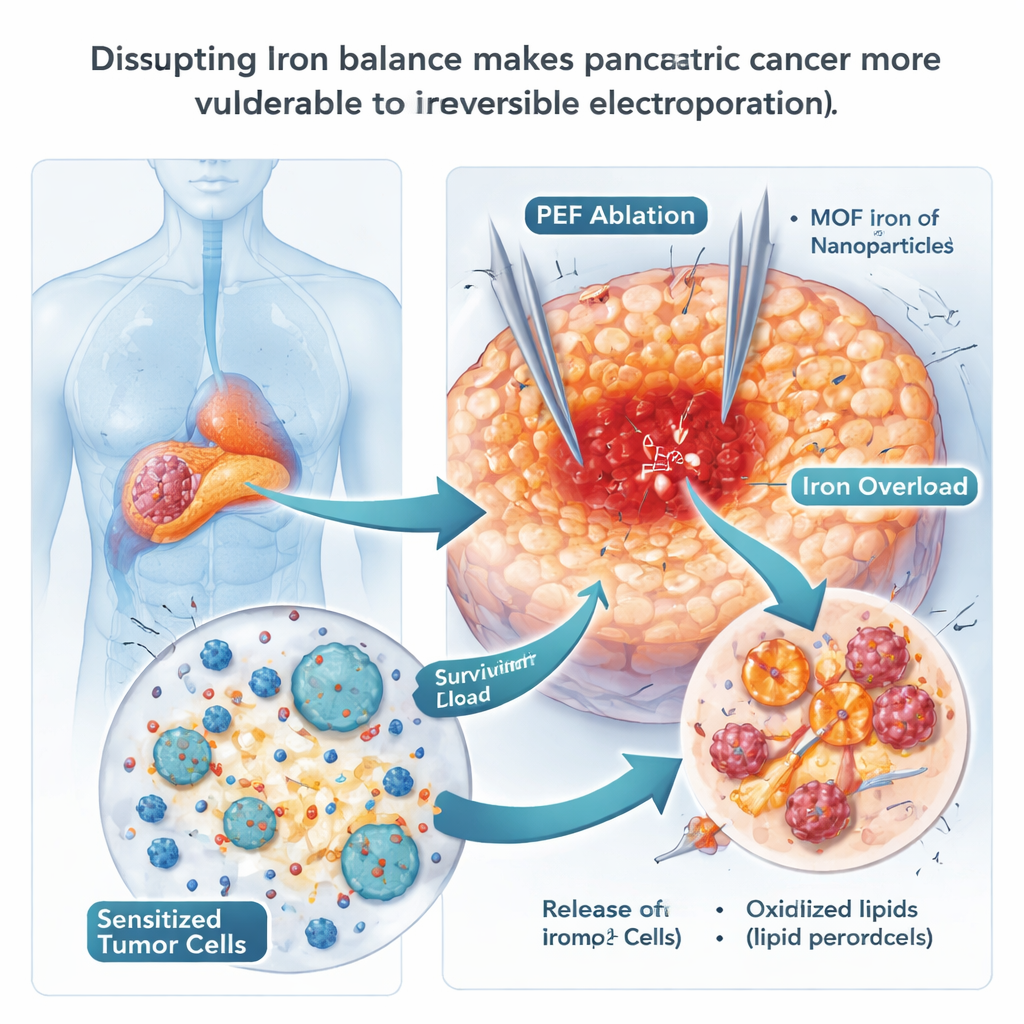
Usare nanoparticelle di ferro per spingere le cellule verso la distruzione
Poiché la ferroptosi dipende dal ferro, gli scienziati hanno testato se nanoparticelle ricche di ferro potessero portare le cellule tumorali oltre il limite di sopravvivenza. Hanno impiegato particelle a struttura metallo-organica contenenti ferro (MOF-Fe), che rilasciano rapidamente ferro all’interno dei compartimenti acidi delle cellule. In colture cellulari, le cellule di cancro pancreatico che hanno assorbito queste particelle accumulavano ferro libero e lipidi ossidati nelle membrane, segnali classici di ferroptosi, e formavano molte meno colonie. Nei topi, la combinazione di MOF-Fe con IRE ha ritardato la ricrescita tumorale più a lungo rispetto a ciascun trattamento singolo, e i tumori mostravano maggiori segni di danno ossidativo. Tuttavia questo beneficio è stato temporaneo: dopo circa tre settimane i tumori hanno cominciato a riprendersi, suggerendo che il cancro avesse trovato un modo per adattarsi al sovraccarico di ferro.
Colpire la “cassaforte” del ferro nella cellula
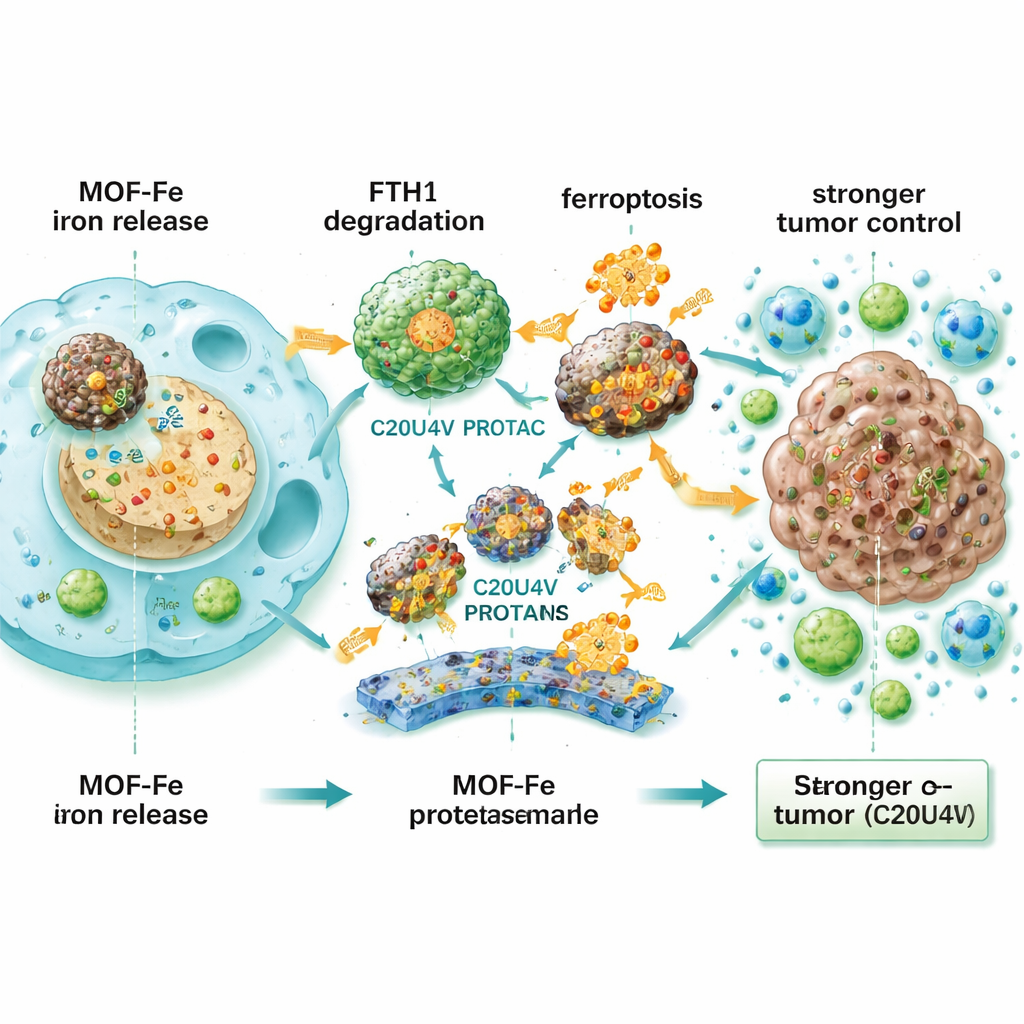
Per capire questa resistenza, il team ha analizzato quali proteine cambiavano dopo il trattamento con MOF-Fe. Una proteina emersa con evidenza è stata la catena pesante della ferritina 1 (FTH1), parte del complesso di immagazzinamento del ferro della cellula — l’equivalente molecolare di una cassaforte ignifuga per il ferro in eccesso. Quando i livelli di FTH1 venivano aumentati sperimentalmente, le cellule tumorali diventavano più resistenti alla ferroptosi; quando FTH1 veniva ridotta, diventavano più vulnerabili. Questo ha indicato FTH1 come uno scudo centrale contro la morte mediata dal ferro. I ricercatori hanno quindi creato una molecola progettata, C20U4V, composta da acido arachidonico (un lipide altamente ossidabile) legato a uno scheletro PROTAC che indirizza proteine specifiche al sistema di smaltimento cellulare. In presenza di MOF-Fe, C20U4V legava la ferritina e ne favoriva il suo tagging e la successiva degradazione, riducendo nettamente i livelli di FTH1 e impedendo alla cellula di mettere al sicuro il ferro.
Dalle colture ai mini-tumori e ai topi
Quando MOF-Fe e C20U4V venivano combinati, le cellule di cancro pancreatico mostravano maggiore stress ossidativo, lipidi di membrana più danneggiati, mitocondri compromessi e notevole riduzione della capacità di ricrescita. Questa sinergia è stata osservata anche in organoidi tridimensionali derivati da pazienti — piccole strutture tumorali cresciute da campioni clinici — dove la coppia di farmaci ha collassato dimensione e numero degli organoidi. Poiché C20U4V è lipofilo e non si dissolve in acqua, il team lo ha incapsulato in micelle sensibili al perossido di ossigeno (M-C20U4V) che circolano nel sangue e rilasciano il farmaco nei tessuti tumorali stressati o danneggiati. In modelli murini con tumori pancreatici sottocutanei e nel pancreas, una combinazione tripla di IRE, MOF-Fe e M-C20U4V ha ridotto i tumori molto più efficacemente e ha prolungato la sopravvivenza rispetto a qualsiasi singolo o doppio trattamento. I tumori trattati presentavano meno cellule in divisione, più marcatori di ferroptosi e maggiore infiltrazione di cellule T e altre cellule immunitarie, indicando che la strategia non solo uccide direttamente le cellule tumorali ma aiuta anche il sistema immunitario a riconoscere e attaccare il tumore.
Cosa potrebbe significare per i pazienti
Per un lettore non specialista, l’idea chiave è semplice: i tumori pancreatici spesso sfuggono dopo l’ablazione con impulsi elettrici perché alcune cellule sopravvivono e si adattano rapidamente. Questo lavoro mostra che caricare quelle cellule di ferro e disattivare contemporaneamente la loro “cassaforte” per il ferro può costringerle in uno stato autodistruttivo che difficilmente possono contrastare. Pur essendo ancora a livello sperimentale e richiedendo ampi test di sicurezza e fattibilità nell’uomo, l’approccio suggerisce che modulare finemente come i tumori gestiscono un elemento fondamentale come il ferro potrebbe trasformare un trattamento locale imperfetto in un colpo più decisivo contro uno dei tumori più letali.
Citazione: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
Parole chiave: cancro pancreatico, elettroporazione irreversibile, ferroptosi, nanoparticelle di ferro, terapia PROTAC