Clear Sky Science · it
HIF mantengono un circuito di regolazione trascrizionale dell’espressione di EPAS1 nel carcinoma renale a cellule chiare
Perché il cancro del rene merita uno sguardo più attento
Il carcinoma renale a cellule chiare è la forma più comune di tumore del rene, e molti pazienti oggi ricevono farmaci che bloccano una proteina chiamata HIF‑2α. Questi medicinali possono ridurre le dimensioni dei tumori, ma non funzionano allo stesso modo per tutti. Questo studio pone una domanda semplice ma importante: cosa spinge alcuni tumori renali a produrre così tanta HIF‑2α, e capire questo “interruttore” può aiutarci a prevedere chi trarrà più beneficio dal trattamento e come progettare nuove terapie?
Il sensore di ossigeno che va fuori controllo
Le cellule renali sane utilizzano una proteina di sicurezza chiamata VHL per mantenere sotto stretto controllo i fattori di risposta all’ossigeno, noti come HIF. Quando l’ossigeno è abbondante, VHL marca le proteine HIF per la distruzione, impedendo loro di attivare geni che favoriscono la formazione di vasi sanguigni e la divisione cellulare. Nel carcinoma renale a cellule chiare, VHL è di solito perso o danneggiato. Di conseguenza, un membro della famiglia HIF, HIF‑2α (codificato dal gene EPAS1), sfugge alla distruzione e si accumula. Lavori precedenti avevano mostrato che un’alta attività di HIF‑2α è collegata a una crescita tumorale più rapida e a risultati peggiori, e che bloccare HIF‑2α può rallentare o fermare i tumori in alcuni pazienti. Tuttavia, i passaggi molecolari che aumentano l’attività del gene EPAS1 nei tumori renali non erano ben compresi.
Un interruttore del DNA nascosto per un gene del cancro
Usando campioni tumorali dei pazienti, dati a cellula singola e modelli cellulari di cancro, gli autori mostrano che l’RNA messaggero di HIF‑2α è marcatamente più alto nei tumori renali a cellule chiare rispetto al tessuto renale normale o ad altri tipi di tumore renale. Hanno quindi passato al setaccio la regione genomica di EPAS1 alla ricerca di marche chimiche e strutturali che segnalano DNA regolatorio attivo. Questo ha rivelato un potente potenziatore—una specie di interruttore genico a lunga distanza—situato a circa 70.000 basi di DNA a monte di EPAS1 che è specificamente attivo nei tumori a cellule chiare. Nelle cellule tumorali, la cromatina in corrispondenza di questo potenziatore è aperta, decorata con marche di attivazione e si avvolge fisicamente per contattare il promotore di EPAS1, mentre nelle cellule normali dei tubuli renali questa regione è in gran parte silente. L’attività di questo potenziatore correla con livelli più alti di EPAS1 in grandi set di dati sul cancro. 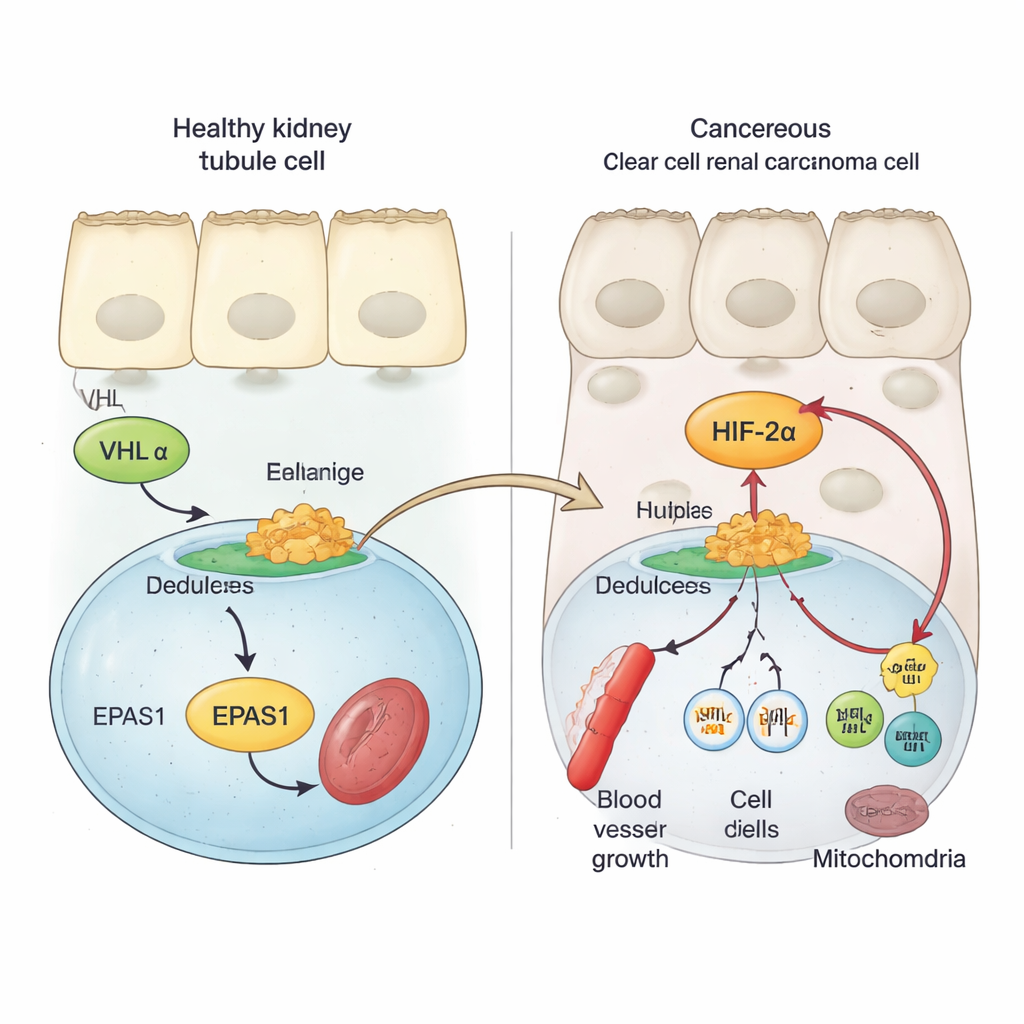
Un circuito auto‑rinforzante guidato da fattori d’identità renale
Lo studio scopre che le proteine HIF fanno più che rispondere alla carenza di ossigeno: contribuiscono effettivamente a promuovere la propria produzione. Quando i ricercatori ripristinano VHL o rimuovono una proteina partner chiave di HIF (HIF‑1β), i livelli di EPAS1 diminuiscono e il potenziatore diventa meno accessibile. La mappatura diretta dei contatti proteina–DNA mostra che HIF si lega a due regioni potenziatrici a monte di EPAS1, incluso il potenziatore specifico per le cellule chiare. Nelle cellule tumorali renali, questo potenziatore è anche occupato da PAX8 e HNF‑1β, fattori di trascrizione che contribuiscono a definire l’identità delle cellule renali e che sono noti per sostenere la crescita tumorale. Disgregare PAX8 o HNF‑1β, o mutare i loro siti di legame all’interno del potenziatore, riduce l’RNA e la proteina di HIF‑2α e indebolisce l’attività del potenziatore. Nel complesso, questi risultati rivelano un circuito auto‑regolatorio: HIF‑2α, lavorando con i fattori di linea renale, aumenta l’attività di un potenziatore di EPAS1, che a sua volta guida una maggiore produzione di HIF‑2α.
Rischio genetico e comportamento tumorale convergono sullo stesso circuito
La regione di EPAS1 è stata a lungo segnalata negli studi genome‑wide come un punto caldo per il rischio di cancro renale, con alcune varianti ereditarie associate a tassi più elevati di cancro e a mutazioni di VHL nei tumori. Combinando dati genetici con misure di espressione genica, gli autori mostrano che gli individui portatori della versione ad alto rischio di una variante chiave di EPAS1 tendono ad avere livelli più elevati di HIF‑2α nei loro tumori—e persino nelle cellule normali dei tubuli renali quando HIF è sperimentalmente stabilizzato. Ciò suggerisce che differenze ereditarie nel DNA possono regolare quanto intensamente il potenziatore risponde, predisponendo alcuni reni ad aumentare HIF‑2α più rapidamente una volta persa la funzione di VHL. Esperimenti in cellule di glioblastoma mostrano che lo stesso potenziatore può essere attivato anche in alcuni tumori cerebrali, suggerendo che questo modulo regolatorio potrebbe essere riutilizzato in altri tumori in cui HIF‑2α è rilevante. 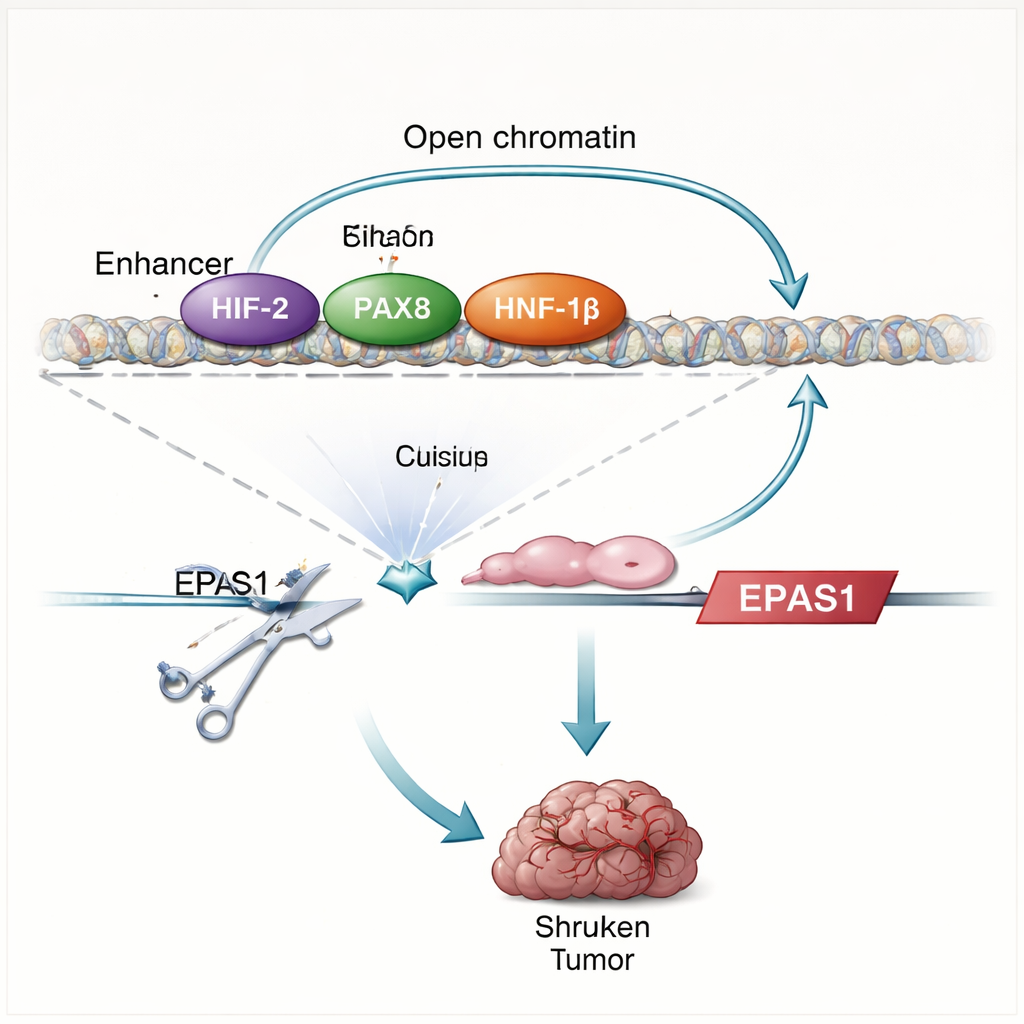
Interrompere il circuito per fermare la crescita tumorale
Per testare quanto sia essenziale questo potenziatore, il gruppo usa l’editing genomico CRISPR per danneggiare i motivi di legame di HIF al suo interno in linee cellulari di carcinoma renale e in cellule tumorali fresche prelevate dai pazienti. Questo taglio riduce l’RNA di HIF‑2α di circa un terzo fino a metà, abbassa i livelli di geni noti bersaglio di HIF‑2α come CCND1 e VEGFA e indebolisce il più ampio programma genetico dell’ipossia. Quando le cellule modificate sono impiantate nei topi, per lo più non riescono a formare tumori, in netto contrasto con le cellule controllo. Il pattern di cambiamenti genici dopo la distruzione del potenziatore rispecchia da vicino gli effetti del blocco diretto di HIF‑2α con un farmaco clinico, sottolineando che questo singolo elemento del DNA è un importante motore della via HIF‑2α in questi tumori.
Cosa significa per i pazienti e le terapie
Per i non specialisti, il messaggio chiave è che gli autori hanno scoperto un interruttore del DNA auto‑amplificante che mantiene attiva una proteina promotrice del cancro di primo piano, HIF‑2α, nei tumori renali a cellule chiare. Questo interruttore dipende sia dalla perdita del freno di sicurezza VHL sia da proteine helper specifiche del rene, ed è influenzato da varianti genetiche ereditarie. Poiché il potenziatore è altamente attivo in molti tumori a cellule chiare ed è strettamente collegato all’intensità della via HIF‑2α, misurarne l’attività—o colpirlo direttamente—potrebbe aiutare a identificare i pazienti che trarranno maggior beneficio dagli attuali inibitori di HIF‑2α e offrire nuove strategie per spegnere questa via quando i tumori diventano resistenti ai farmaci.
Citazione: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
Parole chiave: carcinoma renale a cellule chiare, HIF-2α, potenziatore di EPAS1, mutazione VHL, genetica del cancro renale