Clear Sky Science · it
Reazione CuAAC interrotta atroposelettiva usando diariliodonii ciclici
Perché questa nuova chimica è importante
I chimici si sono a lungo affidati a una semplice reazione “click” per unire velocemente e pulitamente blocchi molecolari, un espediente che supporta tutto, dalla scoperta di farmaci ai materiali autoriparanti. Questo articolo descrive una variante intelligente di quella reazione classica che permette agli scienziati di costruire molecole tridimensionali più complesse con una mano precisa — strutture molto ricercate nei farmaci moderni e nei materiali avanzati.
Affidare un nuovo compito a una reazione click classica
Il punto di partenza è la cicloaddizione azide–alchino catalizzata da rame, spesso chiamata semplicemente CuAAC. Essa unisce due componenti piccoli — un azide e un alchino — in un anello a cinque termini chiamato triazolo in condizioni miti e con notevole affidabilità. Tradizionalmente, una volta che il rame aiuta a formare l’anello del triazolo, la reazione si conclude. Negli ultimi anni, però, i chimici hanno imparato a “interrompere” questo processo, catturando un effimero intermedio rame–triazolo con un terzo partner per costruire prodotti più elaborati. Finora, tali interruzioni non erano in grado di controllare la mano molecolare (chiralità) in modo generale, limitandone l’utilità per la sintesi di molecole chirali sofisticate.
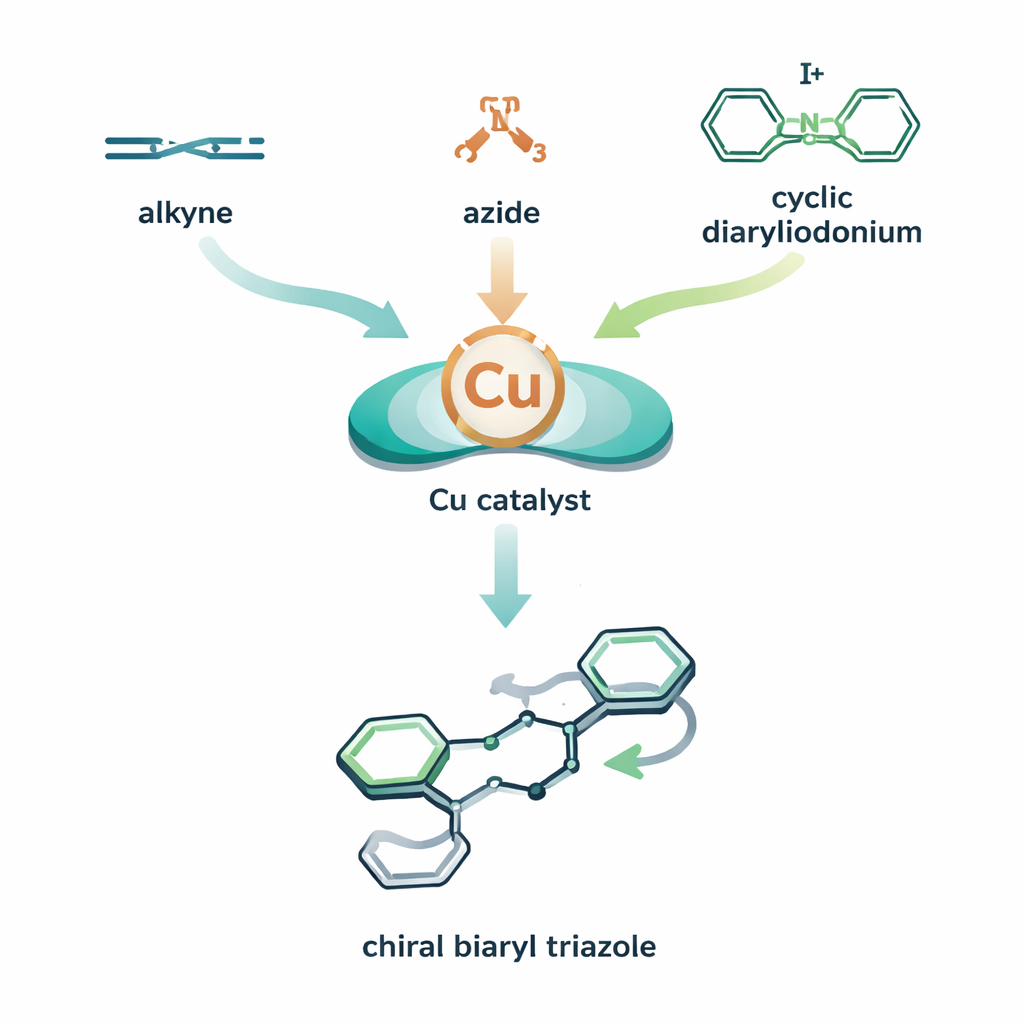
Un puzzle molecolare a tre pezzi con una torsione
Gli autori combinano due cicli di reazione a base di rame in un unico processo orchestrato. Nel loro disegno, un catalizzatore a rame aiuta prima l’alchino e l’azide a formare un intermedio rame–triazolo. Prima che questo intermedio venga neutralizzato, viene introdotto un terzo componente — una molecola anulare, altamente reattiva e contenente iodio, chiamata diariliodonio ciclico. Il rame si inserisce in questo anello e poi lo apre, cucendo uno dei suoi anelli aromatici sul triazolo. Il risultato è un triazolo biarilico: due sistemi ad anello uniti attorno a un legame che può comportarsi come un asse chirale, molto simile a un’elica che può torcersi a sinistra o a destra. Accoppiando il rame a un ligando chirale accuratamente scelto, il gruppo induce un bias nel processo così che una torsione si formi molto più dell’altra, ottenendo un’elevata atroposelettività (controllo su quale “mano” assiale si forma).
Valutare flessibilità e affidabilità del metodo
Per capire quanto fosse generale questa reazione, i ricercatori hanno variato sistematicamente ciascuno dei tre mattoni. Hanno mostrato che molti alchini diversi, compresi quelli con anelli ricchi di elettroni, poveri di elettroni e eteroaromatici, possono partecipare offrendo comunque buone rese e una forte preferenza per una forma chirale. Alcune sostituzioni voluminose hanno migliorato la selettività ma talvolta ridotto la resa, rivelando un compromesso tra ingombro sterico ed efficienza. I partner azidici hanno lavorato meglio se derivati da semplici gruppi estere o ammide o da posizioni benziliche, e una gamma di tali azidi ha fornito prodotti chirali fortemente arricchiti. Anche il componente diariliodonio ciclico è stato suscettibile di messa a punto: alcune sostituzioni hanno preservato sia la resa sia la selettività, mentre altre, soprattutto nelle vicinanze del centro reattivo di iodio, hanno rallentato la reazione o ne hanno ridotto le prestazioni. Nel complesso, lo studio ha fornito una vasta collezione di nuovi triazoli biarilici atropoisomerici accessibili in un solo passaggio.
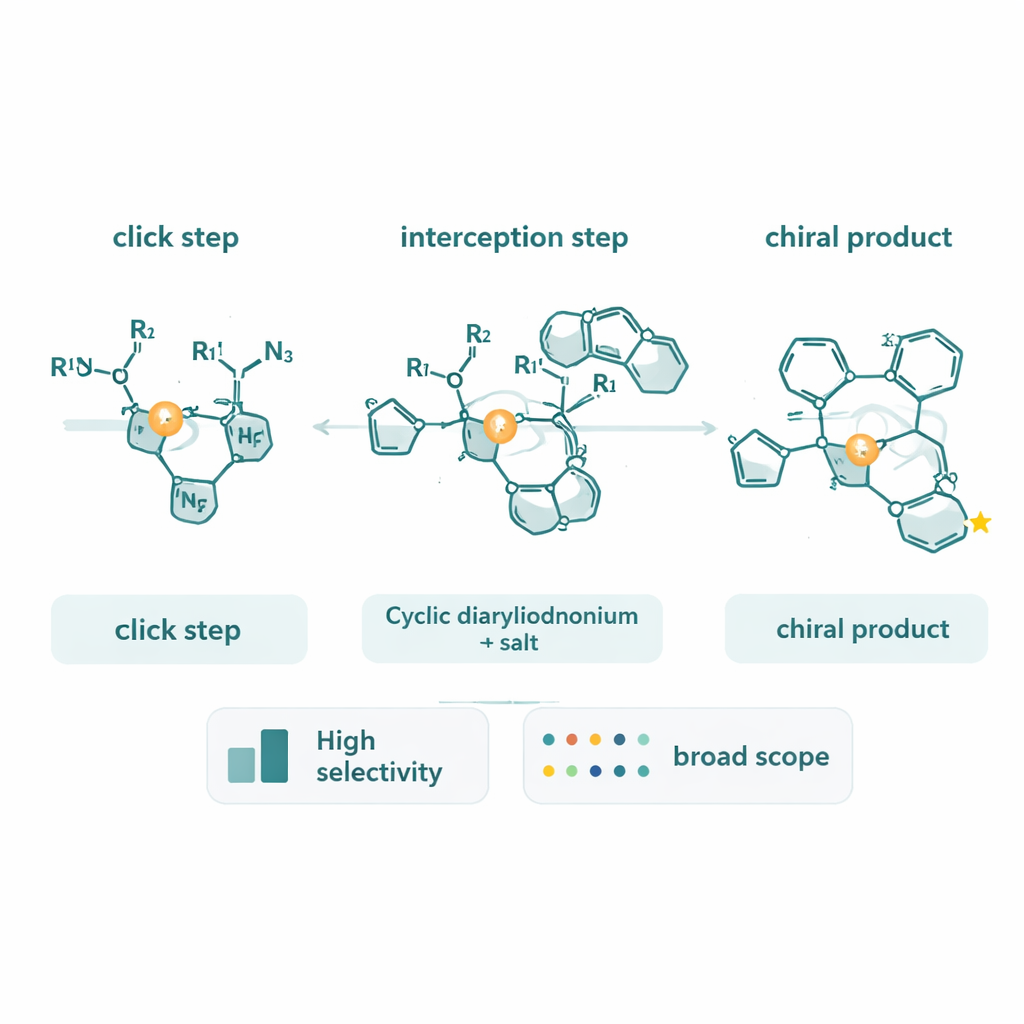
Dare uno sguardo al meccanismo della reazione
Oltre a sintetizzare nuove molecole, il team ha dedicato notevole impegno a comprendere come la reazione lavori effettivamente. Usando alchini marcati con deuterio, hanno osservato un insolito effetto cinetico isotopico inverso, che indica un passo limitante in cui il carbonio dell’alchino cambia il suo carattere di legame piuttosto che limitarsi a rompere un legame C–H. Analisi del progresso della reazione basata su calorimetria ha mostrato che la velocità dipende fortemente dalle concentrazioni di alchino e azide, ma solo debolmente dal diariliodonio ciclico. Queste misure supportano un quadro in cui la formazione e la trasformazione del complesso rame–triazolo, e la sua addizione ossidativa nell’anello del diariliodonio, fissano insieme il ritmo della reazione. Hanno anche scoperto che i prodotti triazolici chirali stessi possono legarsi al rame e rallentare il catalizzatore, suggerendo strategie per ottimizzare ulteriormente il sistema.
Cosa significa per il futuro
In termini pratici, i ricercatori hanno insegnato a una reazione click ben nota un nuovo trucco: invece di limitarsi a unire due pezzi, ora aiuta ad assemblare tre componenti in molecole complesse a forma di elica scegliendo quasi esclusivamente una torsione preferita. Questo fornisce una via scalabile verso triazoli biarilici chirali, strutture preziose come potenziali molecole farmaceutiche, catalizzatori e materiali funzionali. Le intuizioni meccanicistiche — in particolare su come l’intermedio chiave viene intercettato e su come il prodotto può “avvelenare” il catalizzatore — offrono una road map per progettare versioni ancora più efficienti e selettive di questa chimica. Per i non specialisti, il punto chiave è che uno strumento molecolare tipo “Lego” già potente è appena diventato più versatile, permettendo ai chimici di costruire forme più intricate e utili con un controllo fine sulla loro struttura tridimensionale.
Citazione: Li, Y., Yang, S., Duan, L. et al. Atroposelective interrupted CuAAC reaction using cyclic diaryliodoniums. Nat Commun 17, 944 (2026). https://doi.org/10.1038/s41467-026-68574-2
Parole chiave: chimica click, catalisi con rame, biarile chirale, atroposomero, triazolo