Clear Sky Science · it
Biomarcatori di risposta al trattamento neoadiuvante con palbociclib più anastrozolo in carcinoma mammario ER-positivo/HER2-negativo resistente alla terapia endocrina: uno studio di fase 2
Perché questa ricerca è importante per pazienti e famiglie
Molte donne con una forma comune di cancro al seno rispondono inizialmente bene ai farmaci che bloccano gli ormoni, per poi vedere i loro tumori diventare resistenti e ricominciare a crescere. Questo studio pone una domanda cruciale: aggiungere un farmaco più recente che blocca il ciclo cellulare alla terapia ormonale standard può aiutare in questi casi difficili da trattare, e possiamo individuare segnali nel tumore che prevedano chi trarrà beneficio e chi no?
Uno sguardo più approfondito ai tumori ostinati
Lo studio si è concentrato sui carcinomi mammari con recettore per gli estrogeni positivi e HER2‑negativi, il sottotipo più frequente. Tutte le 34 pazienti avevano già ricevuto la terapia ormonale preoperatoria standard (un inibitore dell’aromatasi) ma mostravano ancora attività di proliferazione cellulare, perciò il cancro era considerato “resistente alla terapia endocrina”. I ricercatori hanno quindi trattato queste pazienti prima della chirurgia con la combinazione del farmaco ormonale anastrozolo e del bloccante del ciclo cellulare palbociclib. Hanno valutato la velocità di divisione delle cellule tumorali usando un marcatore chiamato Ki67. Se Ki67 scendeva a livelli molto bassi dopo due settimane, il tumore veniva definito in “arresto completo del ciclo cellulare”, indicando che la divisione delle cellule tumorali era stata efficacemente interrotta.
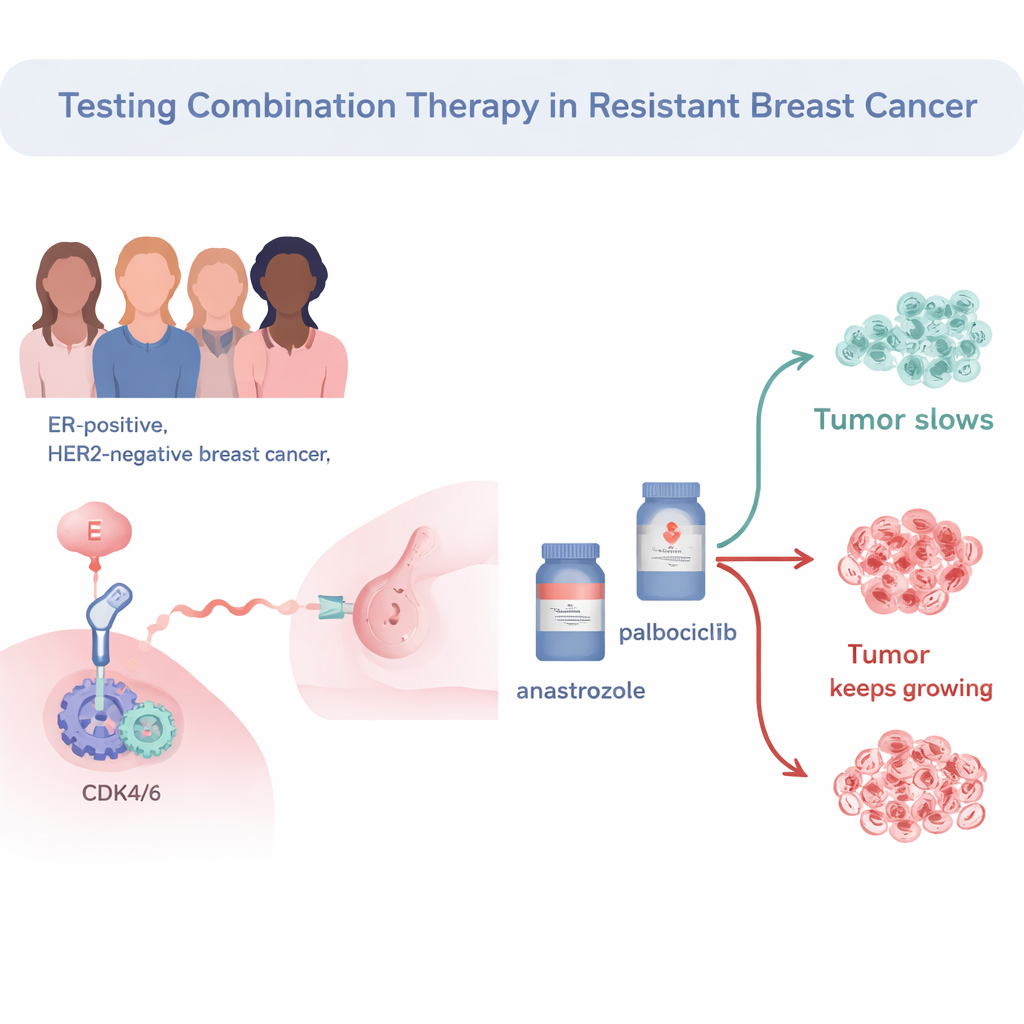
Chi ha risposto alla combinazione farmacologica?
Tra le 33 pazienti i cui tumori sono stati valutati completamente, il 57,6% ha raggiunto l’arresto completo del ciclo cellulare dopo appena due settimane di trattamento combinato. Usando una soglia più modesta—classificando semplicemente i tumori come “sensibili” se Ki67 scendeva sotto il 10%—circa due terzi dei tumori sono stati ritenuti responsivi. Le pazienti i cui tumori mantenevano un alto valore di Ki67 tendevano ad avere tumori più aggressivi: grado più elevato, dimensioni maggiori e valori iniziali di Ki67 più alti. Erano anche più probabili i sottotipi molecolari cosiddetti “non-luminali”, che generalmente si comportano in modo più aggressivo rispetto ai classici tumori “luminal A” guidati dagli ormoni.
Cosa rende alcuni tumori resistenti al trattamento?
Il gruppo ha analizzato i campioni tumorali in profondità con sequenziamento del DNA, sequenziamento dell’RNA e profilazione proteica. I tumori resistenti non erano definiti da una singola mutazione; mostravano invece un quadro di “cablaggio iperattivo”. Rispetto ai tumori sensibili, i tumori resistenti presentavano un segnale del recettore degli estrogeni attenuato ma una maggiore attività in percorsi che guidano la divisione e la crescita cellulare, come i geni del ciclo cellulare, la via di crescita mTOR e diverse reti infiammatorie e legate all’interferone. Mostravano anche livelli più elevati di “freni” immunitari, noti come immune checkpoints, inclusi geni come IDO1 e PD-L1 che possono aiutare i tumori a eludere le difese dell’organismo.
Dai percorsi molecolari a potenziali nuove terapie
Per verificare se questi percorsi iperattivati potessero essere sfruttati contro il cancro, i ricercatori hanno creato modelli cellulari di laboratorio diventati resistenti agli inibitori di CDK4/6 come il palbociclib. Queste cellule resistenti mostravano la stessa firma di potenziamento del ciclo cellulare e della segnalazione interferone/infiammatoria osservata nei tumori delle pazienti. Quando sono state esposte a farmaci che bloccano la segnalazione JAK‑STAT—una via chiave a valle dell’interferone—un medicinale, pacritinib, si è dimostrato particolarmente efficace nel rallentare la crescita delle cellule resistenti e degli organoidi tumorali derivati dalle pazienti. Ciò suggerisce che abbinare gli inibitori di CDK4/6 con alcuni farmaci che mirano JAK potrebbe essere una strategia promettente per le pazienti i cui tumori hanno aggirato le combinazioni attuali.
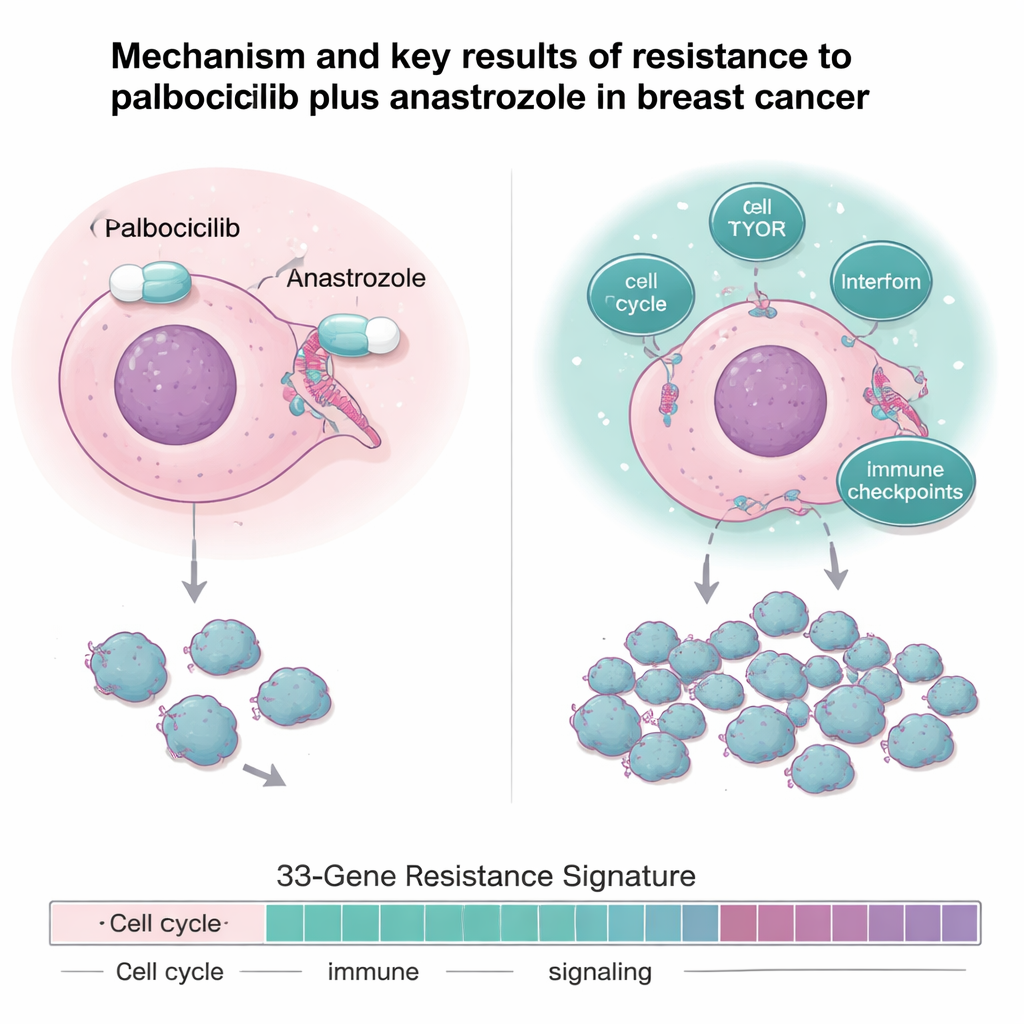
Una impronta genica che predice l’esito
Mettendo a confronto tumori sensibili e resistenti in due studi correlati, gli investigatori hanno costruito una “firma di resistenza” di 33 geni che comprende geni coinvolti nella divisione cellulare, nella riparazione del DNA, nella segnalazione di crescita, nel metabolismo e nelle risposte immunitarie/infiammatorie. Questa impronta genica è stata molto accurata nel distinguere tumori sensibili da resistenti nello studio. Importante, applicando lo stesso schema a 33 geni a un gruppo indipendente di 151 pazienti con carcinoma mammario metastatico trattati nella pratica clinica con inibitori di CDK4/6 più terapia ormonale, coloro i cui tumori avevano un punteggio alto per la firma di resistenza hanno mostrato un tempo più breve prima della progressione della malattia e una sopravvivenza globale ridotta. In altre parole, questo schema genico misurato prima del trattamento potrebbe segnalare le pazienti meno probabilmente beneficiarie a lungo termine dei regimi standard basati su CDK4/6.
Cosa significa per le cure future
Per le persone con carcinoma mammario ER-positivo resistente agli ormoni, questo studio offre sia rassicurazioni sia una mappa di lavoro. Mostra che aggiungere palbociclib all’anastrozolo può ancora bloccare la crescita tumorale in oltre la metà dei casi resistenti. Allo stesso tempo, rivela che alcuni tumori fanno affidamento su percorsi alternativi di crescita e su vie immunitarie, rendendoli più difficili da controllare. La nuova firma di 33 geni e la scoperta che farmaci che prendono di mira JAK come pacritinib possono frenare le cellule resistenti indicano la strada verso terapie più personalizzate: identificare presto chi è meno probabile che risponda alle combinazioni standard e indirizzarle prima verso studi clinici che testino nuovi partner farmacologici che colpiscono direttamente le vie di sopravvivenza alternative del tumore.
Citazione: Kong, T., Mabry, A., Highkin, M. et al. Biomarkers of response to neoadjuvant palbociclib plus anastrozole in endocrine-resistant estrogen receptor-positive/HER2-negative breast cancer: a phase 2 trial. Nat Commun 17, 949 (2026). https://doi.org/10.1038/s41467-026-68570-6
Parole chiave: Carcinoma mammario ER-positivo, Inibitori CDK4/6, Resistenza endocrina, Biomarcatori tumorali, palbociclib anastrozolo