Clear Sky Science · it
Forzare la parete cellulare per una consegna efficiente di DNA nelle diatomee
Alghe come piccole fabbriche verdi
Le diatomee — alghe microscopiche che fluttuano negli oceani — producono silenziosamente circa un quinto del carbonio organico del pianeta, contribuendo a nutrire le reti alimentari marine e a sequestrare anidride carbonica. Gli scienziati vorrebbero trasformare questi organismi resistenti e a crescita rapida in piccole fabbriche verdi per la produzione di carburanti, alimenti e prodotti chimici di pregio. Ma c’è stato un importante ostacolo: è sorprendentemente difficile introdurre nuovo DNA nelle cellule di diatomee in modo affidabile. Questo studio affronta direttamente il problema pratico, descrivendo nuovi metodi per far passare istruzioni genetiche e strumenti di editing genomico oltre il robusto rivestimento esterno delle diatomee.
Ammorbidire il guscio dei microrganismi oceanici
Il lavoro si concentra sulla diatomea modello Phaeodactylum tricornutum, molto usata nei laboratori perché il suo genoma è ben mappato e sono già disponibili alcuni strumenti genetici di base. Gli autori hanno ritenuto che la parete cellulare, la prima barriera fisica che qualsiasi DNA deve attraversare, fosse un collo di bottiglia cruciale. Trattando le cellule con un enzima chiamato alcalase, hanno rimosso parzialmente o completamente questa parete, creando «sferoplasti» e «protoplasti» fragili molto più facili da penetrare. Applicando poi l’elettroporazione — brevi impulsi elettrici che aprono pori temporanei — il numero di trasformanti riusciti è aumentato drasticamente, di circa due ordini di grandezza rispetto ai metodi precedenti. Anche quantità minime di DNA, dell’ordine di un nanogrammo, sono risultate sufficienti per recuperare cellule ingegnerizzate. 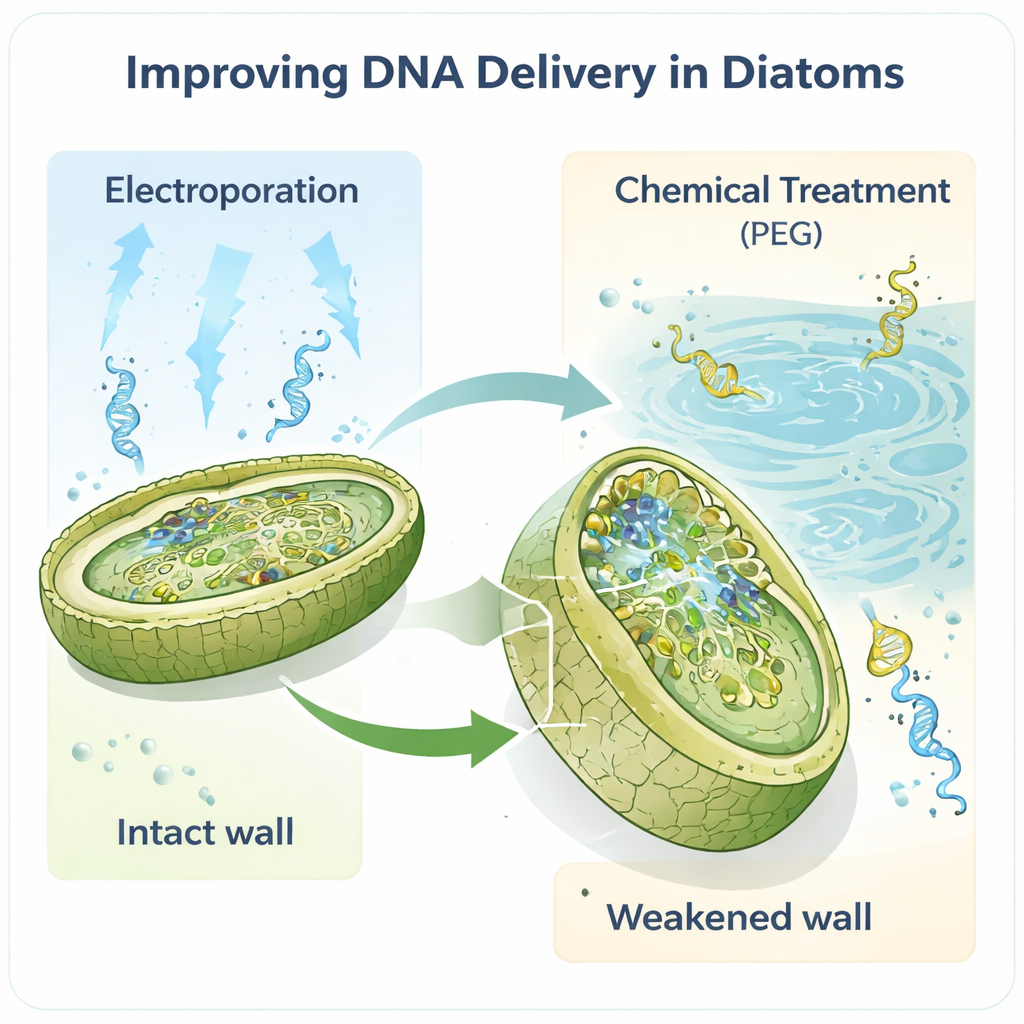
Consegna rapida di DNA senza passaggi attraverso i batteri
I metodi tradizionali per modificare le diatomee spesso si affidano a «corrieri» batterici per trasportare grandi molecole circolari di DNA, chiamate episomi, nelle alghe. Pur essendo efficace, questo approccio è lento, tecnicamente impegnativo e può destabilizzare costrutti di DNA delicati. I nuovi protocolli mostrano che sia l’elettroporazione sia un metodo chimico a base di polietilenglicole (PEG) raffinato possono trasferire gli episomi direttamente nelle diatomee, bypassando la tappa batterica. Sorprendentemente, episomi lunghi fino a 55,6 kilobasi sono stati consegnati e recuperati intatti. Le stesse strategie hanno funzionato anche in una seconda specie, Thalassiosira pseudonana, che possiede una parete più mineralizzata, suggerendo che si tratti di un kit di strumenti di ampia applicabilità piuttosto che di un trucco valido per una sola specie.
Lasciare che la cellula costruisca i propri cerchi genetici
Indagando sul comportamento del DNA introdotto tramite elettroporazione, il team ha scoperto un talento sorprendente: le diatomee possono unire frammenti di DNA autonomamente. Pezzi lineari di episomi entravano nella cellula e venivano riparati in circoli sia tramite giunzioni imprecise «non omologhe» sia tramite riparazione più accurata guidata da sovrapposizioni, detta «homology‑directed repair». Gli autori hanno definito questo processo «assemblaggio in vivo nelle diatomee», o DIVA. Progettando frammenti con sovrapposizioni, hanno indotto le cellule ad assemblare due, tre o quattro pezzi in episomi completi con alti tassi di successo, talvolta incorporando anche piccole cassette sintetiche che aggiungono etichette fluorescenti o nuove funzioni. Questa capacità trasforma il nucleo della diatomea in un piccolo laboratorio di assemblaggio del DNA, potenzialmente sostituendo fasi di assemblaggio laboriose che solitamente si fanno in lievito o in E. coli.
Modificare i genomi solo con complessi proteici
Oltre all’aggiunta di episomi, i ricercatori hanno mostrato di poter consegnare complessi proteina‑RNA CRISPR–Cas9 già pronti direttamente nelle cellule di diatomee usando l’elettroporazione ottimizzata. Mirando a un gene chiamato PtAPT, che determina la sensibilità a un analogo tossico dell’adenina, hanno generato migliaia di mutanti resistenti senza introdurre DNA addizionale nel genoma. Molti di questi mutanti presentavano piccole inserzioni o delezioni nel sito bersaglio; alcuni hanno persino catturato frammenti di DNA «corriere» che erano stati aggiunti per attenuare lo shock elettrico. Il team ha poi co‑consegnato complessi CRISPR ed episomi in un unico passaggio, riscontrando che circa una colonia su dieci portava sia una modifica genomica sia un episoma selezionabile — un modo efficiente per tracciare cambiamenti genetici altrimenti invisibili. 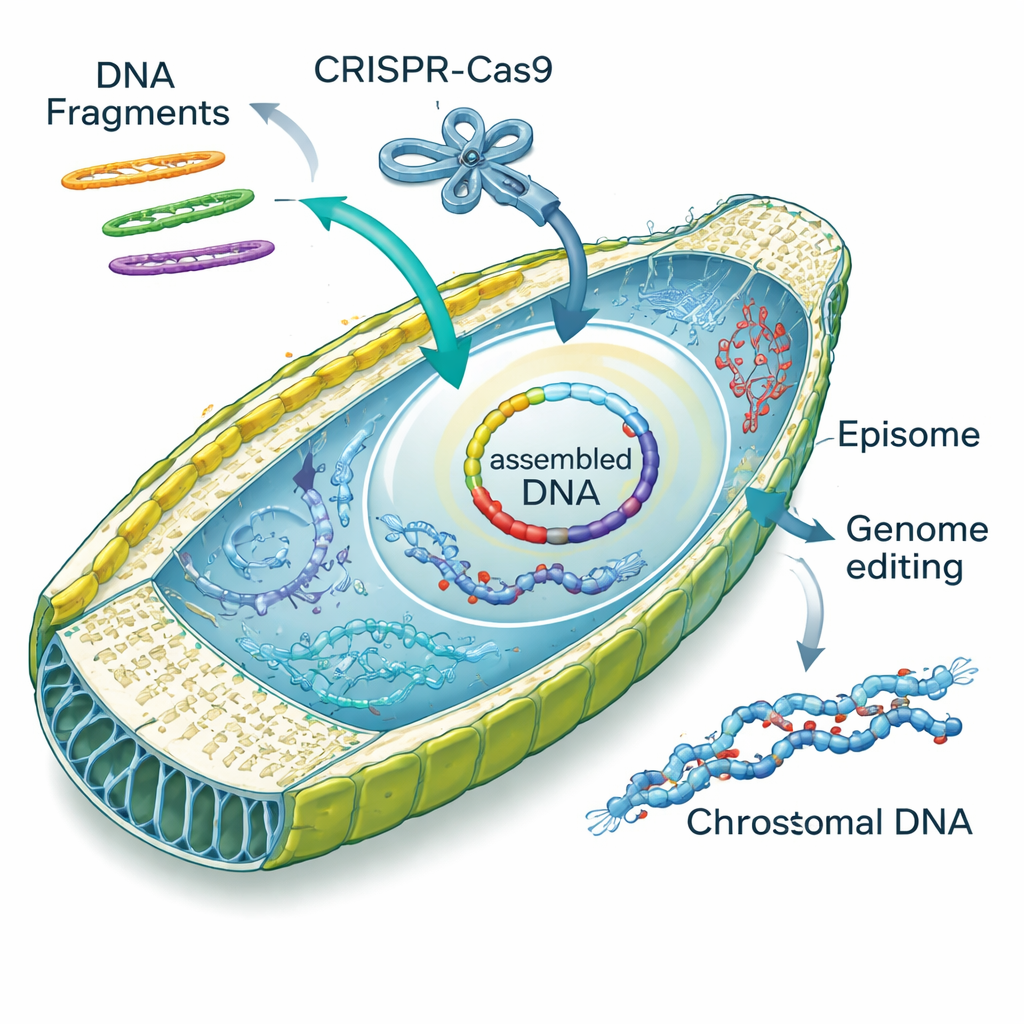
Verso diatomee su misura per un futuro sostenibile
Per i non specialisti, il messaggio chiave è che le diatomee si stanno avvicinando molto a diventare organismi pratici e programmabili. Ammorbidendo o rimuovendo con delicatezza la parete cellulare, gli autori hanno trasformato un processo pignolo e a basso rendimento in una pipeline robusta che utilizza piccole quantità di DNA, funziona con grandi costrutti genetici e permette persino alla cellula di assemblare e modificare il proprio DNA. Questi progressi accorciano il percorso da una sequenza progettata al computer a un ceppo vivo e testato. Sul lungo periodo, tali strumenti potrebbero accelerare gli sforzi per costruire diatomee con cromosomi interamente sintetici e sfruttare questi microrganismi oceanici per carburanti più puliti, chimica a minor impatto climatico e nuove scoperte biologiche.
Citazione: Walker, E.J.L., Pampuch, M., Deng, L. et al. Breaking the cell wall for efficient DNA delivery to diatoms. Nat Commun 17, 1848 (2026). https://doi.org/10.1038/s41467-026-68562-6
Parole chiave: biotecnologia delle diatomee, trasformazione genetica, editing genomico CRISPR, biologia sintetica, ingegneria delle microalghe