Clear Sky Science · it
Strutture della telomerasi umana legata a nucleotidi in diversi passaggi del suo ciclo di aggiunta dei ripetuti del DNA telomerico
Perché contano le estremità dei nostri cromosomi
Ogni volta che una cellula si divide, i cappucci protettivi alle estremità dei nostri cromosomi — detti telomeri — si accorciano un po'. Se diventano troppo corti, le cellule smettono di dividersi o funzionano male, contribuendo all’invecchiamento e alle malattie. Una macchina molecolare chiamata telomerasi può ricostruire questi cappucci ed è insolitamente attiva nella maggior parte dei tumori. Questo studio rivela, con dettaglio senza precedenti, come la telomerasi umana afferra ed estende i telomeri passo dopo passo, offrendo indizi su come potremmo un giorno modulare questo enzima in disturbi legati all’età e nel cancro.
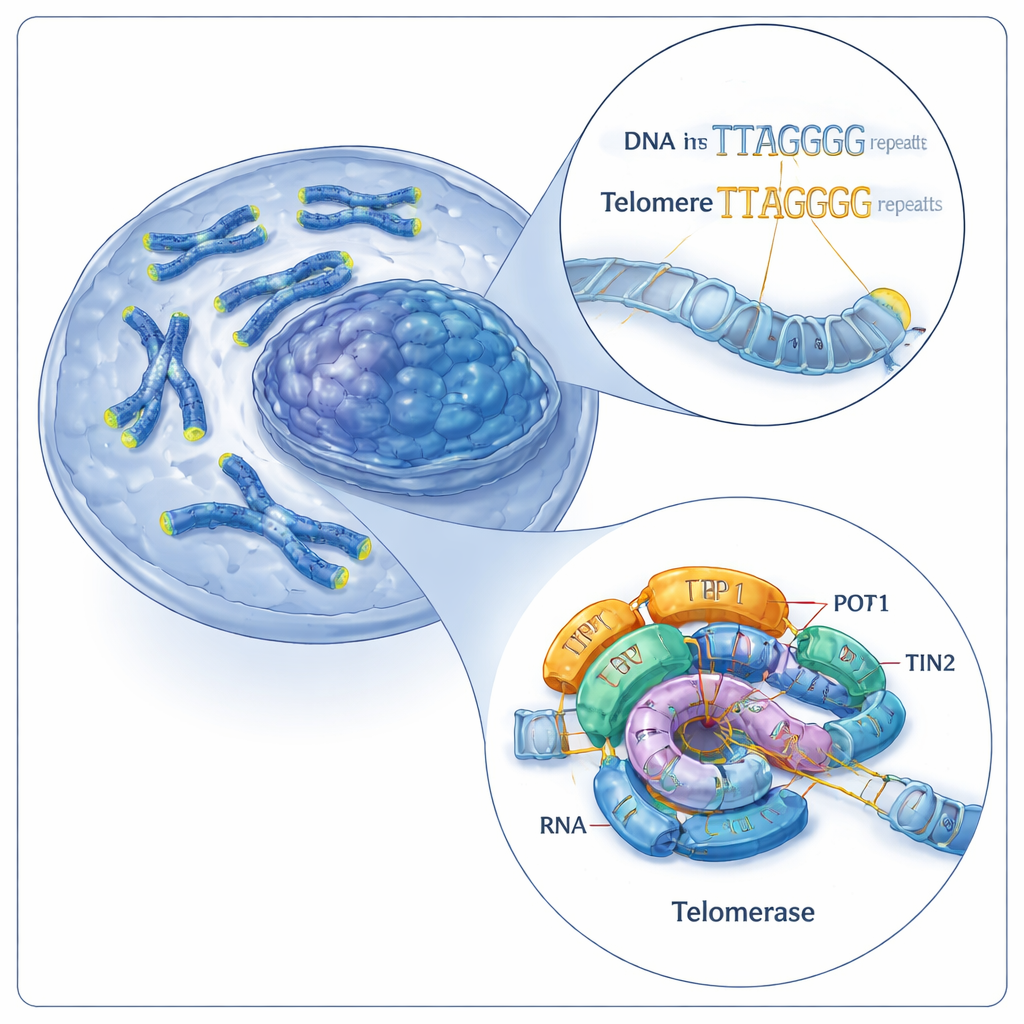
La squadra che ripara i cappucci cromosomici
I telomeri sono composti da brevi sequenze di DNA ripetute (negli esseri umani, un motivo di sei lettere: TTAGGG). La telomerasi allunga i telomeri aggiungendo altre di queste ripetizioni alle estremità dei cromosomi. Lo fa tramite due parti principali: una proteina chiamata telomerasi reverse transcriptasi (TERT) e una molecola di RNA incorporata (hTR) che funge da stampo. Insieme queste componenti formano un nucleo catalitico, ulteriormente assistito da proteine accessorie note come shelterin, incluso un trio chiamato TPP1–POT1–TIN2. Lavori precedenti avevano visualizzato la telomerasi umana in un solo stato operativo, lasciando aperta una domanda fondamentale: come fa questa macchina ad aggiungere ripetizioni ripetutamente senza staccarsi dal DNA?
Congelare la telomerasi in azione
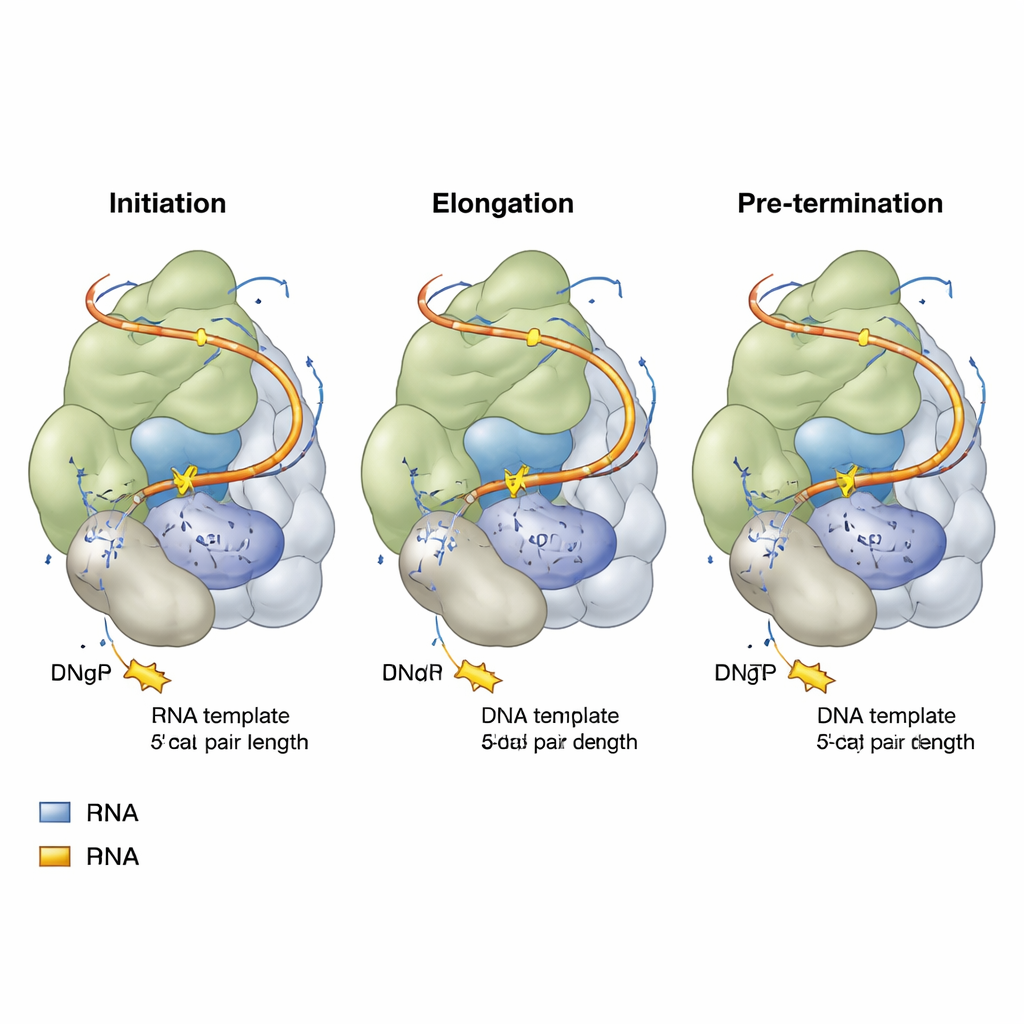
I ricercatori hanno ricostruito la telomerasi umana in cellule umane e poi l’hanno assemblata con pezzi di DNA telomerico progettati appositamente e analoghi di nucleotidi non reattivi — molecole che assomigliano alle lettere del DNA ma non possono essere incorporate completamente. Usando la crio‑microscopia elettronica ad alta risoluzione, hanno catturato istantanee della telomerasi in tre fasi chiave del suo ciclo di aggiunta di ripetuti: l’inizio (iniziazione), la fase centrale della copia (elongazione) e poco prima di completare una ripetizione (pre‑terminazione). Ogni istantanea mostrava il nucleo catalitico della telomerasi che abbraccia un breve ibrido DNA‑RNA, con un nucleotide in arrivo posizionato nel sito attivo, pronto per essere aggiunto al filamento di DNA in crescita.
Una piccola cerniera che controlla un grande processo
In tutte e tre le fasi è emerso un tema sorprendente: l’ibrido DNA‑RNA all’interno della telomerasi rimane essenzialmente della stessa lunghezza — solo quattro coppie di basi, temporaneamente estese a cinque quando entra un nuovo nucleotide. Un amminoacido specifico in TERT, soprannominato “testa‑cerniera”, segna costantemente la fine di questo breve ibrido e ne impedisce l’allungamento. Man mano che nuove lettere di DNA vengono aggiunte, una coppia di basi all’estremità lontana si scioglie, perciò l’ibrido non si estende mai oltre questa finestra ristretta di quattro‑cinque coppie. Questo design compatto probabilmente facilita la separazione e lo scorrimento dei filamenti, permettendo all’enzima di avanzare e iniziare la ripetizione successiva senza lasciar completamente il DNA. Sottili differenze nelle lettere del DNA e dell’RNA che occupano questo breve ibrido spiegano perché alcune sequenze terminali legano la telomerasi più saldamente di altre.
Linker di RNA flessibili e parti mobili
Il filamento di RNA stampo all’interno della telomerasi non fluttua liberamente; è ancorato da tratti flessibili su entrambi i lati, chiamati linker dello stampo 5′ e 3′. Quando la telomerasi progredisce dall’iniziazione alla pre‑terminazione, il linker a monte (5′) viene tirato come una corda elastica, raggiungendo infine uno stato completamente teso che contribuisce a segnalare la fine di una ripetizione. Nel frattempo, il linker a valle (3′) si rigonfia verso l’esterno e si avvicina a un’altra struttura dell’RNA (il cappio P6.1) e a regioni proteiche vicine. Se questi linker diventano troppo corti o troppo lunghi, o se P6.1 è alterato, la capacità della telomerasi di aggiungere ripetizione dopo ripetizione diminuisce fortemente. È importante che certe regioni proteiche — il dominio TEN e un inserto specifico della telomerasi chiamato cuneo TRAP — agiscano come guide regolabili, entrando in contatto sia con il DNA sia con questi linker di RNA. Mutazioni che riducono l’ingombro del cuneo TRAP possono in realtà rendere l’enzima più processivo, suggerendo che questo cuneo funge normalmente da barriera controllata che temporizza il movimento dello stampo.
Nuove intuizioni su un bersaglio terapeutico
Combinando istantanee strutturali con test funzionali di mutazioni mirate, lo studio propone un modello meccanico dettagliato su come la telomerasi umana allunghi ripetutamente i telomeri. L’enzima mantiene un ibrido DNA‑RNA molto corto, usa un residuo a forma di cerniera per imporne la lunghezza e si affida a linker di RNA flessibili e a elementi proteici mobili per avanzare lo stampo e mantenere il DNA ancorato durante molteplici cicli di copia. Per i non specialisti, il messaggio chiave è che la telomerasi non funziona come una macchina di copia statica ma come un dispositivo finemente tarato e caricato a molla la cui geometria e parti mobili determinano quanto e quanto efficacemente può mantenere i telomeri. Comprendere questa coreografia apre la porta a farmaci che potrebbero o attenuare la telomerasi nei tumori o stabilizzarne la funzione nelle malattie da invecchiamento prematuro.
Citazione: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
Parole chiave: telomerasi, telomeri, crio‑EM, stabilità del genoma, biologia del cancro